Rhumatologie
Réunion annuelle de 2017 de l’ACR et de l’ARHP
Nouvelles options thérapeutiques dans la polyarthrite rhumatoïde : un virage vers la sélectivité envers la JAK1
San Diego – Forts d’une plus grande sélectivité pour la JAK1, les nouveaux inhibiteurs des JAK opposés à la polyarthrite rhumatoïde (PR) en sont aux dernières étapes des études cliniques. Des quatre enzymes JAK, c’est la JAK1 qui est la plus étroitement reliée à une régulation positive des cytokines inflammatoires incriminées dans la PR. Par cette plus grande sélectivité, on ne cherche pas uniquement à mieux inhiber ces cytokines, mais aussi à raréfier les effets indésirables collatéraux. Ces agents de nouvelle génération se montrent efficaces dans les cas où les traitements de fond de synthèse, qu’ils soient classiques ou biologiques, ne maîtrisent pas bien la maladie. Les données sur les nouveaux agents présentées lors de la réunion de 2017 de l’ACR comprenaient, entre autres, des résultats d’études de phase III.
Les nouveaux agents en voie d’homologation par les instances réglementaires
Se fondant sur l’utilité clinique du tofacitinib, l’inhibiteur de JAK actuellement homologué, les chercheurs ont créé une nouvelle génération de ces agents alliant une plus grande efficacité à une meilleure innocuité. L’upadacitinib, le baricitinib et le filgotinib comptent parmi ceux qui sont en voie d’être homologués par les instances réglementaires. Ces agents se distinguent les uns des autres par leur sélectivité pour la JAK1 et pourraient ne pas être interchangeables. Cela dit, les données recueillies, y compris celles tirées d’études de phase III, témoignent de taux élevés de maîtrise de la maladie chez des patients obtenant des résultats médiocres avec les autres options thérapeutiques. De plus, les données sur leur innocuité sont encourageantes. Deux études contrôlées par placebo s’inscrivant dans le programme SELECT, qui est composé de six études de phase III sur l’upadacitinib, ont été présentées lors de la réunion de l’ACR et de l’ARHP de cette année. L’une d’elles, qui s’intitule SELECT-BEYOND et qui a fait l’objet d’une présentation de dernière heure, a été menée chez des patients dont le traitement par au moins un agent biologique avait échoué. L’autre, intitulée SELECT-NEXT, a été réalisée chez des patients réfractaires aux traitements de fond de synthèse classiques. Les sujets de ces deux études ont été affectés aléatoirement à des doses uniquotidiennes de 15 mg ou de 30 mg d’upadacitinib ou d’un placebo par voie orale. Or les courbes rendant compte de la réaction au traitement ont presque immédiatement donné l’avantage au traitement actif dans ces deux études.
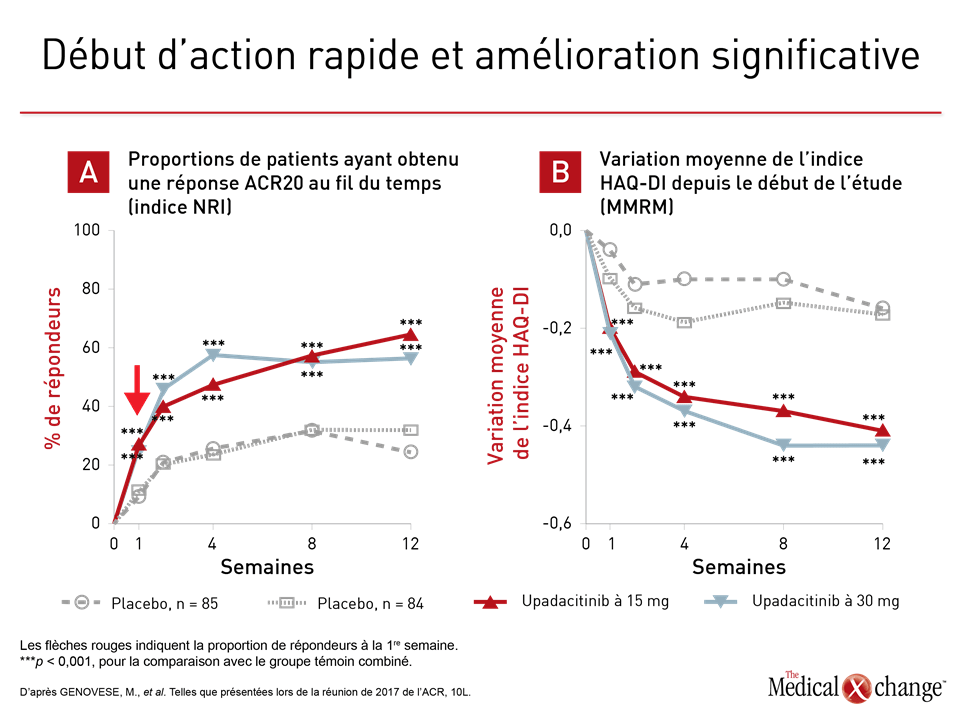
L’amélioration spectaculaire de la maîtrise de la maladie, dont témoignent de nombreux paramètres de mesure, cadre avec l’entrée en jeu rapide de la sélectivité pour la JAK1.
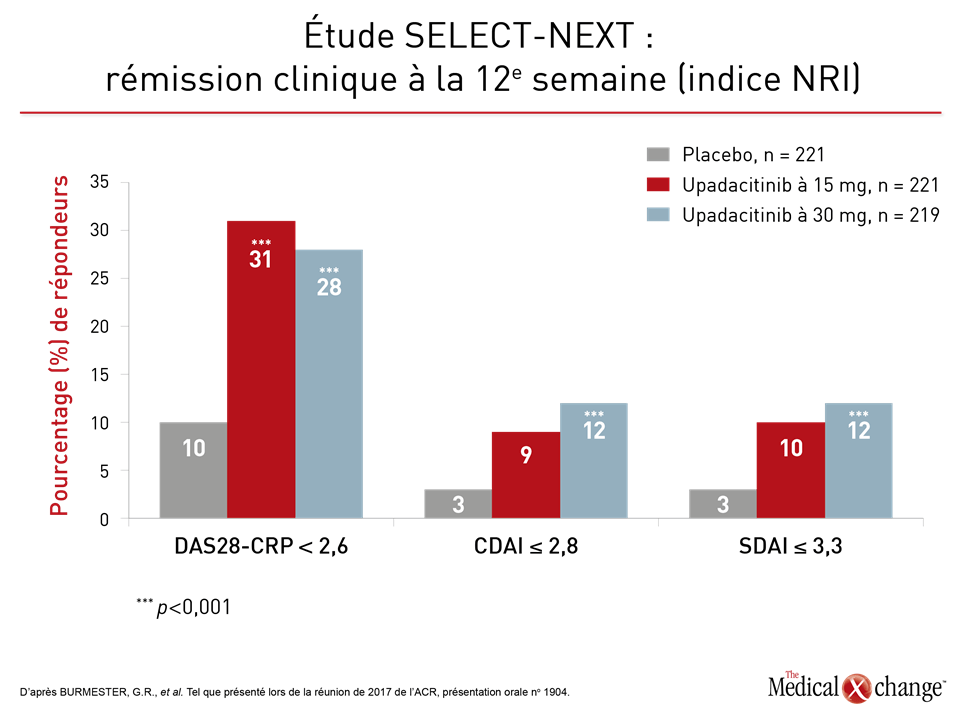
« Le médicament a commencé à agir remarquablement vite, des bienfaits significatifs sur le plan statistique ayant été notés dans les deux groupes traités par l’upadacitinib dès la première semaine », a rapporté le clinicien-chercheur principal de l’étude SELECT-BEYOND, le Dr Mark Genovese, Codirecteur de la Division d’immunologie et de rhumatologie, de l’université Stanford, de Stanford, en Californie. L’amélioration spectaculaire de la maîtrise de la maladie, dont témoignent de nombreux paramètres de mesure, cadre avec l’entrée en jeu rapide de la sélectivité pour la JAK1 (Fig. 1a et 1b). Des patients ont mis un terme à leur biothérapie, mais ont continué de recevoir des doses stables d’un traitement de fond de synthèse classique pendant l’étude. Les patients pouvaient être admis à l’étude SELECT-BEYOND s’ils avaient été traités, mais en vain, avec un agent biologique ou plus, qu’ils aient appartenu à la même classe de médicaments ou non. Environ 25 % des 499 sujets s’étant prêtés au processus de répartition aléatoire avaient subi un traitement par deux de ces agents, mais sans succès et une autre tranche de 25 % en avait reçu au moins trois avec le même résultat. Malgré cela, 65 % et 56 % des sujets affectés aux doses de 15 et de 30 mg d’upadacitinib avaient obtenu une réponse ACR20 à la 12e semaine. Les taux de réponse ACR50 et ACR70 ont été respectivement de 34 % et de 36 %, et de 12 % et de 23 %. Selon le Dr Genovese, les taux de réponse étaient similaires chez les sujets ayant connu le plus grand nombre d’échecs avec des biothérapies de fond que chez ceux qui en avaient connu le moins. L’étude SELECT-NEXT, qui a été réalisée chez 661 patients réfractaires aux traitements de fond de synthèse classiques affectés aléatoirement à des doses de 15 et de 30 mg d’upadacitinib ou d’un placebo, a permis de constater des résultats analogues, dont l’obtention rapide d’une réponse. Bien qu’à la 12e semaine de l’étude SELECT-NEXT, les patients traités par les doses de 15 et de 30 mg d’upadacitinib aient manifesté une réponse ACR20 dans des proportions semblables à ceux de l’étude SELECT-BEYOND, il n’en demeure pas moins qu’ils ont été légèrement plus nombreux à montrer une réponse ACR50 (38 % et 43 %, respectivement) et ACR70 (21 % et 27 %). Le soulagement des symptômes à la 12e semaine : un constat répété « Les patients en rémission clinique à la 12e semaine de traitement par l’upadacitinib étaient environ trois fois plus nombreux que les témoins, que nous ayons utilisé le score DAS-CRP ou les indices CDAI ou SDAI comme paramètres de mesure », a déclaré le clinicien-chercheur principal de cette étude, le Dr Gerd R. Burmester, Professeur de rhumatologie et d’immunologie clinique, à l’hôpital de la Charité, de l’Université de Berlin, en Allemagne (Fig. 2).
« Les patients en rémission clinique à la 12e semaine de traitement par l’upadacitinib étaient environ trois fois plus nombreux que les témoins. »
Au cours des 12 premières semaines de l’étude SELECT-BEYOND, le taux total des effets indésirables (56,2 % vs 55,5 %) et le taux d’abandons pour cause d’effets indésirables (5,2 % vs 2,4 %) étaient légèrement plus élevés dans le groupe témoin que dans le groupe traité par l’upadacitinib à 15 mg. Ils étaient plus élevés (67,3 % et 9,1 %, respectivement) chez les patients ayant pris l’upadacitinib à 30 mg. Lors de l’étude SELECT-NEXT, dans l’ensemble, le taux global d’abandons motivés par des effets indésirables était plus bas dans le groupe témoin et dans le groupe traité par l’upadacitinib à 15 mg (3,2 % pour les deux) que dans celui ayant reçu la dose de 30 mg d’upadacitinib (5,9 %). Compte tenu de ceux qui avaient été signalés avec les inhibiteurs de JAK précédents, les effets indésirables d’intérêt ont été rassurants. À preuve, les taux de zona enregistrés pendant l’étude SELECT-BEYOND ont été plus élevés dans le groupe traité par l’upadacitinib à 30 mg (2,4 %), mais identiques dans le groupe témoin et celui traité par l’upadacitinib à 15 mg (0,6 %). Pendant l’étude SELECT-NEXT, un seul cas de zona a été répertorié chez les témoins et les patients prenant la dose de 15 mg d’upadacitinib, et deux chez les patients traités par la dose de 30 mg, alors qu’aucun cas d’embolie pulmonaire (EP) ou de thromboembolie veineuse profonde (TEVP) n’a été rapporté. Ces derniers ont été plus fréquents dans les groupes de traitement actif de l’étude SELECT-BEYOND, mais le Dr Genovese a tenu à expliquer que les facteurs de risque préexistants font en sorte que le risque est plus difficile à cerner. Aucune tendance ne s’est dessinée quant à l’apparition d’une EP ou d’une TEVP en rapport avec l’amorce du traitement par l’upadacitinib. Les différences mesurées pour l’hémoglobinémie et la plaquettémie pendant le traitement n’étaient significatives dans aucune des deux études.
Les effets indésirables ayant un lien avec la sélectivité pour les JAK
Ces effets indésirables particuliers présentent un grand intérêt, car la sélectivité pour les JAK pourrait réduire le risque d’effets indésirables collatéraux. La JAK1 active les cytokines pro-inflammatoires telles que l’interleukine-6 (IL-6) et l’interféron par la voie de signalisation JAK-STAT (Signal transducer and activator of transcription). Ces derniers sont incriminés dans l’inflammation qui accompagne non seulement la PR, mais aussi d’autres maladies inflammatoires comme le psoriasis. Les trois autres isoformes, JAK2, JAK3 et TYK2 (le quatrième membre de la famille des enzymes JAK), ont un lien avec d’autres fonctions biologiques, soit respectivement l’hématopoïèse, la fonction lymphocytaire et la régulation de l’interféron, de l’IL-12 et de l’IL‑23. Comparativement au tofacitinib, qui exerce son activité inhibitrice sur d’autres JAK hormis la JAK1 et surtout sur la JAK3, les nouveaux inhibiteurs plus sélectifs des JAK qui en sont aux derniers stades des programmes d’essais cliniques et leur profil d’activité possiblement plus ciblé sont surveillés de près. Il faudra réaliser des comparaisons à grande échelle des médicaments dotés de profils différents quant à l’inhibition des enzymes JAK pour prouver cette hypothèse, mais les études menées jusqu’à maintenant sur les agents de nouvelle génération donnent à penser que leur activité anti-inflammatoire pourrait se comparer à celle de cet agent de première génération. Ce sont, entre autres, le baricitinib, dont les résultats des études de phase III ont été annoncés il y a presque un an, et le filgotinib pour lequel les études de phase III sont en cours. Les instances réglementaires européennes ont déjà homologué le baricitinib pour le traitement de la PR bien qu’il inhibe lui aussi la JAK2 et qu’il soit moins sélectif que l’upadacitinib et que le filgotinib.
Les résultats obtenus avec le baricitinib aux 12e et 24e semaines
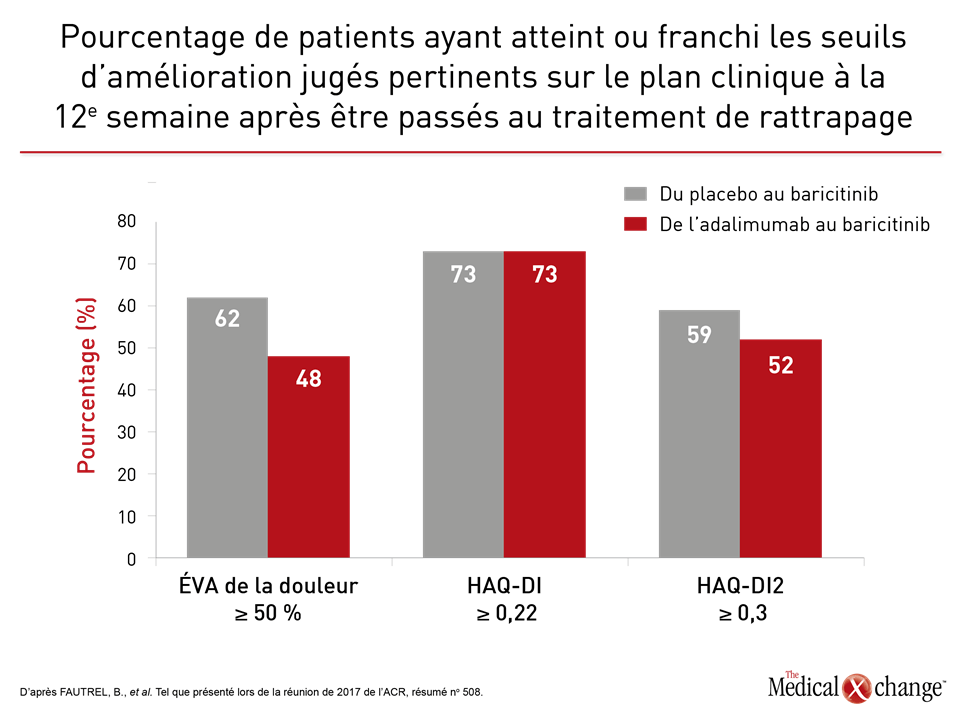
« Les différences observées entre le baricitinib et l’adalimumab ont franchi le seuil de la signification statistique aux 12e et 24e semaines pour plusieurs mesures cliniques », a déclaré le Dr Peter Nash, du Département de rhumatologie et d’immunologie de l’Université du Queensland, à Brisbane, en Australie. Il parlait notamment de l’indice CDAI global moyen (Clinical Disease Activity Index) obtenu à la 12e semaine (p = 0,008) et à la 24e semaine (p = 0,035), ainsi que du nombre de patients ayant connu une amélioration de leur score CDAI moyen équivalant à 12 ou plus aux mêmes intervalles de mesure (p < 0,001 et p < 0,010). Au cours de l’étude RA-BEAM, 1355 patients ayant réagi de façon insatisfaisante au méthotrexate ont été répartis aléatoirement de façon à prendre des doses uniquotidiennes de 4 mg de baricitinib par voie orale, un placebo ou des doses de 40 mg d’adalimumab toutes les deux semaines. Les données présentées par le Dr Nash pendant la réunion de l’ACR étaient tirées d’analyses secondaires ou réalisées a posteriori consacrées à l’activité de ce médicament. Dans une autre étude présentée par le Dr Bruno Fautrel, du Département de rhumatologie et d’immunologie, de l’université Pierre et Marie Curie, de Paris, en France, les bienfaits du traitement ont été évalués chez les sujets que la répartition aléatoire avait d’abord affectés au placebo ou à l’adalimumab et qui ont ensuite suivi un traitement de rattrapage par le baricitinib. Bien que seulement 12 % des sujets traités par l’adalimumab soient passés au traitement de rattrapage comparativement à 26 % de ceux ayant reçu le placebo, ils ont tous obtenu une amélioration de leur état à peu de chose près identique après ce remplacement, et ce pour plusieurs paramètres d’évaluation (Fig. 3). « Lorsque le traitement par l’adalimumab échoue, un traitement de rattrapage par le baricitinib permet de maîtriser la maladie rapidement et d’atténuer les symptômes importants aux yeux des patients », a soutenu le Dr Fautrel.
Les résultats d’une méta-analyse sur l’innocuité du baricitinib sont rassurants
Les résultats d’une méta-analyse sur l’innocuité du baricitinib réalisée à partir de cinq études menées chez 2006 patients sont encourageants. Comparativement au placebo, le baricitinib a été relié à une hausse modeste du risque relatif approché (RRA) calculé pour le risque global de tous les effets indésirables confondus (RRA : 1,35; p = 0,05), mais à aucune augmentation des effets indésirables graves (RRA : 1,12; p = 0,58). « L’innocuité du baricitinib ne semble pas avoir suscité quelque inquiétude que ce soit pendant les six premiers mois où il a été administré », a conclu l’auteur principal de cette méta-analyse, le Dr Sumit Kunwar, du département de rhumatologie, du Centre hospitalier MedStar Washington, à Washington, D.C. Cette observation cadre avec la réduction possible des effets indésirables collatéraux attribuable à la sélectivité des inhibiteurs des JAK. Des données prometteuses aussi été présentées sur l’innocuité du filgotinib lors de la réunion de 2017 de l’ACR. Selon les données recueillies pendant le long suivi de l’étude DARWIN3, une étude de prolongation menée en mode ouvert pour laquelle ont été recrutés des participants aux études de phase IIb DARWIN1 et DARWIN2, aucune variation n’a été relevée dans un large éventail d’analyses de laboratoire pendant les 917 jours (médiane) d’administration du médicament. Quelque 520 des 603 patients admis à l’étude DARWIN3 y ont participé pendant au moins 84 semaines.
L’innocuité du filgotinib pour ce qui est des effets indésirables collatéraux
Dans cette analyse, le taux d’effets indésirables a été stratifié en fonction de la dose de filgotinib (100 mg 2 fois par jour ou 200 mg une fois par jour) et de l’administration ou non de méthotrexate. Les chercheurs ont bel et bien constaté un effet proportionnel à la dose, ce qui explique que les effets indésirables graves et les anomalies analytiques de grade 2 ou plus ont été plus fréquents avec les doses plus fortes, mais les effets indésirables de grade 3 ou plus ont été rares, y compris ceux qui auraient pu avoir un lien avec une inhibition aspécifique des JAK, notamment une variation de l’hémoglobinémie, de l’activité lymphocytaire, de la plaquettémie et de la fonction rénale.
« Le bilan d’innocuité du filgotinib est resté favorable au fil du temps. »
« Le bilan d’innocuité du filgotinib est resté favorable au fil du temps, a affirmé le Dr Genovese, qui a aussi présenté ces résultats sur le filgotinib. Dans une perspective d’efficacité durable qui a d’ailleurs été observée aussi au cours de ce suivi à long terme, il a ajouté que les résultats obtenus plaident en faveur de la poursuite des programmes d’études cliniques de phase III.
Conclusion
Une nouvelle génération d’inhibiteurs des JAK dotés d’une plus grande sélectivité envers la JAK1, l’isoforme considérée comme la plus importante en ce qui concerne l’inflammation causée par la PR, en est aux dernières étapes des études cliniques. Or il se peut que la sélectivité de ces agents soit en rapport avec leur efficacité et leur innocuité. Il faudra certes réaliser des essais comparatifs pour vérifier cette hypothèse, mais l’efficacité et l’innocuité dont ont fait preuve ces agents dans les études cliniques sont prometteuses. Il s’agit notamment de deux études de phase III qui sont récemment arrivées à leur terme, l’une sur l’upadacitinib, un inhibiteur sélectif de la JAK1, et l’autre sur le baricitinib, un inhibiteur des JAK1 et JAK2 qui avait déjà franchi l’étape des études de phase III. Ces médicaments sont appelés à enrichir les options thérapeutiques offertes aux patients atteints de PR et peut-être même d’autres maladies inflammatoires.