rhumatologie
Réunion annuelle de 2018 de l’ACR et de l'ARHP
Les inhibiteurs de JAK pour voie orale pourraient supplanter les agents biologiques injectables dans le traitement de la PR
Chicago – De nouvelles données issues d’essais cliniques de phase III et présentées lors la réunion annuelle de 2018 de l’ACR/ARHP provoquent un virage dans la perception des nouveaux inhibiteurs de Janus kinases (JAK) pour voie orale. Ces agents pourraient en effet modifier la séquence des traitements opposés à la polyarthrite rhumatoïde (PR). Dans un de ces essais, un agent doté d’une sélectivité plus grande pour la voie de la JAK1 que pour les autres voies des JAK s’est révélé supérieur au placebo et à l’inhibiteur du facteur de nécrose tumorale (TNF) chez des patients dont la PR n’était pas bien maîtrisée avec le méthotrexate. Dans un autre essai, le même inhibiteur de JAK utilisé en première intention a fait preuve d’une grande efficacité et d’un effet protecteur contre l’évolution objectivée par radiographie. Lors du troisième essai, un agent différent, qui en est aux derniers stades des essais cliniques, s’est montré très actif dans des cas de réponse insatisfaisante ou d’intolérance à un traitement de fond biologique.
Les inhibiteurs de JAK expérimentaux prennent l’avance
Le tofacitinib, premier inhibiteur de JAK homologué pour le traitement de la PR, a maintenant pour vis-à-vis le baricitinib dans certains pays. Cette classe de médicaments est toutefois sur le point de s’enrichir de nouveaux inhibiteurs de JAK conçus pour cibler plus précisément la voie de la JAK1. L’upadacitinib, un des agents ayant fait l’objet d’essais de phase III mentionnés précédemment s’est révélé supérieur à un inhibiteur du TNF dans le cadre d’un traitement de deuxième intention.
« Selon moi, ces études provoquent un changement de paradigme », a affirmé le Dr Roy E. Fleischmann, Professeur clinicien de rhumatologie, au Southwestern Medical Center de l’Université du Texas, à Dallas. Faisant référence aux données sur les nouveaux agents, dont celles sur l’upadacitinib qu’il venait de présenter, ce chercheur a déclaré que, personnellement, il opterait pour un des inhibiteurs de JAK les plus actifs avant d’avoir recours à un inhibiteur du TNF, toutes choses étant par ailleurs égales, notamment les coûts. Il a ajouté : « L’upadacitinib semble supérieur au baricitinib et au tofacitinib, mais nous savons tous que ne pouvons faire pareille affirmation [tant qu’ils n’auront pas été comparés directement dans des essais cliniques] ».
« L’upadacitinib semble supérieur au baricitinib et au tofacitinib, mais nous savons tous que nous ne pouvons faire pareille affirmation [tant qu’ils n’auront pas été comparés directement dans des essais cliniques] ».
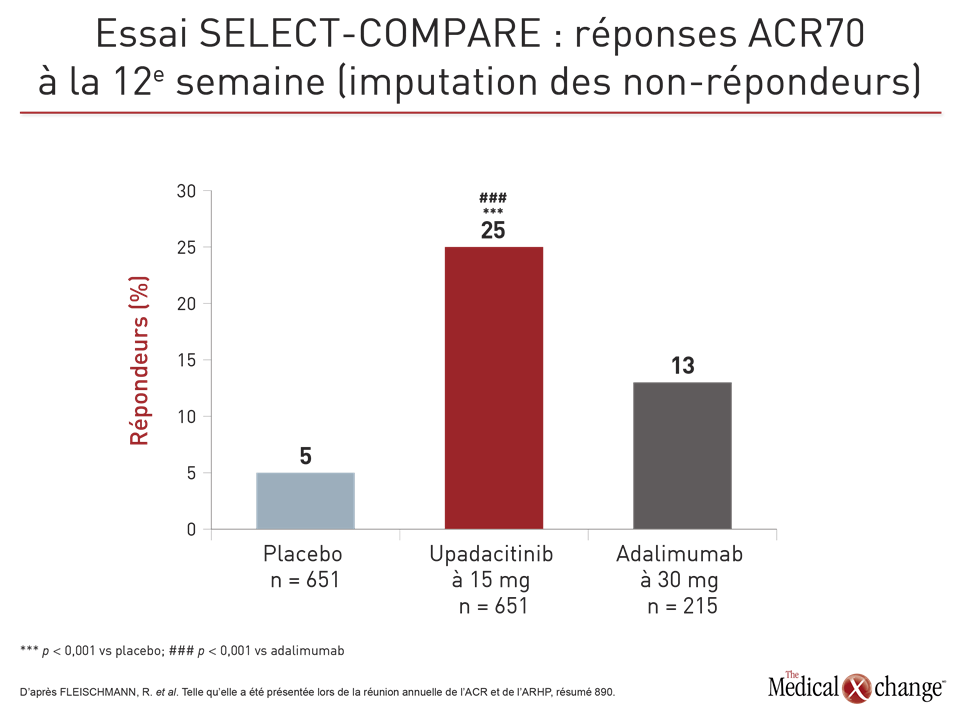
Les inhibiteurs de JAK n’ont pas encore fait l’objet d’essais comparatifs de grande envergure, mais d’après les résultats de l’essai SELECT-COMPARE présentés par le Dr Fleischmann, ils exerceraient un effet clinique plus prononcé. Lors de cet essai, 1629 patients atteints d’une PR évolutive mal maîtrisée par le méthotrexate ont été répartis aléatoirement de façon à recevoir 15 mg d’upadacitinib par voie orale une fois par jour ou 40 mg d’adalimumab (un inhibiteur du TNF) une semaine sur deux, ou un placebo, tout en continuant à prendre du méthotrexate.
Les résultats prometteurs de l’essai SELECT-COMPARE
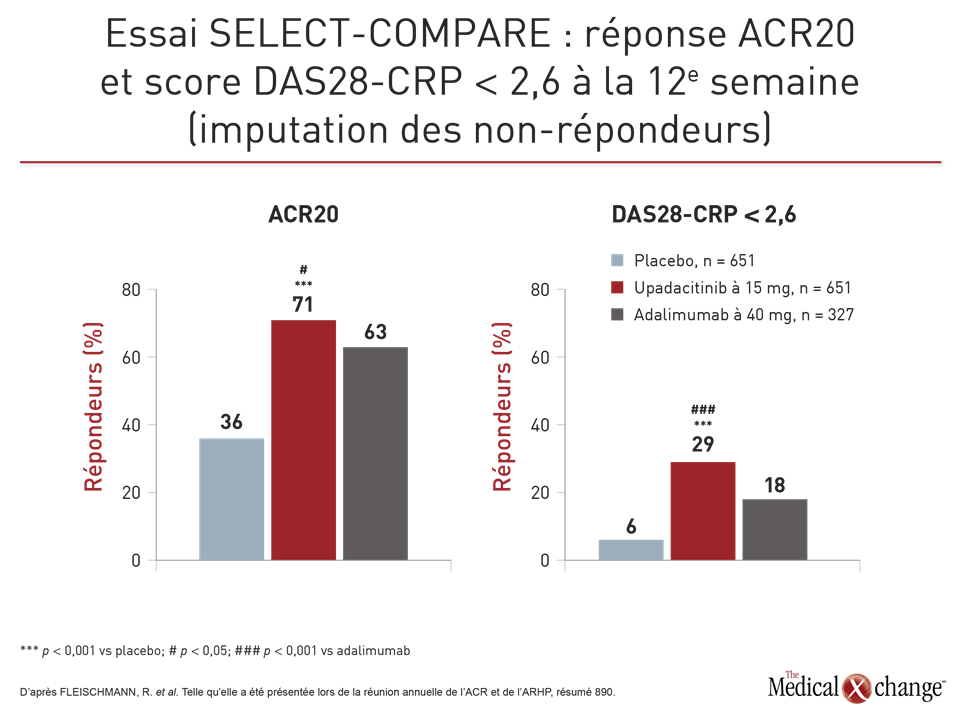
L’upadacitinib et l’adalimumab se sont montrés supérieurs au placebo pour ce qui est des deux paramètres d’évaluation principaux soit le taux de réponse ACR20 et d’obtention d’un score DAS28-CRP inférieur à 2,6 à la 12e semaine (Fig. 1). De plus, l’upadacitinib s’est révélé significativement plus efficace que l’adalimumab non seulement pour ces deux paramètres, mais aussi pour un large éventail d’autres mesures telles que l’indice CDAI (Clinical Disease Activity Index), les critères booléens définissant la rémission et divers résultats propres aux patients, comme ceux mesurés à l’aide du sommaire des composantes physiques du questionnaire SF-36 et de l’indice HAQ-DI (Health Assessment Questionnaire-Disability Index). En outre, le taux de réponse ACR70 obtenu avec l’upadacitinib était près de deux fois plus élevé (25 % vs 13 %; p < 0,001).
Une réponse rapide au traitement
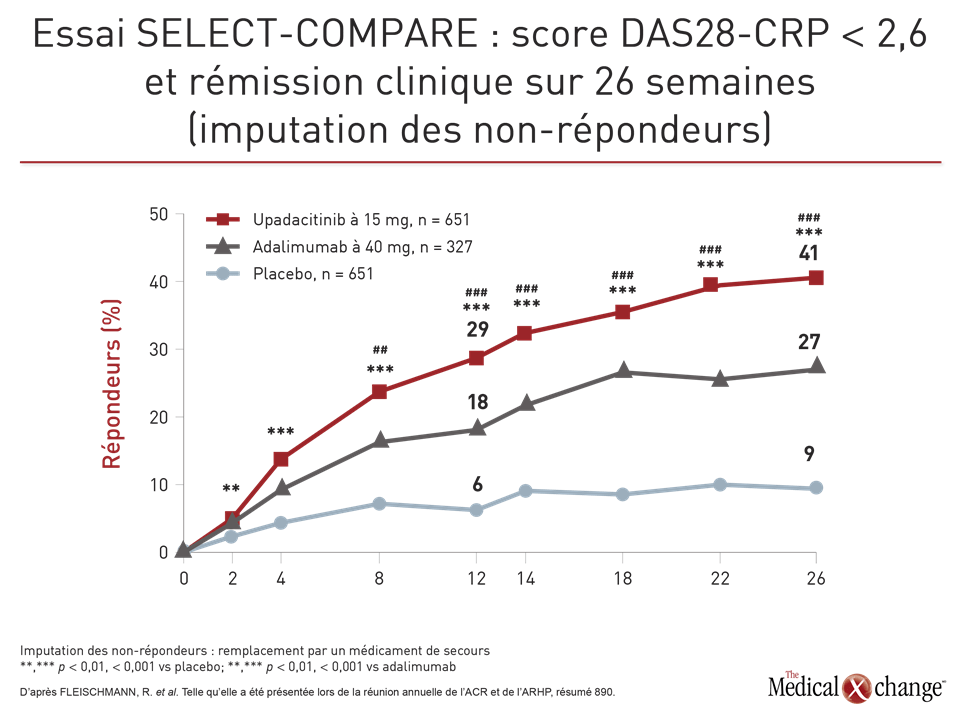
Les patients ont également répondu plus vite à l’upadacitinib qu’à l’adalimumab, même si la dose d’upadacitinib à l’étude dans cet essai était de 15 mg, alors qu’elle s’élevait à 30 mg dans les autres essais de phase III. Par exemple, la courbe de l’upadacitinib illustrant l’obtention d’un score DAS28-CRP inférieur à 2,6 a commencé à s’éloigner de celle des autres produits en quelques semaines, l’écart ayant atteint la signification statistique à la 8e semaine (p < 0,001), et a poursuivi sa course jusqu’à la fin de l’essai (Fig. 2).
« La réponse rapide des sujets à l’upadacitinib ne nous a pas surpris, puisque nous l’avions déjà constatée lors d’études précédentes. Nous nous attendions toutefois à ce que l’adalimumab rattrape son retard, mais il ne l’a jamais fait », a déclaré le Dr Fleischmann.
Le tofacitinib ne s’est pas montré supérieur à l’adalimumab lors d’un essai réalisé antérieurement selon un protocole similaire à celui de l’essai SELECT-COMPARE (VAN VOLLENHOVEN, R. F., et al. N Engl J Med, vol. 367, 2012, p. 508-519). Cela dit, le Dr Fleischmann met en garde contre les comparaisons trop rapides entre les essais et insiste sur le fait que des comparaisons directes restent essentielles.
L’essai SELECT-MONOTHERAPY porte sur les paramètres d’évaluation de l’efficacité de la FDA
Dans le cadre de l’essai SELECT-MONOTHERAPY, un autre essai de phase III de grande envergure sur l’upadacitinib, 648 patients ont été répartis aléatoirement de manière à poursuivre leur traitement par le méthotrexate ou à passer à l’upadacitinib à 15 ou à 30 mg. Si les objectifs principaux de l’essai, soit la détermination du taux de réponse ACR20 et d’obtention d’un score DAS28-CRP de 3,2 ou moins, ont été choisis, c’est qu’ils correspondent respectivement aux exigences réglementaires de la FDA des États-Unis et de l’Agence européenne des médicaments.
Selon le Dr Josef Smolen, Chef de la Division de rhumatologie, de l’Université de médecine de Vienne, en Autriche, les deux objectifs principaux et tous les objectifs secondaires ont été atteints.
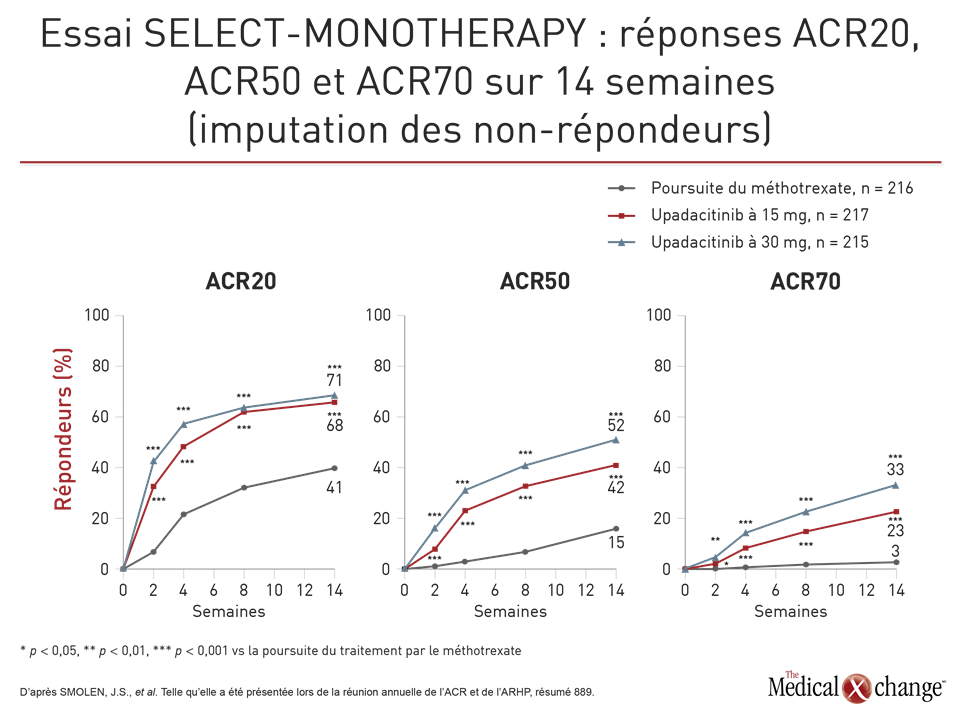
À la 14e semaine, le taux de réponse ACR20 s’élevait à 41 % dans le groupe poursuivant le traitement par le méthotrexate, alors qu’il se chiffrait à 68 % et à 71 % dans les groupes recevant les doses de 15 et de 30 mg d’upadacitinib. Pour ce qui est du score DAS-CRP de 3,2 ou moins, les taux s’établissaient à 19 %, à 45 % et à 53 %, respectivement. L’avantage relatif de l’upadacitinib était chaque fois extrêmement significatif sur le plan statistique (p < 0,001 pour les deux doses).
D’après le Dr Smolen, la réponse des sujets a été rapide tant pour ces paramètres que pour les réponses ACR50 et ACR70, ainsi que pour les indices HAQ-DI et CDAI. Par exemple, en deux semaines à peine, la proportion de patients affichant une réponse ACR50 était significativement plus forte chez ceux traités par l’upadacitinib, peu importe la dose administrée (p < 0,001). La proportion de patients ayant obtenu une réponse ACR70 était aussi plus forte et a franchi le seuil de la signification statistique à la 4e semaine.
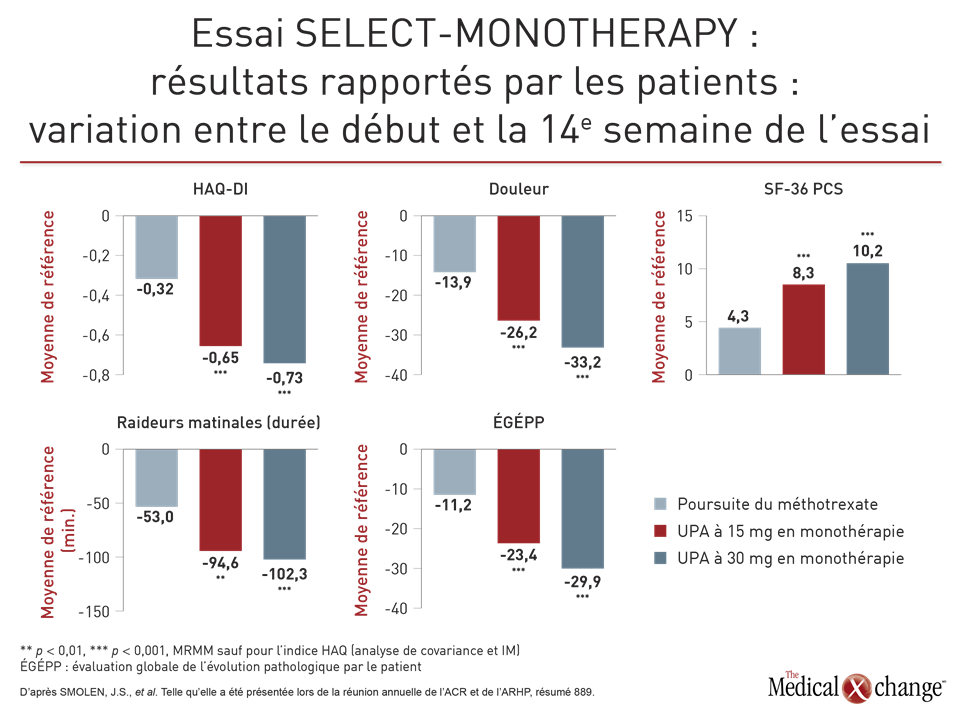
La perception des patients était à l’image de cette efficacité. Alors que le score HAQ-DI médian, qui était de 1,5 au début de l’essai, a baissé de 0,32 point seulement dans le groupe méthotrexate, celui du groupe upadacitinib à 30 mg a diminué de presque la moitié (0,73 point) et légèrement moins dans celui recevant la dose de 15 mg (0,65 point) (p < 0,001 pour les deux doses versus le méthotrexate).
Un bilan d’innocuité rassurant
L’upadacitinib a été bien toléré pendant ces essais sans que rien d’alarmant et de nouveau ou d’inattendu comparativement aux essais réalisés précédemment avec cet agent ou d’autres inhibiteurs de JAK ne soit signalé. En ce qui concerne les effets indésirables d’intérêt, tels que la thromboembolie veineuse (TEV) et le cancer, les chercheurs n’ont noté aucune différence significative entre le groupe traité par l’upadacitinib et le groupe témoin; à ce chapitre, ils n’ont pas constaté non plus d’effet proportionnel à la dose après avoir comparé les deux doses étudiées.
« Des cas de TEV ont été rapportés dans les trois groupes de sujets », a souligné le Dr Fleischmann, en faisant état des taux de TEV survenue dans les groupes upadacitinib (0,3 %), adalimumab (0,9 %) et placebo (0,2 %) de l’essai SELECT-COMPARE. Les autres effets indésirables potentiellement graves sont survenus dans des proportions respectivement similaires.
Seule exception pendant l’essai SELECT-MONOTHERAPY : le zona. Il a en effet été plus répandu chez les sujets ayant pris la dose de 30 mg (2,8 %) que chez ceux traités par la dose de 15 mg (1,4 %) et ceux ayant poursuivi le traitement par le méthotrexate (0,5 %). Pendant l’essai SELECT-COMPARE, ces taux se sont chiffrés à 0,5 %, à 0,3 % et à 0,6 % pour l’upadacitinib, l’adalimumab et le placebo, respectivement. Qualifiant le taux plus élevé de zona dans le groupe traité par l’upadacitinib de « prévisible », le Dr Fleischmann a conclu en précisant que l’ensemble des données indique que « l’upadacitinib est au moins aussi bon que l’adalimumab » pour ce qui est du risque d’effets indésirables.
L’essai SELECT-EARLY : la monothérapie chez les patients dont la maladie risque fort d’évoluer
Dans un autre essai de phase III intitulé SELECT-EARLY, l’upadacitinib a été comparé au méthotrexate comme traitement de première intention chez 947 patients atteints d’une forme modérément ou fortement évolutive de PR n’ayant jamais reçu de méthotrexate et affectés aléatoirement à un traitement par l’upadacitinib à 15 mg ou à 30 mg ou par le méthotrexate. Pour être admissibles, les patients devaient présenter au moins une érosion sur les clichés radiographiques ou avoir eu un résultat positif au dépistage du facteur rhumatoïde et des anticorps anti-CCP, a rapporté le Dr Ronald van Vollenhoven, Professeur et Chef du Département d’immunologie et de rhumatologie cliniques des Centres médicaux universitaires d’Amsterdam, et Directeur du Centre de rhumatologie et d’immunologie d’Amsterdam, aux Pays-Bas. Au début de l’essai, le score HAQ-DI moyen se chiffrait à 1,6 et le score de Sharp total modifié (mTSS), à 18 environ.
À la 12e semaine, les taux de réponse ACR50 s’élevaient à 28 %, à 52 % et à 56 % pour le méthotrexate, l’upadacitinib à 15 mg et l’upadacitinib à 30 mg. Pour ce qui est de l’autre objectif principal, soit l’obtention d’un score DAS28-CRP inférieur à 2,6 à la 24e semaine, les taux s’établissaient à 19 %, à 48 % et à 50 %. Toutes les valeurs calculées pour les deux doses d’upadacitinib étaient extrêmement significatives sur le plan statistique comparativement au méthotrexate (p < 0,001).
L’inhibition de l’évolution de la maladie visible à la radiographie
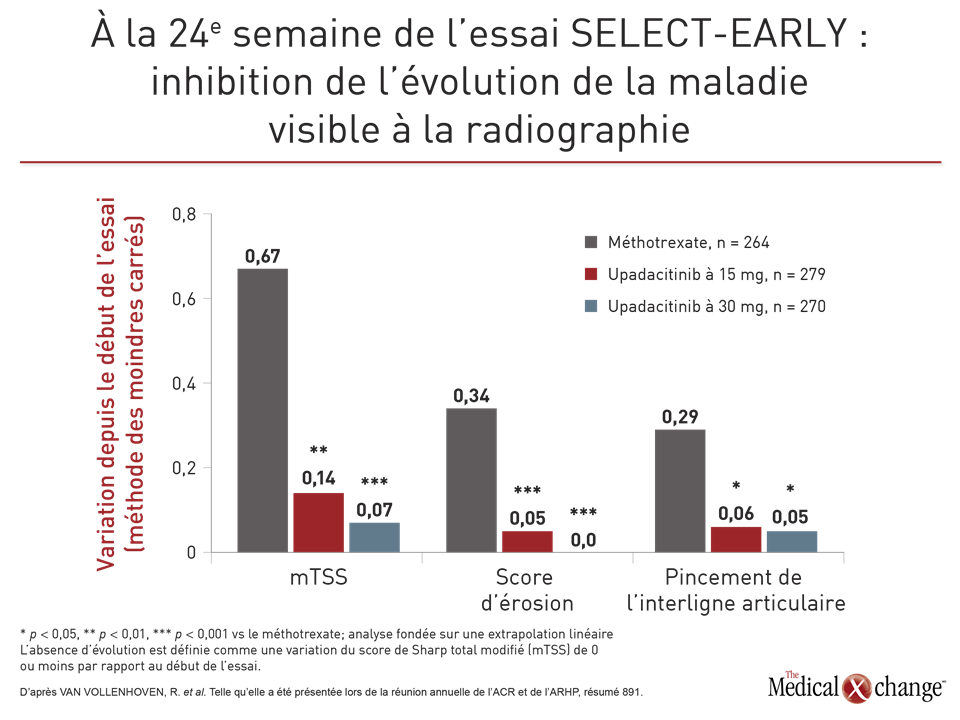
Comme ce fut le cas lors des autres essais, la réponse des sujets traités par l’upadacitinib s’est manifestée rapidement pour ces paramètres, mais aussi pour d’autres, notamment la réponse ACR70, le CDAI de 10 ou moins et le score HAQ-DI comparativement à ceux traités par le méthotrexate. Toutefois, l’inhibition de l’évolution de la maladie visible à la radiographie est probablement l’observation la plus importante de cet essai. Les deux doses d’upadacitinib ont en effet été reliées à une atténuation de l’atteinte structurelle des articulations contrairement au méthotrexate pour lequel une nette évolution a été objectivée à la radiographie (Fig. 3).
« La signification statistique de ces différences était extrêmement marquée, même après 24 semaines de suivi seulement » a affirmé le Dr van Vollenhoven. Indiquant que le positionnement des inhibiteurs de la JAK1 est désormais « un sujet de discussion majeur », il a ajouté : « Nous savons que certains patients ont un taux de protéine C-réactive très élevé et une maladie très évolutive associée à un pronostic plus sombre ». Il a laissé entendre qu’un traitement plus énergique pourrait convenir à ces patients.
« Nous savons que certains patients ont un taux de protéine C-réactive très élevé et sont affligés d’une maladie fortement évolutive pour laquelle le pronostic est plus sombre. [Or ces patients pourraient tirer avantage d’un traitement énergique en première intention]. »
De nouveaux inhibiteurs de la JAK1
Lors de la réunion annuelle, il a également été question des résultats d’études de phase III sur le filgotinib et le péficitinib, de nouveaux inhibiteurs de la JAK1. Les données de dernière minute sur le filgotinib présentées sous forme d’affiches indiquaient que 448 patients aux prises avec une PR fortement évolutive et une réponse insuffisante ou une intolérance aux traitements de fond biologiques ont été répartis aléatoirement de façon à recevoir 100 mg de filgotinib, 200 mg de filgotinib ou un placebo tout en continuant de prendre une dose stable de leur traitement de fond classique. L’objectif principal, soit l’obtention d’une réponse ACR20 à la 12e semaine, a été atteint chez environ deux fois plus de sujets traités par le filgotinib à 100 mg (66,1 %) ou à 200 mg (57,5 %) que chez les témoins (31,1 %; p < 0,001 vs l’une ou l’autre des doses).
Le filgotinib se montre efficace après les traitements de fond biologiques
« Les données nous ont appris que le filgotinib est efficace chez les patients affligés d’une PR évolutive que les agents biologiques ne parviennent pas à maîtriser convenablement », a déclaré le Dr Mark C. Genovese, Directeur de la Clinique de rhumatologie de l’Université Stanford, de Stanford, en Californie. À l’instar de ses confrères ayant présenté les données sur l’upadacitinib, il a mis de l’avant la possibilité que les agents dotés de sélectivité pour la voie JAK1 puissent exercer une activité clinique plus prononcée que les agents plus anciens de cette classe de médicaments. Comme eux, il a aussi insisté sur la nécessité de réaliser des essais comparatifs.
« Les données nous ont appris que le filgotinib est efficace chez les patients affligés d’une PR évolutive que les agents biologiques ne parviennent pas à maîtriser convenablement. »
L’essai de phase III sur l’utilisation du péficitinib chez des patients ayant répondu de façon insatisfaisante aux traitements de fond classiques a été mené au Japon, en Corée et à Taïwan. Comparativement au placebo, les doses de 100 et de 150 mg de péficitinib ont toutes les deux permis d’atteindre l’objectif principal de cet essai, soit un taux de réponse ACR20 plus élevé à la fin de la 12e semaine. Selon le Dr Yoshiya Tanaka, Chef du Département de médecine interne de l’Université de la santé au travail et de la salubrité de l’environnement, de Kitakyushu, au Japon, une demande d’homologation du péficitinib a officiellement été soumise à l’organisme de réglementation nippon.
Conclusion
Selon l’hypothèse avancée, la JAK1 serait, de toutes les enzymes transmettrices de signaux qui composent la famille des JAK, la plus étroitement liée à l’inhibition des voies inflammatoires intervenant dans la PR et d’autres maladies auto-immunes. Une fois le tofacitinib homologué, il a été postulé que les inhibiteurs de JAK conçus de manière à avoir une plus grande sélectivité pour la JAK1 que pour les trois autres voies de signalisation pourraient exercer des effets anti-inflammatoires plus marqués tout en risquant moins de provoquer des effets collatéraux. Bien que les inhibiteurs de JAK n’aient pas été comparés directement dans le cadre d’essais cliniques, les nouvelles données issues d’essais de phase III ayant porté sur des agents novateurs tels que l’upadacitinib et le filgotinib renforcent la thèse voulant que les nouveaux agents permettent d’enrichir et peut-être même d’améliorer l’arsenal thérapeutique opposé à la PR.
Diapositives additionelles
Figure 4 (Fig. 4), Figure 5 (Fig. 5), Figure 6 (Fig. 6) et Figure 7 (Fig. 7).