Oncologie
Congrès de 2022 de la Société européenne de médecine interne cancérologique (ESMO)
Obtenir une vision plus approfondie du traitement par des inhibiteurs de CDK 4 et de CDK 6 pour le cancer du sein avancé
Paris – Dans le traitement de première intention du cancer du sein avancé avec récepteurs hormonaux positifs et récepteurs 2 du facteur de croissance épidermique humain négatifs (RH+/HER2-) chez les femmes ménopausées, des données sur la survie globale (SG) ont été présentées dans le cadre des trois dernières études majeures multicentriques à répartition aléatoire visant à évaluer un inhibiteur de CDK 4 et de CDK 6 dans cette population. Cette dernière étude, appelée MONARCH 3, a été présentée à l’ESMO et a associé un inhibiteur de CDK 4 et de CDK 6 à une tendance favorable dans l’analyse intermédiaire, mais pas à un avantage statistiquement significatif par rapport à l’hormonothérapie seule. Ces résultats diffèrent des données sur la SG antérieures des deux autres études, MONALEESA-2 qui a démontré un avantage significatif et PALOMA-2 qui n’a démontré aucun signe d’avantage, malgré des méthodologies, critères d’admission et avantages pour le résultat de la survie sans progression (SSP) similaires. Pour la SG, les inhibiteurs de CDK 4 et de CDK 6 ne semblent pas être interchangeables.
Dans l’étude MONARCH 3, la comparaison se faisait entre l’ajout d’abémaciclib ou d’un placebo à l’un des deux inhibiteurs de l’aromatase (anastrozole ou létrozole). Dans une étude présentée il y a un an, MONALEESA-2 a comparé l’ajout de ribociclib au létrozole seul. L’ajout du palbociclib au létrozole seul a été évalué dans l’étude PALOMA-2. Comparativement à l’effet bénéfique hautement significatif sur la SG démontré avec le ribociclib dans l’étude MONALEESA-2 et à l’absence d’effet bénéfique sur la SG statistiquement significatif dans l’étude PALOMA-2, l’étude MONARCH 3 a démontré une tendance favorable qui n’a pas encore atteint la signification statistique.
Pour une entrevue exclusive avec le Dr Alexandre Hamelin-Masse couvrant l’impact sur la pratique clinique, cliquez ici.
Les résultats montrent que les inhibiteurs de CDK 4 et de CDK 6 ne sont pas interchangeables
« Ce ne sont pas des composés identiques. Ils ont des profils pharmacodynamiques et des posologies différents, et ils ont produit des résultats différents lors d’études comparables évaluant des traitements d’appoint réalisés antérieurement », a déclaré la Dre Meritxell Bellet Ezquerra, chercheuse principale, Institut d’oncologie de Vall d’Hebron, Barcelone, Espagne. En tant que spécialiste du cancer du sein métastatique, la Dre Bellet Ezquerra a été invitée par l’ESMO à replacer les derniers résultats de MONARCH 3 dans leur contexte clinique.
Ce ne sont pas des composés identiques. Ils ont des profils pharmacodynamiques et des posologies différents, et ils ont produit des résultats différents dans des études comparables.
La Dre Bellet Ezquerra a insisté sur le fait que les résultats de la SG de l’étude MONARCH 3 ont été analysés en tant qu’analyse intermédiaire du suivi en cours et ne sont pas négatifs. En se basant plutôt sur la trajectoire de la SG, elle considère qu’un avantage sur la SG sera « probable » lors d’une analyse finale, qui devrait être réalisée en 2023. Selon la Dre Bellet Ezquerra, les trois inhibiteurs de CDK 4 et de CDK 6 ont démontré des données favorables sur la SSP, mais les données sur la SG devraient guider le choix actuel des inhibiteurs de CDK 4 et de CDK 6.
« La ribociclib a le niveau maximal de données probantes sur la SG en première intention et devrait donc être d’abord envisagée », a-t-elle dit. Cependant, elle n’a pas exclu l’abémaciclib ou même le palbociclib comme choix raisonnable dans le cas d’une raison convaincante d’envisager une solution de rechange, telle que la présence de contre-indications.
[L’inhibiteur de CDK 4 et de CDK 6 avec] le niveau maximal de données probantes sur la SG en première intention doit être d’abord envisagé.
Les études sur les inhibiteurs de CDK 4 et de CDK 6 mettent en question la norme de soins
Dans l’étude MONARCH 3, 493 femmes ménopausées atteintes d’un cancer du sein RH+/HER2- de stade avancé ont été réparties aléatoirement selon un rapport de 2:1 dans les groupes expérimental ou témoin. Dans le groupe expérimental, les patientes ont reçu 150 mg d’abémaciclib deux fois par jour plus 1 mg d’anastrozole ou 2,5 mg de létrozole une fois par jour. Dans le groupe témoin, les patientes ont reçu l’un ou l’autre des inhibiteurs de l’aromatase seul. Au moment où l’étude MONARCH 3 a débuté, comme pour les études MONALEESA-2 et PALOMA-2, l’hormonothérapie était encore la norme de soins.
Le critère d’évaluation principal de la SSP a été publié en 2017. À ce moment, la SSP médiane n’avait pas été atteinte pour le groupe expérimental par rapport à 14,7 mois pour l’hormonothérapie seule, ce qui représente une amélioration hautement significative de 46 % du risque de décès ou de progression (RRI 0,54; p = 0,000021). Des bienfaits similaires de SSP ont été associés aux autres études sur CDK 4 et de CDK 6. En 2016, les données de SSP ont démontré exactement la même amélioration relative de la SSP pour le ribociclib par rapport à l’hormonothérapie seule (non atteinte vs 14,7 mois). Les données de SSP du palbociclib dans l’étude PALOMA-2 ont également été publiées en 2016, associant l’inhibiteur de CDK 4 et de CDK 6 à une SSP médiane de 24,8 mois par rapport à 14,5 mois pour l’hormonothérapie seule.
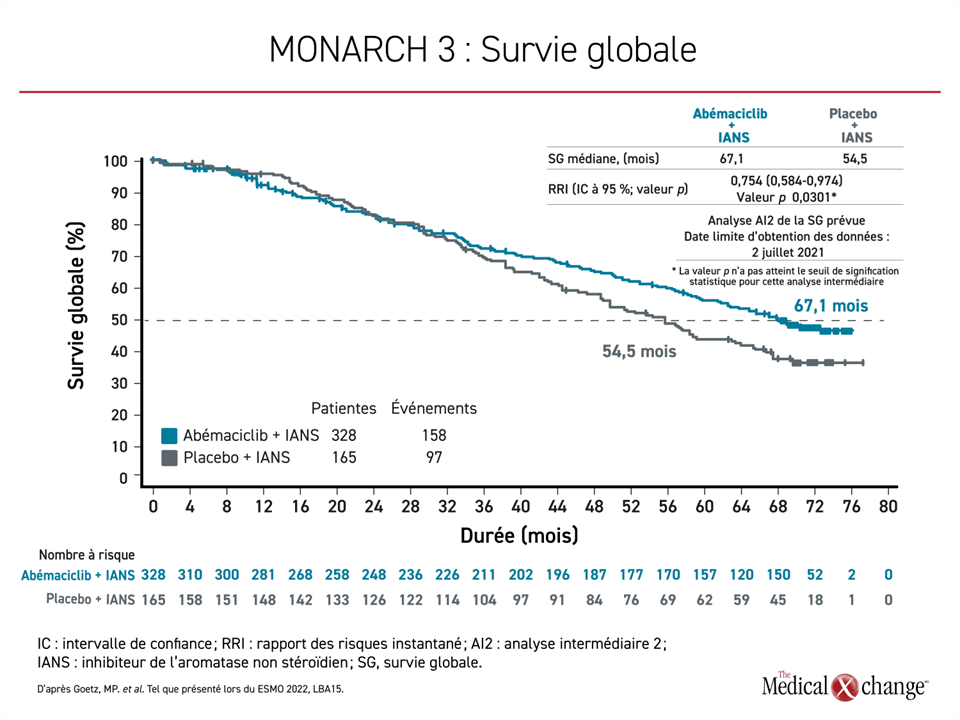
Pour évaluer les avantages en termes de SG dans l’étude MONARCH 3, deux analyses intermédiaires et une analyse finale ont été prévues. La première analyse intermédiaire, après 189 décès, a été menée en 2020 et n’a pas associé l’abémaciclib à un avantage significatif. Dans la deuxième analyse actuelle, réalisée après 252 décès et au bout de 70,2 mois de suivi en moyenne, la SG médiane était de 67,1 mois avec l’inhibiteur de CDK 4 et de CDK 6 contre 54,5 mois dans le groupe témoin. Le rapport de risque correspondait à une réduction d’environ 26 % du risque de décès (RRI 0,0754; p = 0,0301), mais la limite prédéfinie de l’avantage en termes de SG par calcul d’alpha n’a pas été franchie (figure 1).
Par conséquent, « la signification statistique n’a pas été atteinte » a déclaré l’investigateur principal, le Dr Matthew Goetz, Département d’oncologie, Mayo Clinic, Rochester, Minnesota, États-Unis.
Cependant, les données « avancent de manière favorable », a-t-il ajouté. L’augmentation médiane de la SG a été d’un peu plus de 12 mois et des signes supplémentaires d’avantages ont été observés. Plus particulièrement, l’amélioration de la SG dans le sous-groupe de patientes atteintes d’une maladie viscérale à la référence était de plus de 16 mois (48,8 par rapport à 65,1 mois), entraînant une réduction d’environ 30 % du risque de décès dans ce groupe (RRI 0,708; p = 0,0392). Encore une fois, la signification statistique n’a pas été atteinte, mais, comme pour la SG totale, la différence entre les courbes de survie des patientes réparties aléatoirement pour recevoir l’inhibiteur de CDK 4 et de CDK 6 par rapport au groupe témoin semble continuer à s’élargir lors de l’analyse la plus récente.
Bien que la signification statistique « n’ait pas été atteinte » pour un avantage sur le plan de la SG dans l’étude MONARCH 3, les données « prennent une direction favorable ».
Courbes de survie séparées au bout de 3 ans
Les courbes de survie pour les groupes expérimental et témoin ont commencé à se séparer après environ 3 ans pour favoriser l’inhibiteur de CDK 4 et de CDK 6. L’avantage a continué de croître avec le temps, même si 31,5 % des patientes réparties aléatoirement dans le groupe témoin, contre seulement 10,1 % dans le groupe de traitement actif, ont reçu un inhibiteur de CDK 4 et de CDK 6 par la suite. Une analyse complète d’autres sous-groupes, comme ceux différenciés par âge, origine ethnique, statut de l’hormone progestérone, région géographique, exposition antérieure à une hormonothérapie ou à d’autres traitements et nombre d’organes touchés, a également favorisé l’inhibiteur de CDK 4 et de CDK 6 plutôt que l’hormonothérapie seule.
Dans l’étude MONARCH 3, l’abémaciclib a également été associé à une augmentation d’environ 16 mois de la survie sans chimiothérapie (46,7 par rapport à 30,6 mois), ce qui représente une réduction de près de 40 %, bien qu’aucune valeur p n’ait été calculée (RRI 0,636).
L’innocuité et la tolérabilité de l’abémaciclib dans l’étude MONARCH 3 correspondaient à celles signalées lorsque les résultats de la SSP ont été publiés il y a 5 ans. Cela correspond aux données d’innocuité des autres inhibiteurs de CDK 4 et de CDK 6 évalués dans le traitement du cancer du sein postménopausique de stade avancé, qui sont en général élevées, mais non identiques. Dans une méta-analyse en réseau de 8 études, l’abandon du traitement causée par les événements indésirables était plus élevée avec l’abémaciclib qu’avec le ribociclib ou le palbociclib, une différence attribuée à un plus grand nombre d’événements indésirables gastro-intestinaux (Desnoyers A et al. Cancer Treat Rev. 2020;90:102086). Lors de l’analyse la plus récente de l’étude MONARCH 3, seulement trois événements indésirables de gravité de grade ≥ 3 ont été observés plus fréquemment avec l’abémaciclib qu’avec l’inhibiteur de l’aromatase seul. Il s’agissait d’une neutropénie (27,2 % par rapport à 1,2 %), d’une anémie (8,9 % par rapport à 1,2 %) et d’une diarrhée (9,8 % par rapport à 1,2 %).
Les avantages en termes de SG dans l’étude MONARCH 3 semblent probables
D’après les trajectoires de la SG lors de cette deuxième analyse intermédiaire, un avantage relatif en termes de SG pour l’abémaciclib est attendu dans l’analyse finale, selon le Dr Goetz et la Dre Bellet Ezquerra, cette dernière suggérant qu’il est instructif et cliniquement important de tenir compte des différences potentielles entre les inhibiteurs de CDK 4 et de CDK 6 étudiés. Elle a suggéré que les résultats appuient l’hypothèse selon laquelle les médicaments ne sont pas interchangeables pour l’indication spécifique qui était l’objet des études MONARCH 3, MONALEESA-2 et PALOMA-2, même s’il existait des différences modestes dans leur conception et leurs critères d’admission.
PALOMA-2 : l’amélioration des résultats se limite à la SSP
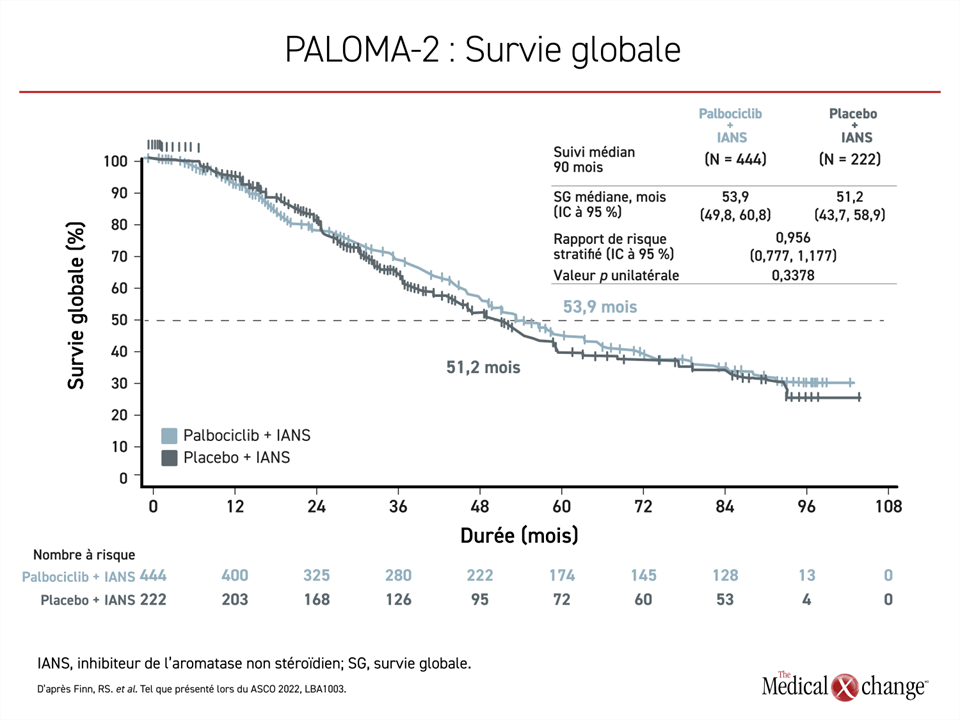
Parmi ces études, PALOMA-2 semble être la plus différente des deux autres. Dans cette étude menée auprès de 666 patientes réparties aléatoirement selon un rapport de 2:1 dans les groupes expérimental et témoin, il n’y avait essentiellement aucun signe d’avantage en termes de SG après un suivi médian de 90 mois lorsque 405 décès étaient survenus. À ce moment, la SG médiane était de 53,9 mois dans le groupe recevant le palbociclib comparativement à 51,2 mois dans le groupe recevant l’hormonothérapie seule. La réduction de 4 % du risque de décès n’a pas atteint la signification statistique (RRI 0,956; p = 0,3378) (figure 2). Une analyse de sensibilité a posteriori excluant les patientes perdues de vue ou qui ont retiré leur consentement n’a pas modifié les conclusions.
Avantages importants et significatifs en termes de SG dans l’étude MONALEESA-2
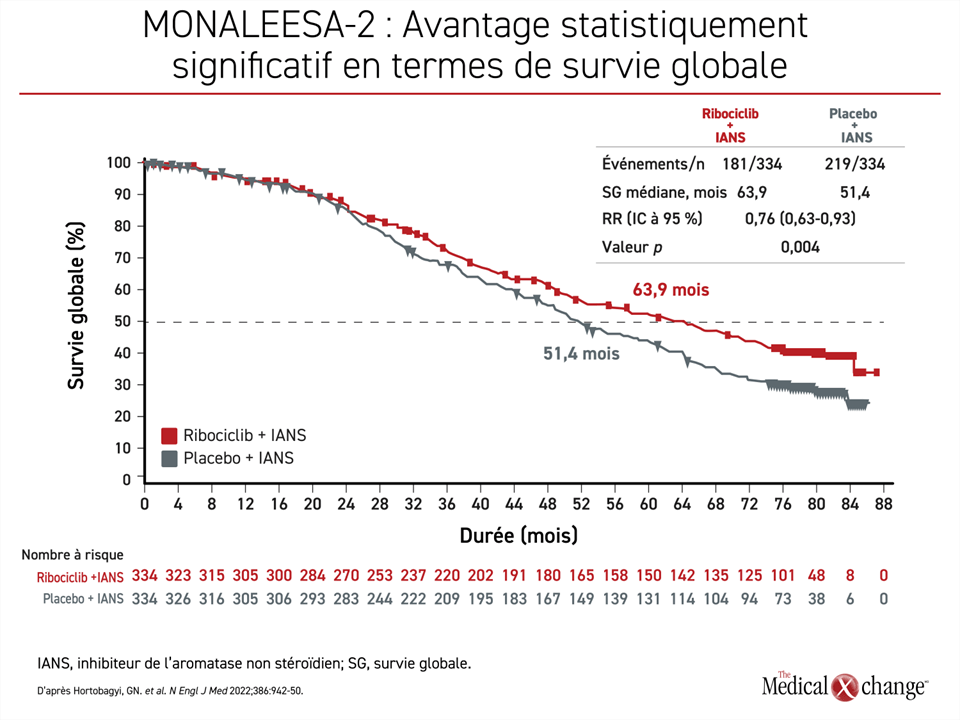
En revanche, l’étude MONALEESA-2, qui a réparti aléatoirement 668 patientes selon un rapport 1:1 dans des groupes recevant le ribociclib en association avec le létrozole ou le létrozole en association avec un placebo, a démontré un avantage important en termes de SG après 80 mois de suivi lorsque 400 décès étaient survenus. L’avantage en termes de SG de plus de 12 mois (63,9 par rapport à 51,4 mois) représente une réduction de 24 % et une réduction hautement significative sur le plan statistique de la mortalité (RRI 0,76; p = 0,008) (figure 3). Comme dans l’étude MONARCH 3, la séparation des courbes de survie a commencé au bout d’environ 2 ans.
De plus, les avantages en termes de SG dans l’étude MONALEESA-2 concordent avec ceux de deux autres études, MONALEESA-3, qui comptait également des patientes ménopausées, et MONALEESA-7, qui comptait des patientes préménopausées, démontré par la réduction d’environ 30 % du risque de décès, peu importe leur statut ménopausique, avec l’ajout de ribociclib par rapport au traitement endocrinien seul.
Un examen plus approfondi de trois études sur les inhibiteurs de CDK 4 et de CDK 6
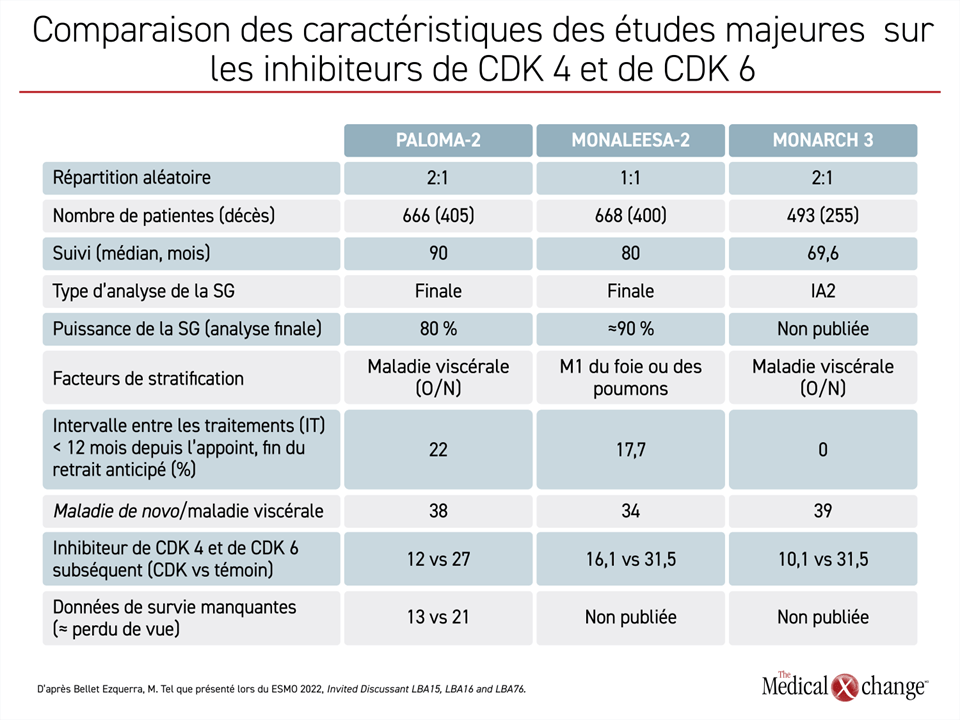
Dans une comparaison juxtaposée des caractéristiques potentiellement pertinentes des trois études portant sur les inhibiteurs de CDK 4 et de CDK 6, la Dre Bellet Ezquerra n’a trouvé aucune différence majeure qui pourrait pleinement tenir compte des différences dans les résultats (tableau 1).
Par exemple, la proportion de patientes recevant un inhibiteur de CDK 4 et de CDK 6 par la suite dans le groupe témoin (environ 30 % dans les trois études) et la proportion de patientes atteintes de maladie de novo (environ 35 à 40 % dans les trois études) étaient similaires. Une proportion plus élevée de patientes dans l’étude PALOMA-2 (22 %) ont participé à l’étude moins de 12 mois après l’interruption du traitement endocrinien par rapport à l’étude MONARCH 3 (0 %) et à l’étude MONALEESA-2 (17,7 %), mais la Dre Bellet Ezquerra n’a pas considéré que cela avait eu un impact majeur sur les résultats.
Malgré ces résultats, selon la Dre Bellet Ezquerra, tous les inhibiteurs de CDK 4 et de CDK 6 continueront probablement de jouer un rôle dans la maîtrise des maladies et du cancer du sein. Même dans le cas du cancer du sein métastatique RH+/HER2- postménopausique, elle pense que le palbociclib devrait rester « dans l’équation », un avis fondé sur certaines données probantes en situation réelle d’avantages potentiels en termes de SG. Cependant, elle a dit que les données disponibles définissent l’ordre actuel des traitements à prendre en considération pour cette indication en attendant des comparaisons directes.
En raison du fait qu’un seul de ces médicaments présente maintenant un niveau 1A de données probantes pour une norme de soins, fondé sur les données de SG, le ribociclib est « majoritairement la première option » à l’heure actuelle.
Conclusion
Plus de 7 ans après le début de trois études multinationales définitives évaluant les bienfaits de l’ajout d’un inhibiteur de CDK 4 et de CDK 6 à l’hormonothérapie, les résultats de la SG sont maintenant disponibles. Les avantages variaient; bien qu’un avantage important et statistiquement significatif en termes de SG ait été associé au ribociclib dans l’étude MONALEESA-2, aucun avantage en termes de SG n’a été observé avec le palbociclib dans l’étude PALOMA-2. La dernière étude visant à publier des données de SG, MONARCH 3, a montré une tendance très favorable pour la SG qui n’a pas encore atteint la signification statistique.