Hématologie
Congrès hybride de 2023 de l’European Hematology Association (EHA)
Efficacité à long terme dans la LLC : données probantes collectées chez des patients jamais traités ou atteints d’une LLC R/R
Francfort/en ligne – Des présentations données lors du congrès de 2023 de l’European Hematology Association (EHA) ont fait état de la multiplication des données probantes établissant des différences entre les inhibiteurs de la tyrosine kinase de Bruton (iBTK) de première et de deuxième génération dans le traitement de la leucémie lymphoïde chronique (LLC). Y ont été présentées, entre autres, les données à long terme de l’étude SEQUOIA et les résultats de l’étude ALPINE sur la qualité de vie liée à la santé (QVLS), qui ont confirmé les effets positifs des iBTK de deuxième génération. Ils ont également mis en relief l’importance de la sélectivité à l’égard de la BTK et de la liaison à cette dernière comme traits distinctifs des iBTK de deuxième génération et leur répercussion possible sur l’innocuité et l’efficacité du traitement.
Santé Canada a récemment ajouté le traitement de première ligne de la LLC et celui des formes réfractaires ou récidivantes (R/R) de cette maladie aux indications du zanubrutinib, un iBTK de deuxième génération, à la lumière de deux études multicentriques de phase III, les études SEQUOIA et ALPINE, qui ont établi la plus grande efficacité de cet agent et sa meilleure tolérabilité par rapport au traitement de référence auquel il était comparé.
Pour une entrevue exclusive avec le Dr Talha Munir couvrant l’impact sur la pratique clinique, cliquez ici.
Efficacité d’un inhibiteur de la BTK de deuxième génération employé en première ligne
Lorsque les résultats de l’étude SEQUOIA ont été rapportés il y a un an, le zanubrutinib avait abaissé d’au moins 50 % (RRI : 0,42; p < 0,0001) le taux de progression de la maladie ou de décès comparativement à une association de bendamustine et de rituximab (BR) chez des patients atteints de LLC ou d’un lymphome à petits lymphocytes (LPL) (Tam, C. S. et al. Lancet Oncology 2022;8:1031-1043). Or les résultats de 18 mois de suivi supplémentaires présentés au congrès de l’EHA confirment que les gains enregistrés persistent au fil du temps et que les taux relatifs d’effets indésirables sont faibles.
« Les résultats de ce suivi prolongé corroborent la grande utilité du zanubrutinib en tant que traitement de première ligne », a rapporté le Dr Talha Munir, du Service de diagnostic hémato-oncologique, à l’Institut d’oncologie St‑James, de Leeds, au R.-U.
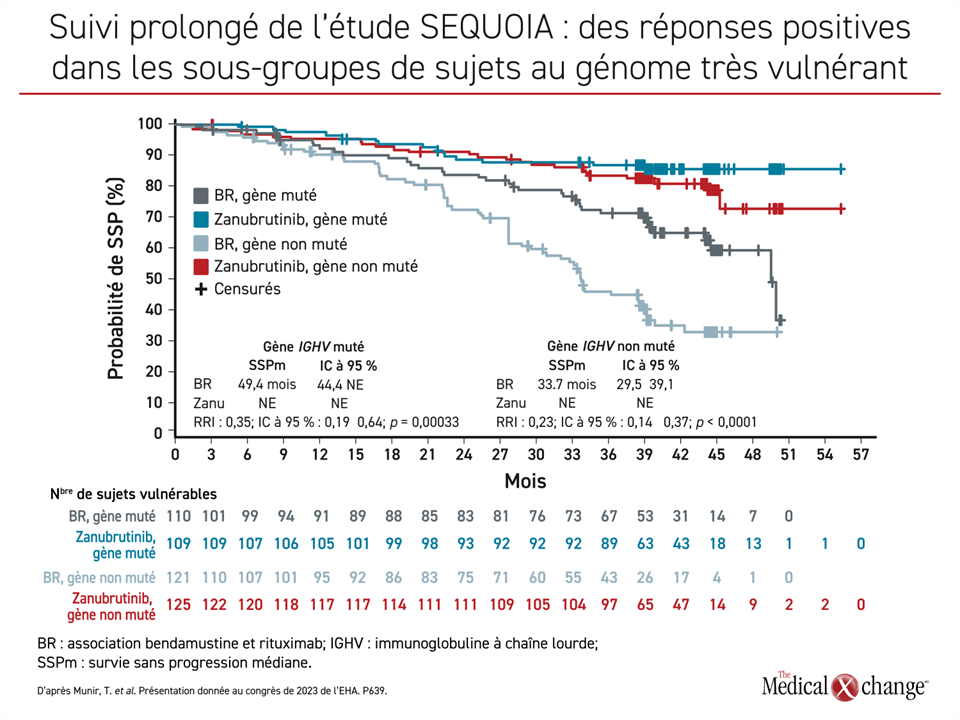
Lors de l’étude SEQUOIA, 479 patients jamais traités auparavant et exempts d’une délétion 17p ont été affectés aléatoirement au zanubrutinib ou à l’association BR (cohorte 1), tandis que 111 autres patients porteurs de cette délétion ont été suivis pendant qu’ils prenaient du zanubrutinib en monothérapie (cohorte 2). La durée médiane du suivi frôle les 4 ans dans les deux cohortes (cohorte 1 : 43,7 mois; cohorte 2 : 47,9 mois). Pendant la phase à double insu, la survie sans progression (SSP) médiane se chiffrait à 42,2 mois dans le groupe traité par l’association BR, mais n’avait toujours pas été atteinte dans le groupe zanubrutinib, d’où une réduction relative de 70 % à l’avantage de l’iBTK de deuxième génération (RRI : 0,30; p < 0,0001).
De plus, le gain observé avec le zanubrutinib était similaire que les patients soient porteurs ou non d’une mutation du gène IGHV. La SSP médiane n’est toujours pas atteinte dans les deux groupes zanubrutinib, alors que celle obtenue avec l’association BR se chiffre à 49,4 mois dans le groupe IGHV muté et à 33,7 mois dans le groupe non muté. Résultat : une réduction relative du risque de décès ou d’évolution de la maladie de 65 % avec le zanubrutinib par rapport à l’association BR chez les patients porteurs d’un gène IGHV muté (RRI : 0,35; p = 0,00033) et de 77 % chez les patients porteurs d’un gène IGHV non muté (RRI : 0,23; p < 0,0001) (Figure 1).
« Les résultats de ce suivi prolongé corroborent la grande utilité du zanubrutinib en tant que traitement de première ligne. »
Dans la cohorte 2, celle formée de porteurs d’une délétion 17p, 70,3 % des patients traités par le zanubrutinib suivent toujours leur traitement à ce jour. La SSP médiane n’est toujours pas atteinte dans cette cohorte traitée par le zanubrutinib, mais elle a été estimée à 79,4 % à 42 mois, soit un peu moins que les 82,4 % de celle estimée chez les patients exempts de cette délétion.
Une innocuité soutenue
Comme ils s’y attendaient, les chercheurs ont relevé peu de différences entre le zanubrutinib et l’association BR au chapitre des taux d’effets indésirables survenus pendant le traitement (EIT) et de la nature de ces derniers. Les effets indésirables d’intérêt du zanubrutinib correspondaient à ceux qui étaient à prévoir avec un iBTK de deuxième génération. Quant aux effets indésirables de grade 3 ou supérieur, les cas de diarrhée (1,7 % vs 2,2 %), de neutropénie (12,5 % vs 51,1 %), d’anémie (0,4 % vs 2,2 %) et de thrombocytopénie (2,1 % vs 7,9 %) ont été moins nombreux avec le zanubrutinib, contrairement aux cas d’infection (23,8 % vs 22,0 %), de saignements (5,8 % vs 1,8 %) et d’hypertension (9,2 % vs 6,6 %) qui ont été plus répandus. Chez les porteurs d’une délétion 17p, aucun de ces effets indésirables n’était sensiblement plus fréquent avec le zanubrutinib.
Il faut souligner que pendant l’étude SEQUOIA, dont l’effectif était surtout composé de patients âgés, les cas de fibrillation auriculaire (FA), de flutter auriculaire, d’hémorragie grave et d’hypertension ont été peu fréquents chez les patients affectés aléatoirement à l’association BR ou au zanubrutinib. Ceci est important car ces effets indésirables sont souvent préoccupants chez les patients traités par l’ibrutinib. Les taux de FA/flutter auriculaire de grade 3 ou plus dans les groupes zanubrutinib étaient de 1,3 % chez les patients sans mutation del(17p) et de 4,5 % chez les patients avec une mutation del(17p), et les taux d’hypertension de grade 3 ou plus étaient de 6,6 % et 9,2 % respectivement. Dans l’ensemble, la tolérabilité du zanubrutinib a été bonne pendant toute la durée de la phase de traitement prolongée.
Les agents de deuxième génération supplantent l’inhibiteur de la BTK de première génération
Les iBTK de deuxième génération, qui comprennent l’acalabrutinib et le zanubrutinib, se sont montrés plus sûrs que l’ibrutinib, l’agent de première génération, au cours des études, y compris celles de phase III menées avec comparaison directe. Fait important à noter, la supériorité de l’efficacité du zanubrutinib sur l’ibrutinib a aussi été confirmée. La sélectivité relative à l’égard de la kinase cible, des caractéristiques pharmacocinétiques plus favorables et une liaison plus prononcée à la BTK sont toutes des facteurs qui distinguent les agents de deuxième génération de celui de première génération et même les agents de deuxième génération les uns des autres.
L’étude ELEVATE R/R menée chez des patients atteints d’un LLC R/R (Byrd, J. et al. J Clin Oncol 2021;39:3441-3452) a révélé que la sélectivité à l’égard de la BTK cible joue un rôle important. Elle a en effet permis de constater que le risque d’incidents cardiovasculaire (CV) était plus faible avec l’acalabrutinib qu’avec l’ibrutinib. La SSP médiane était identique dans les deux groupes, soit 38,4 mois (p = 0,002), et le rapport des risques instantanés s’élevait à 1,00 (figure 2).
Les résultats de l’étude ALPINE ont été publiés plus tôt cette année (Brown et al. N Engl J Med 2023;388:319-332). Tout comme l’acalabrutinib pendant l’étude ELEVATE R/R, le zanubrutinib a été relié à une baisse du risque d’incidents CV et d’autres effets indésirables qui, en théorie, sont provoqués par l’inhibition d’enzymes hors cible. Le zanubrutinib a aussi permis d’obtenir une SSP supérieure à celle observée avec l’ibrutinib. À 24 mois, le taux de SSP se chiffrait à 79,5 % dans le groupe zanubrutinib et à 67,3 % dans le groupe ibrutinib. À 35 %, la baisse relative du risque d’évolution de la maladie ou de décès était à l’avantage du zanubrutinib (RRI : 0,65; p = 0,002).
« Le zanubrutinib est un iBTK de deuxième génération très actif et sélectif. Sa conception visait à offrir une meilleure tolérabilité en maximisant sa liaison à la BTK et en réduisant au minimum ses effets collatéraux », a déclaré la Dre Jennifer R. Brown, du département d’oncologie médicale, à l’Institut de cancérologie Dana-Farber, de Boston, et principale clinicienne-chercheuse de l’étude ALPINE. Elle a aussi dirigé une analyse de l’innocuité du zanubrutinib dans plusieurs hémopathies malignes à lymphocytes B, qui a été présentée devant l’EHA.
« Le zanubrutinib est un iBTK de deuxième génération très actif et sélectif. Sa conception visait à offrir une meilleure tolérabilité en maximisant la liaison à la BTK et en réduisant au minimum les effets collatéraux. »
Innocuité et sélectivité des inhibiteurs de la BTK dans les hémopathies malignes à lymphocytes B
Dix études, dont l’étude ALPINE, ont permis de collecter des données sur l’innocuité auprès de 1550 patients traités par le zanubrutinib et 422 autres traités par l’ibrutinib. Ils étaient majoritairement (60,5 %) atteints de LLC ou de LPL, les autres étant aux prises avec une macroglobulinémie de Waldenström, un lymphome de la zone marginale, un lymphome folliculaire ou un lymphome diffus à grandes cellules B. Le tiers environ des patients traités par le zanubrutinib n’avaient jamais subi de traitement auparavant et près de 20 % en avaient déjà subi au moins 3.
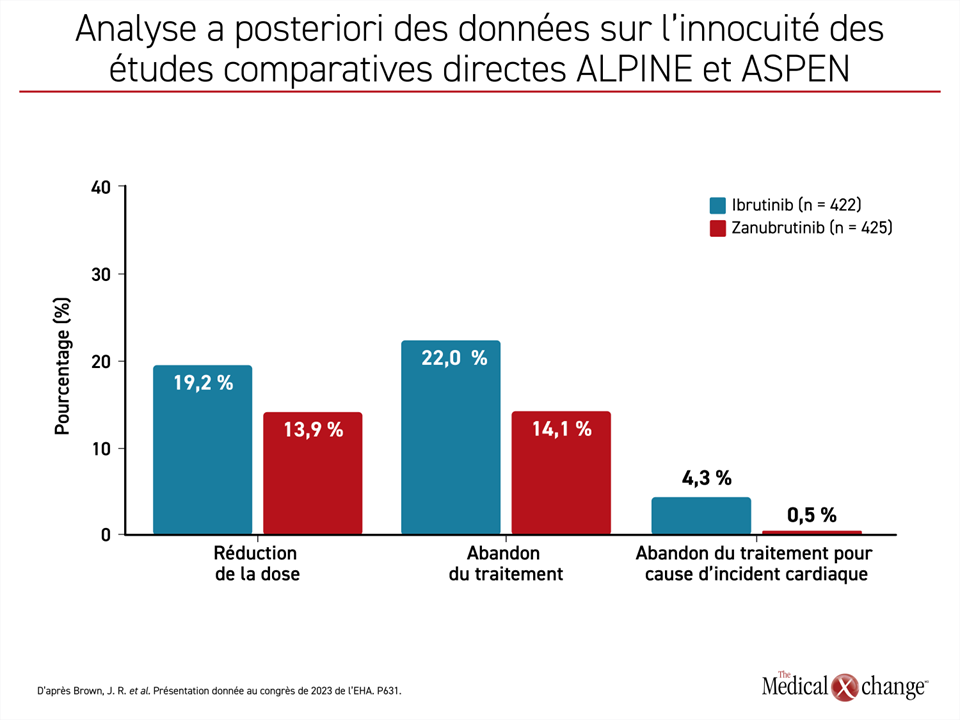
Que les sujets aient été traités par le zanubrutinib ou par l’ibrutinib, les taux d’effets indésirables autres que cardiovasculaires étaient similaires lorsqu’ils étaient exprimés sous forme de taux d’incidence pondérée en fonction de l’exposition, mais l’hypertension et la fibrillation auriculaire ont été plus répandues avec l’ibrutinib. Dans l’ensemble, les effets indésirables les plus souvent signalés avec le zanubrutinib ont été les infections des voies respiratoires supérieures, la diarrhée et les contusions, mais elles étaient généralement peu ou modérément intenses. Si on se restreint aux deux études ayant servi à comparer directement le zanubrutinib à l’ibrutinib (études ALPINE et ASPEN), on constate que les réductions posologiques, les abandons du traitement et les abandons imputables à un EIT cardiaque ont tous été plus répandus avec l’ibrutinib (Figure 2). En outre, le zanubrutinib y a été incriminé dans un moins grand nombre d’EIT cardiaques mortels que l’ibrutinib (0,2 % vs 1,7 %).
« Comme les iBTK doivent être administrés en continu pour traiter la plupart des hémopathies malignes à lymphocytes B, leur tolérabilité et la faiblesse de leur taux d’abandons du traitement sont des facteurs importants », a souligné la Dre Brown, en ajoutant que la sélectivité ne fournit pas seulement une explication possible des différences observées entre les agents de première et de deuxième générations, mais qu’elle a aussi son importance pour les médicaments de deuxième génération eux-mêmes dans la mesure où elle raréfie les effets collatéraux.
La qualité de vie (QdV) et le traitement prolongé de la LLC
Selon d’autres données de l’étude ALPINE sur la maîtrise de la maladie obtenue avec les iBTK de deuxième génération, des différences dans la QVLS auraient été relevées entre le zanubrutinib et l’ibrutinib. Les données sur ce paramètre d’évaluation secondaire ont été recueillies à l’aide des 30 questions du questionnaire sur la qualité de vie de l’European Organization for Research and Treatment of Cancer (questionnaire EORTC QLQ‑C30), auxquelles les sujets ont répondu à la fin des 7e et 13e cycles de traitement.
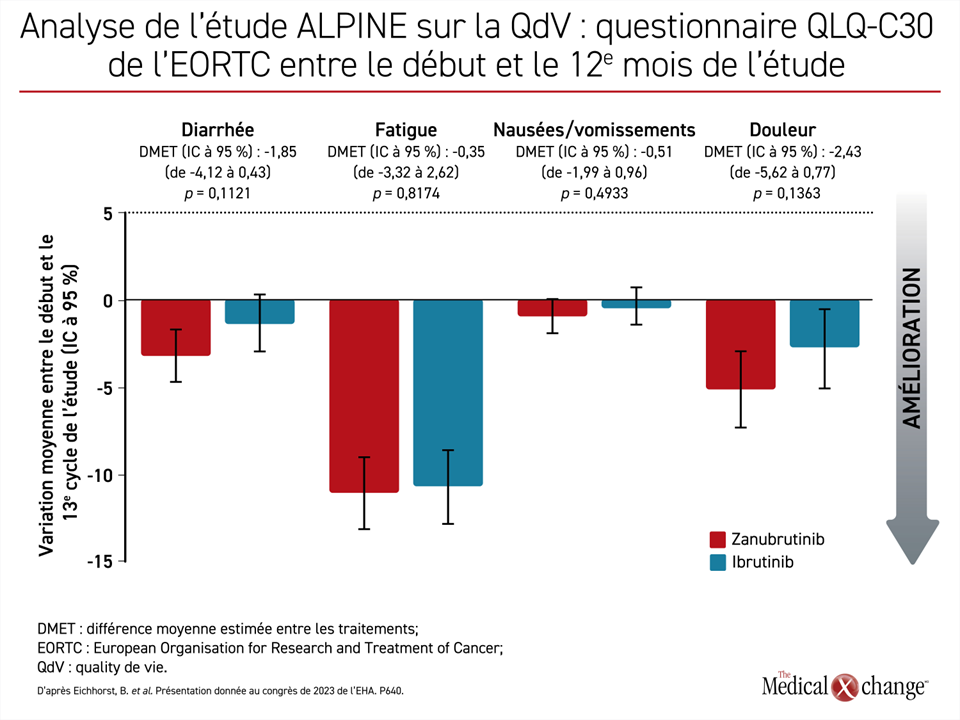
« La fatigue et la douleur se sont atténuées chez les sujets des deux groupes, mais elles ont diminué de façon cliniquement significative pendant les deux cycles chez ceux traités par le zanubrutinib », a rapporté la Dre Barbara Eichhorst, professeure agrégée à la Division d’hématologie de l’Université de Cologne, en Allemagne.
Lorsqu’ils ont été comparés sous l’angle de l’état de santé général, du fonctionnement physique et du fonctionnement occupationnel, le zanubrutinib s’est révélé supérieur à l’ibrutinib dans tous les domaines, au moins numériquement parlant. Les améliorations se sont maintenues du 6e au 12e mois, qui se trouve être la date butoir de collecte des données fixée pour ces analyses (Figure 3).
« [Ces symptômes] ont diminué de façon cliniquement significative pendant les deux cycles chez les patients traités par le zanubrutinib »
D’autres études visant à apparier la QdV à l’efficacité, à l’innocuité et aux résultats rapportés par les patients sont prévues, mais la Dre Eichhorst a mentionné que l’amélioration de la QdV, qui dépend à la fois de la maîtrise du traitement et de l’absence relative d’effets indésirables liés au traitement, est parfois un aspect négligé de la prise en charge de la LLC et des autres hémopathies malignes à lymphocytes B. Aux premiers stades de la maladie, quand la QdV est généralement intacte et que les symptômes sont peu nombreux, un traitement bien toléré permet de préserver le bien-être du patient. Or les iBTK sont souvent administrés indéfiniment afin de maîtriser les hémopathies malignes à lymphocytes B, d’où l’intérêt de réduire au minimum les effets indésirables, y compris les effets indésirables collatéraux qui compromettent la QdV.
Différenciation des iBTK
Les tentatives visant à différencier les agents de deuxième génération d’après leur efficacité et leur innocuité ont jusqu’à maintenant été indirectes. Selon le Dr Mazyar Shadman, médecin traitant au Centre de cancérologie Fred Hutchinson, de Seattle, Washington, les études expérimentales ont fait ressortir des différences entre ces agents. Par exemple, le profilage des kinases montre que « le zanubrutinib est plus sélectif que l’ibrutinib, l’acalabrutinib et le principal métabolite de ce dernier ».
De plus, les différences pharmacologiques, notamment la plus longue demi-vie du zanubrutinib, peuvent avoir une incidence sur la liaison à la BTK. Les données présentées devant l’EHA par le Dr Shadman montraient que l’effet indésirable ayant motivé le remplacement de l’ibrutinib ou de l’acalabrutinib par le zanubrutinib pour cause d’intolérance n’était pas revenu chez une forte proportion des patients concernés
« Le zanubrutinib a permis de maîtriser la maladie chez plus de 95 % des patients évaluables qui avaient bien répondu à l’ibrutinib ou à l’acalabrutinib, mais qui ne les supportaient pas », a-t-il ajouté.
D’après cette analyse à long terme, 67,7 % et 73,0 % des manifestations d’intolérance envers l’ibrutinib et l’acalabrutinib ne se sont pas reproduites. Ces résultats à plus long terme concernant l’efficacité et l’innocuité portent à croire qu’il peut être avantageux sur le plan clinique de remplacer les autres iBTK par le zanubrutinib chez les patients qui y sont intolérants.
Conclusion
Grâce à des études à répartition aléatoire de grande envergure, le zanubrutinib est désormais indiqué pour le traitement de la LLC jamais traitée auparavant et de la LLC R/R. Il est venu rejoindre l’acalabrutinib comme traitement privilégié pour ces indications, alors que l’ibrutinib est maintenant vu comme une option de second choix. La phase de suivi prolongée de l’étude SEQUOIA a de nouveau confirmé l’avantage offert par le zanubrutinib et son efficacité soutenue comme option thérapeutique de première ligne. Le bilan d’innocuité des iBTK de deuxième génération, y compris le zanubrutinib, est plus favorable que celui de l’ibrutinib, l’iBTK de première génération. La sélectivité de ces agents à l’égard de la BTK et leur liaison à cette enzyme expliquent en partie les différences d’efficacité et d’innocuité objectivées. Les caractéristiques qui distinguent les iBTK de deuxième génération de l’iBTK de première génération ont peut-être aussi un rapport avec les différences d’efficacité et d’innocuité observées entre les agents de deuxième génération pendant les études indépendantes.