Revue d’experts
Les IPP et le RGO : les besoins restant à satisfaire
Chapitre 1 : Les enjeux actuels dans la maîtrise du RGO
David Armstrong, M. A., M.B. B.Chir., FRCP(R.-U.), FACG, AGAF, FRCPC
Professeur agrégé, Division de gastroentérologie
L’Université McMaster, Hamilton (Ontario)
Les raisons pour lesquelles certains patients atteints de reflux gastro-œsophagien (RGO) ne réussissent pas à soulager leurs symptômes de manière satisfaisante au moyen des inhibiteurs de la pompe à protons (IPP) se sont révélées étonnamment complexes. Même si les doses classiques d’IPP à administration uniquotidienne permettent de guérir l’œsophagite érosive chez un grand nombre de patients, beaucoup d’entre eux continuent d’éprouver des symptômes une fois cette affection guérie. Comparativement aux patients atteints d’œsophagite, le pourcentage de ceux qui présentent un RGO donnant des résultats négatifs à l’endoscopie (RGO non érosif) et qui obtiennent un soulagement insuffisant de leurs symptômes est encore plus élevé. Les multiples travaux de recherche réalisés sur le lien entre le reflux, acide ou non, et les symptômes de RGO ont permis de mieux comprendre les mécanismes physiopathologiques qui entrent en jeu. Les nouvelles perspectives issues de ces travaux orientent maintenant les stratégies susceptibles de combler les lacunes des traitements actuels. En substance, il a été démontré que le RGO est une entité hétérogène caractérisée par d’autres facteurs étiologiques favorisants hormis la sécrétion excessive d’acide gastrique. Or une démarche systématique visant à mieux cerner les principaux mécanismes à l’origine des symptômes permettrait vraisemblablement d’améliorer l’issue des traitements.
Définition et caractéristiques épidémiologiques
On entend par reflux gastro-œsophagien (RGO) la remontée du contenu de l’estomac dans l’œsophage. Si la plupart des gens ont des accès de RGO à l’occasion, ces derniers ne sont considérés pathologiques que lorsque leurs symptômes deviennent incommodants1. Si l’on se fie à cette description axée sur le patient, le RGO est donc une affection qui se définit par ses symptômes, même si elle peut aboutir à des complications telles que l’œsophagite érosive et l’œsophage de Barrett, de même qu’à des troubles extra-œsophagiens (par ex., la laryngite et la toux chronique). Le RGO est par définition l’écoulement du contenu gastrique dans le sens opposé au sens physiologique, ce qui n’exclut pas l’existence possible d’autres affections touchant les voies digestives hautes de manière concomitante. Par ailleurs, le RGO peut être associé à d’autres symptômes hormis ceux auxquels il est habituellement relié. Dans le cadre d’une étude canadienne sur la dyspepsie dont ont été écartés les patients se plaignant uniquement de brûlures d’estomac ou de régurgitation, l’endoscopie a révélé que 54,7 % des sujets étaient atteints d’une œsophagite2. Même si bon nombre de ces patients s’étaient plaints, au milieu de leur pléthore de symptômes, de brûlures d’estomac ou de régurgitation, cette étude est venue confirmer la présence fréquente d’un RGO chez les patients souffrant de dyspepsie n’ayant fait l’objet d’aucun examen et dont les brûlures d’estomac ne sont qu’un des symptômes parmi tant d’autres. Aux États-Unis et au Royaume-Uni, l’incidence du RGO se situe environ à 5 nouveaux cas pour chaque tranche de 1000 années-patients. En extrapolant ces chiffres au contexte canadien, il est possible de présumer que 170 000 nouveaux cas de RGO seront diagnostiqués annuellement3. Une revue récente des études de population n’a pas permis de corroborer la théorie selon laquelle l’incidence du RGO augmente avec l’âge, mais ses résultats portent à croire que les patients âgés sont plus sujets à l’œsophagite érosive4. Cette analyse a également abouti à la conclusion que les symptômes du RGO perdent en intensité et en définition avec l’âge. Sachant à quel point l’expression des symptômes du RGO est hétérogène, les cliniciens qui pratiquent dans des pays où, comme au Canada, les gens de plus de 60 ans forment une proportion toujours plus grande de la population, pourraient juger ces observations fort intéressantes. Même si le rôle du reflux non acide ou légèrement acide du contenu gastrique dans l’apparition des symptômes de RGO a fait l’objet d’une certaine attention récemment5, la maîtrise du reflux acide reste le principe fondamental sur lequel reposent les traitements. La réaction du RGO à la maîtrise du reflux acide est tellement caractéristique de cette affection que l’Association canadienne de gastro-entérologie (ACG) considère l’essai d’un traitement antisécrétoire reposant sur l’administration d’un inhibiteur de la pompe à protons (IPP) notamment, comme une épreuve diagnostique de certitude6. Cela dit, l’absence de réaction favorable à un IPP, surtout s’il est administré une fois par jour, n’élimine pas d’emblée un diagnostic de RGO. Une réaction insatisfaisante au traitement doit certes inciter les cliniciens à chercher d’autres causes pour expliquer les symptômes. Il conviendra d’envisager un diagnostic de RGO réfractaire dans les cas où l’administration biquotidienne d’un IPP ne permet pas d’atténuer suffisamment les symptômes et où aucune autre cause n’a pu être découverte3.
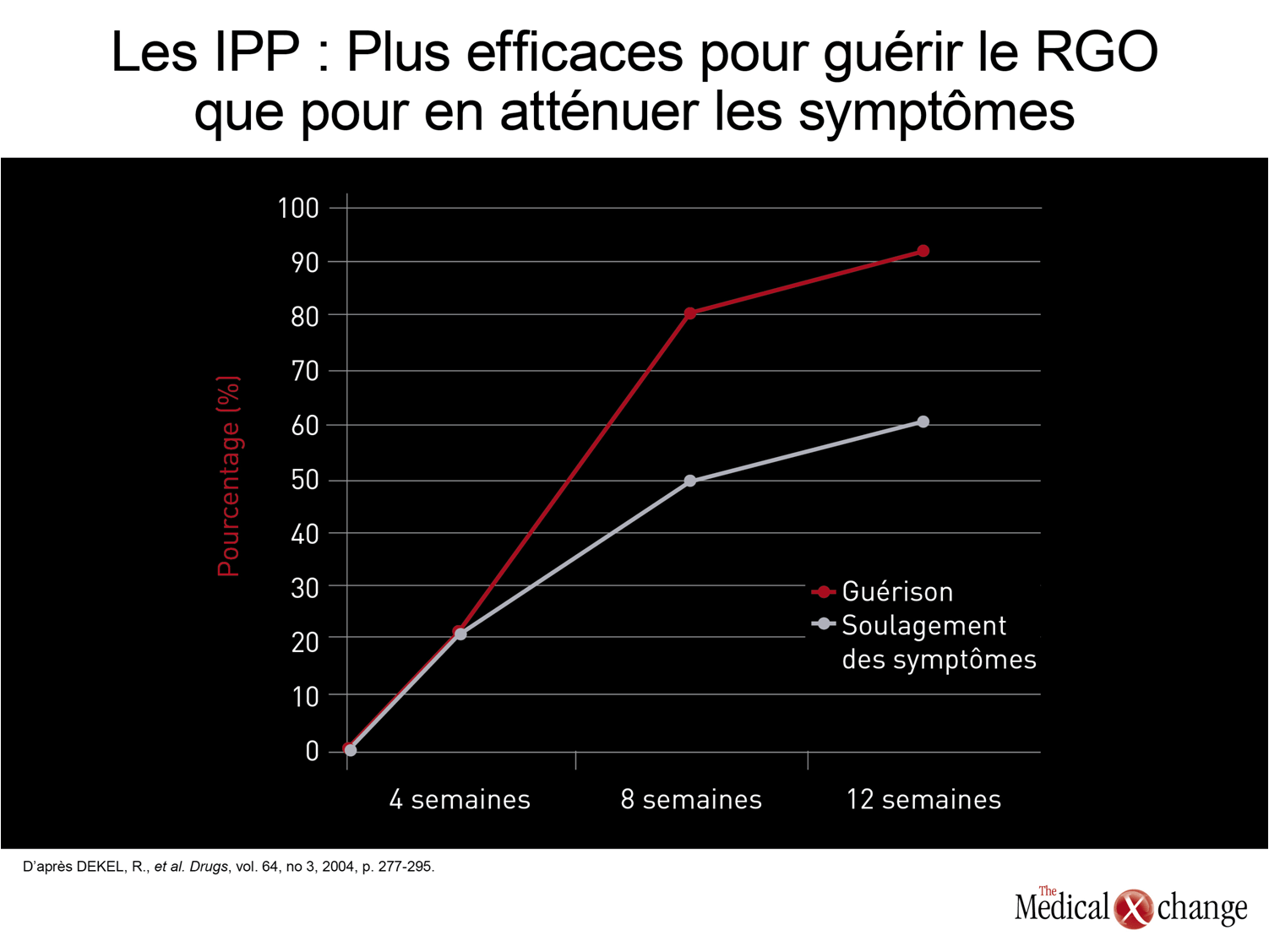
Les traitements classiques reposant sur l’administration uniquotidienne d’un IPP se soldent par un échec chez une proportion considérable de patients quand l’objectif visé est la maîtrise des symptômes
Les traitements classiques reposant sur l’administration uniquotidienne d’un IPP se soldent par un échec chez une proportion considérable de patients quand l’objectif visé est la maîtrise dessymptômes. Comparativement aux taux de guérison, qui ont toujours dépassé les 90 % lors des essais portant sur l’issue de traitements de 8 à 12 semaines, les taux enregistrés pour la maîtrise des symptômes oscillent plutôt entre 50 et 65 %7 (Fig. 1). Chez les patients atteints d’une forme non érosive de RGO, les taux rapportés pour la maîtrise des symptômes sont généralement encore plus faibles que ceux obtenus chez les patients aux prises avec une œsophagite8. Notons toutefois que la majorité des essais réalisés chez des patients présentant un RGO non érosif ont duré 4 semaines seulement et que certaines données, du moins celles qui ont été recueillies chez des patients souffrant de brûlures d’estomac n’ayant fait l’objet d’aucun examen, révèlent que la proportion de patients qui voient leurs symptômes s’atténuer augmente avec la poursuite du traitement, celui-ci pouvant aller jusqu’à 12 semaines9.Bien que les taux de maîtrise des symptômes soient beaucoup plus élevés avec les IPP qu’avec n’importe quel autre agent utilisé dans le traitement du RGO, il faudra trouver des traitements encore meilleurs en raison du lien profond entre les symptômes et la diminution de la qualité de vie10.
Le RGO contre le RGO non érosif
La meilleure description que l’on puisse donner au RGO non érosif est peut-être un RGO qui en est à ses débuts ou une forme légère de RGO. D’autres ont plutôt avancé que le RGO non érosif est une entité distincte, qui risque peu d’évoluer vers l’œsophagite et autres complications
Dans ses lignes directrices, l’ACG donne son aval au traitement empirique dans les cas de brûlures d’estomac et de régurgitation, qui ne montrent aucun symptôme alarmant tel qu’une perte pondérale inexpliquée ou des signes de saignements, sur la seule présomption d’un RGO sous-jacent6. Chez les patients qui réagissent favorablement au traitement, il se peut que l’examen ne soit jamais poussé plus loin, empêchant ainsi la reconnaissance des sous-types du RGO que sont l’œsophagite érosive et le RGO non érosif. La meilleure description que l’on puisse donner au RGO non érosif est peut-être un RGO qui en est à ses débuts ou une forme légère de RGO. Certains ont plutôt avancé que le RGO non érosif est une entité distincte, qui risque peu d’évoluer vers l’œsophagite et autrescomplications11. Cela dit, notre compréhension du RGO non érosif est freinée par le fait qu’il n’existe aucun examen objectif qui permettrait de confirmer la présence d’un reflux– acide ou non – chez les patients aux prises avec ce problème puisque, par définition, il ne provoque aucune lésion visible à l’endoscopie. En l’absence de reflux, il est à prévoir que les traitements antireflux se révéleront inefficaces. De la même façon, advenant que ce soit le reflux d’autres constituants du contenu gastrique hormis l’acide qui provoquent les symptômes, ces derniers risquant peut-être moins d’entraîner une œsophagite érosive, la maîtrise de la production d’acide gastrique pourrait aussi se solder par un échec. Si les traitements antisécrétoires se montrent efficaces dans la plupart des cas de RGO non érosif, il n’en demeure pas moins que la concentration d’acide dans la partie basse de l’œsophage est supérieure aux valeurs physiologiques seulement chez la moitié environ des patients atteints de cette affection12. Dans l’ensemble, la physiopathologie et l’évolution naturelle du RGO non érosif restent entourées d’incertitude.
Pour ce qui est du RGO, la relation qui relie la maîtrise de l’acidité et le soulagement des symptômes est plus complexe et le traitement de cette affection pourrait être grandement amélioré si nous la comprenions mieux
La prise en charge de l’œsophagite est relativement simple, la relation étroite entre l’excès d’acidité et l’inflammation étant corroborée par les taux élevés de guérison obtenus en haussant le pH de la partie basse de l’œsophage. Or pour ce qui est du RGO, la relation qui relie la maîtrise de l’acidité et le soulagement des symptômes est plus complexe et sa prise en charge empirique pourrait être grandement améliorée si nous la comprenions mieux. De toutes les théories plausibles expliquant l’apparition d’un RGO non érosif en l’absence de concentrations élevées d’acide, une des plus solides est très certainement celle qui est fondée sur l’hypersensibilité viscérale13. Plusieurs mécanismes sont à l’origine du déclenchement des signaux de douleur, cause profonde des symptômes du RGO non érosif, qui sont envoyés par les récepteurs nociceptifs de la muqueuse œsophagienne. En plus de l’hypersensibilité au reflux faiblement acide14, on trouve parmi ces mécanismes les altérations microscopiques de l’intégrité de la muqueuse risquant de favoriser le contact entre les nerfs et l’acide et autres constituants du contenu gastrique, d’où l’apparition de symptômes à un pH qui n’est ordinairement pas considéré comme pathologique15. (Tableau 1) Il est possible que certains symptômes évoquant un RGO n’aient rien à voir avec la présence d’acide. Par exemple, les patients ayant un œsophage sensible se plaignent parfois de ressentir des symptômes normalement associés au RGO lorsqu’ils boivent du jus d’agrumes ou de l’alcool, ou qu’ils mangent des tomates ou des plats épicés. L’exposition à ces aliments et boissons n’exacerbe pas forcément le RGO ou le reflux; elle irrite simplement un œsophage qui est déjà sensible ou lésé. Les variations de la motilité imputables à l’altération du péristaltisme peuvent aussi provoquer des symptômes touchant les voies digestives hautes. S’il est vrai que les troubles de la motilité sont bien moins souvent responsables de ce type de symptômes que les brûlures d’estomac causées par l’acidité, il reste que la manométrie à haute résolution rend leur détection beaucoup plus facile aujourd’hui16. Dans de tels cas, la surveillance du pH et de l’impédance, ainsi que les techniques manométriques sont de bons moyens pour mettre au jour les causes sous-jacentes des symptômes chez les patients réfractaires aux IPP. Ces méthodes sont toutefois généralement réservées à ceux dont les symptômes persistent malgré l’essai de plusieurs traitements pharmacologiques, notamment l’administration de doses plus élevées ou plus fréquentes d’IPP.
Traitement : améliorer la maîtrise de l’acidité
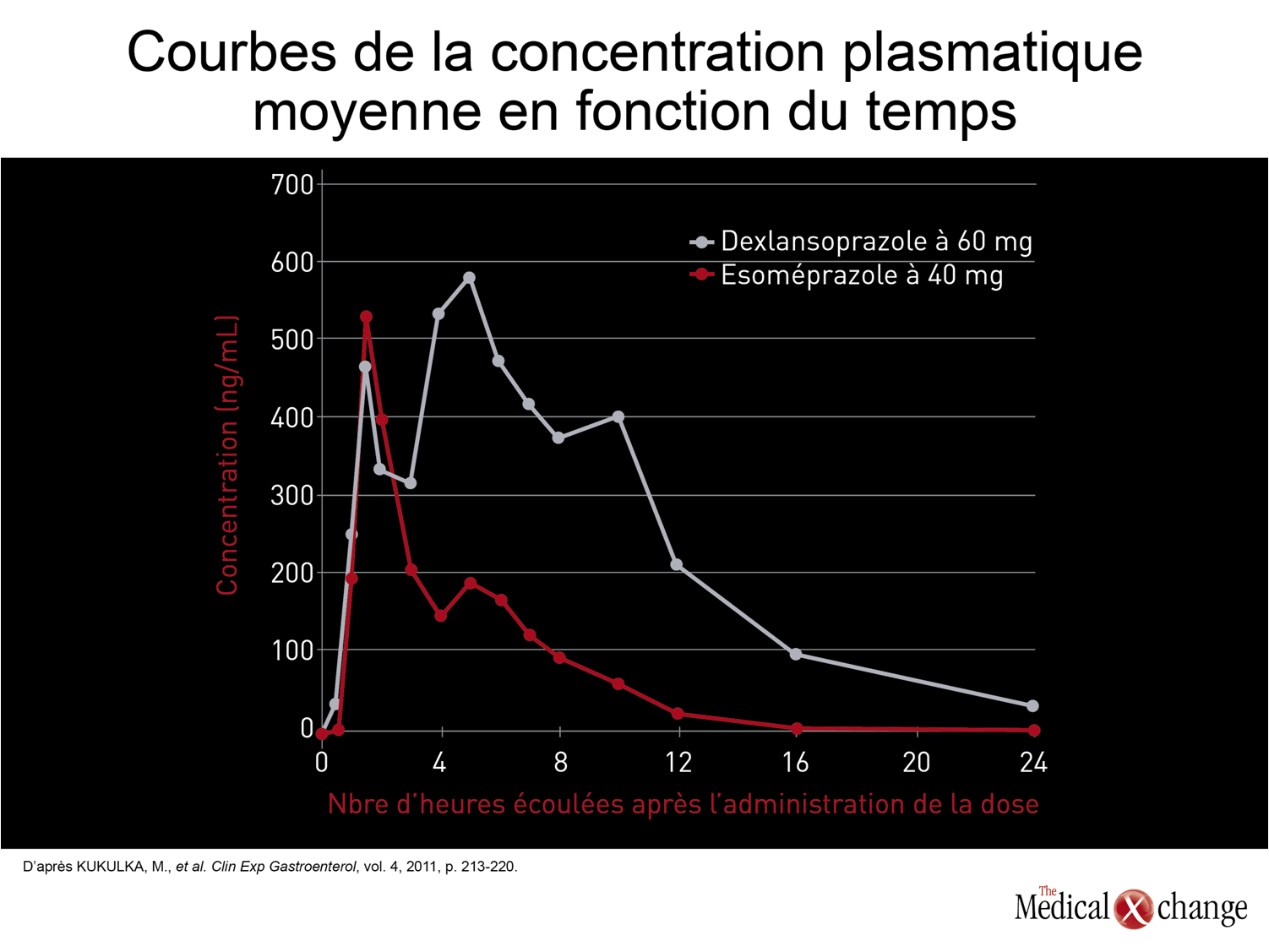
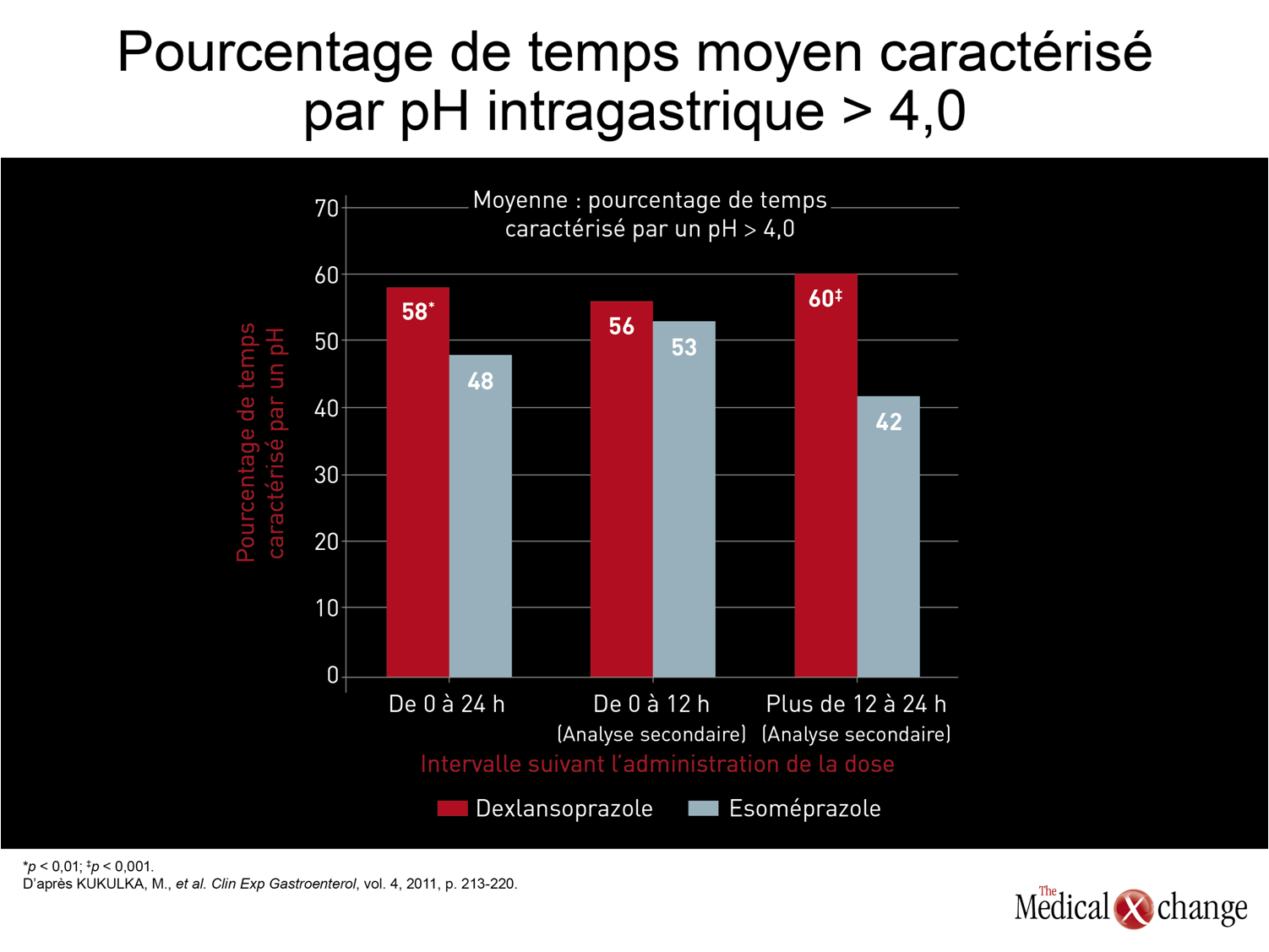
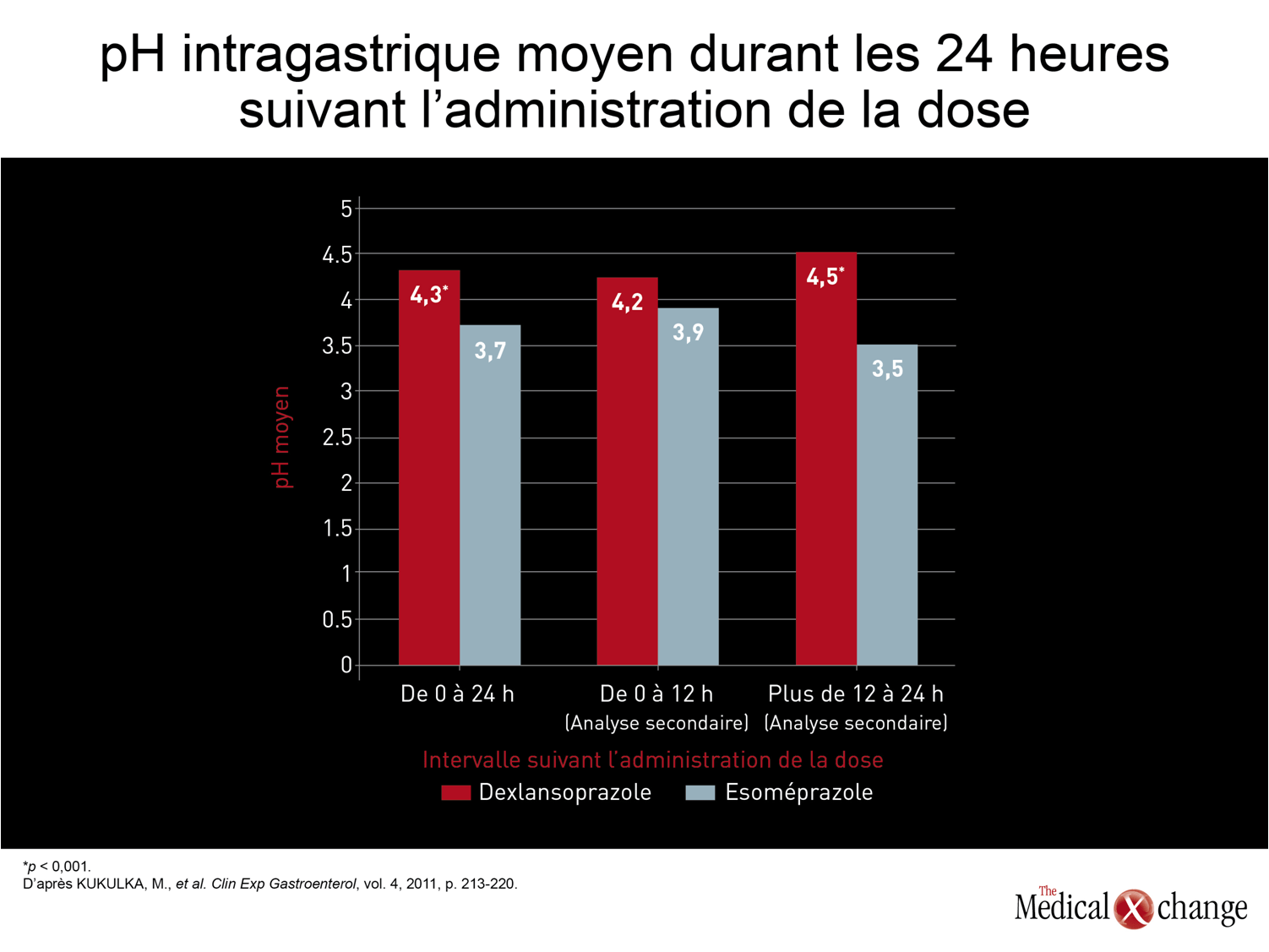
Dans ses lignes directrices, l’ACG recommande l’administration uniquotidienne de doses types d’un IPP dans les cas de symptômes de RGO persistants6. La dose type du premier médicament de cette classe, l’oméprazole, est de 20 mg. Les doses types des IPP commercialisés par la suite, dont la biotransformation et les caractéristiques pharmacocinétiques sont légèrement différentes, vont de 20 à 40 mg. En règle générale, les différences entre les IPP de première génération au chapitre de l’efficacité étaient apparemment minimes, voire nulles. Bien qu’aucune étude d’envergure assortie de paramètres cliniques ayant servi à comparer directement les IPP n’ait été effectuée avant l’arrivée de l’esoméprazole, l’énantiomère lévogyre de l’oméprazole, son composé d’origine, les taux de guérison de l’œsophagite et de maîtrise des symptômes enregistrés chez les patients n’ayant fait l’objet d’aucun examen étaient du même ordre de grandeur. Lors des essais effectués avec l’esoméprazole, qui a permis d’accroître le pourcentage de temps caractérisé par un pH supérieur à 4,0 durant l’intervalle posologique de 24 heures17, les taux de guérison obtenus avec ce médicament se sont révélés supérieurs à ceux rapportés avec les IPP plus anciens, tels que l’oméprazole, mais aussi le lansoprazole, le pantoprazole et le rabéprazole18. Les bienfaits relatifs de l’esoméprazole par rapport à ceux des IPP moins récents ayant permis de constater l’avantage conféré par une meilleure maîtrise de l’acidité dans la prise en charge du RGO, les chercheurs se sont par la suite employés à trouver de nouvelles stratégies pour supprimer efficacement l’acidité d’un intervalle posologique à l’autre afin d’améliorer l’issue clinique des traitements. Certaines de ces stratégies ont simplement consisté à doubler la dose des IPP, notamment en les administrant deux fois par jour plutôt qu’une19ou à y adjoindre un inhibiteur des récepteurs H2 de l’histamine20. Ces stratégies pourraient toutefois comporter certains désavantages, l’un d’eux étant qu’elles ne favorisent pas autant la fidélité au traitement qu’une posologie uniquotidienne. Dernièrement, une autre stratégie fondée sur l’utilisation d’un nouvel IPP, le dexlansoprazole, qui est fabriqué selon une technologie permettant la double libération retardée du médicament (technologie permettant la libération du médicament en deux temps afin d’obtenir deux pics de concentration plasmatique distincts), a été mise de l’avant21. Au cours d’un essai réalisé avec répartition aléatoire des sujets portant sur la mesure du pH intragastrique, le dexlansoprazole s’est montré plus efficace que l’esoméprazole administré à la dose type, tout comme ce dernier s’était révélé plus efficace que les autres IPP plus anciens (Fig. 2)22. Même si le pH moyen mesuré sur une période de 24 heures était supérieur chez les sujets traités par le dexlansoprazole (4,3 vs 3,7; p < 0,003), les différences significatives relevées 12 heures et 24 heures après l’administration de la dose pour ce qui est du pourcentage de temps caractérisé par un pH de plus de 4,0 (60 % vs 42 %; p < 0,001) et du pH moyen (4,5 vs 3,5; p < 0,001) laissent entrevoir une meilleure maîtrise des symptômes de RGO imputables à la production d’acide (Fig. 3) et (Fig. 4).
Lorsqu’il est question du traitement empirique du RGO, on peut raisonnablement s’attendre à ce que les meilleures chances d’obtenir la maîtrise des symptômes viennent d’une meilleure suppression de la production d’acide durant chaque intervalle posologique
Lorsqu’il est question du traitement empirique du RGO, on peut raisonnablement s’attendre à ce que les meilleures chances d’obtenir la maîtrise des symptômes viennent d’une suppression de la production d’acide plus marquée durant chaque intervalle posologique. Or il est particulièrement important de réaliser une telle suppression pendant la nuit, puisque 80 % des patients atteints de RGO se plaignent de symptômes nocturnes et que près de la moitié d’entre eux affirment que la qualité de leur sommeil en souffre23. Compte tenu de l’amélioration modeste obtenue sur le plan thérapeutique en augmentant la dose des IPP administrés une fois par jour, le soulagement insuffisant typiquement observé avec les IPP classiques porte à croire que la suppression de la production d’acide obtenue avec ces médicaments n’est pas assez soutenue. Cette observation est tout à fait logique étant donné que de nouvelles pompes à protons sont formées une fois que les concentrations sériques d’IPP ne sont plus suffisamment élevées pour en inhiber l’activité de manière irréversible. D’ailleurs, les nouvelles pompes à protons sécrétant activement de l’acide qui sont formées vers la fin de l’intervalle posologique de 24 heures réagissent favorablement aux traitements reposant sur l’administration d’IPP dotés d’une plus longue durée d’action, leurs concentrations restant élevées pendant plus longtemps. Pour le moment, les autres stratégies pharmacologiques, comme celles visant à donner plus de tonus au sphincter œsophagien inférieur (SOI), ne semblent pas avoir de bonnes chances de réussite sur le plan clinique, mais elles pourraient s’imposer dans le cadre des études cliniques en cours24. Bien que la chirurgie visant l’amélioration du fonctionnement du SOI reste une option thérapeutique dans les cas de RGO, les bienfaits qu’elle exerce sur les symptômes provoqués par la production d’acide ne sont pas forcément supérieurs à ceux des IPP25. Les stratégies axées sur la libération prolongée de principes actifs durant la formation des pompes à protons restent donc une des avenues les plus intéressantes à explorer pour soulager encore davantage les symptômes.
Conclusion
Chez les patients atteints de RGO, mais ne présentant aucun symptôme alarmant, le traitement empirique au moyen d’un IPP permet à la fois de confirmer le diagnostic et de traiter cette affection. Le taux de réussite obtenu avec les IPP dans le traitement de l’œsophagite est très élevé, les doses types de ces médicaments permettant de guérir la majorité des patients. Aucun autre traitement pharmacologique ne s’est montré supérieur aux IPP pour maîtriser les symptômes. Cela dit, les effets limités des doses types de ces agents suscitent de plus en plus de préoccupations en raison de l’étroite relation entre la persistance des symptômes et l’altération de la qualité de vie qui en découle. Même si la production d’acide n’est pas toujours le facteur dominant chez les patients qui n’obtiennent pas un soulagement satisfaisant de leurs symptômes évoquant un RGO, il est permis d’espérer que l’utilisation d’IPP plus actifs ou une meilleure libération de ces médicaments se traduisent par une suppression encore plus marquée de la production d’acide. Il serait donc bon d’explorer sérieusement cette avenue avant de mener de nouvelles études diagnostiques visant à écarter l’hypothèse des sources de symptômes n’ayant rien à voir avec la production d’acide.
Références
1. VAKIL, N, S. V. van Zanten, P. Kahrilas, J. Dent et R. Jones. « The Montreal definition and classification of gastroesophageal reflux disease: a global evidence-based consensus », Am J Gastroenterol, vol. 101, no 8, 2006, p. 1900-1920; questionnaire 43. 2. THOMSON, A. B., A. N. Barkun, D. Armstrong, et al. « The prevalence of clinically significant endoscopic findings in primary care patients with uninvestigated dyspepsia: the Canadian Adult Dyspepsia Empiric Treatment – Prompt Endoscopy (CADET-PE) study », Aliment Pharmacol Ther, vol. 17, no 12, 2003, p. 1481-1491. 3. FEDORAK, R. N., S. Veldhuyzen van Zanten et R. Bridges. « Canadian Digestive Health Foundation Public Impact Series: gastroesophageal reflux disease in Canada: incidence, prevalence, and direct and indirect economic impact », Can J Gastroenterol, vol. 24, no 7, 2010, p. 431-434. 4. BECHER, A. et J. Dent. « Systematic review: ageing and gastro-oesophageal reflux disease symptoms, oesophageal function and reflux oesophagitis », Aliment Pharmacol Ther, vol. 33, no 4, 2011, p. 442-454. 5. KARAMANOLIS, G., G. Kotsalidis, K. Triantafyllou, et al. « Yield of combined impedance-pH monitoring for refractory reflux symptoms in clinical practice », J Neurogastroenterol Motil, vol. 17, no 2, 2011, p. 158-163. 6. ARMSTRONG, D., J. K. Marshall, N. Chiba, et al. « Canadian Consensus Conference on the management of gastroesophageal reflux disease in adults – update 2004 », Can J Gastroenterol, vol. 19, no 1, 2005, p. 15-35. 7. DEKEL, R., C. Morse et R. Fass. « The role of proton pump inhibitors in gastro-oesophageal reflux disease », Drugs, vol. 64, no 3, 2004, p. 277-295. 8. VAN PINXTEREN, B., M. E. Numans, J. Lau, N. J. de Wit, A. P. Hungin et P. A. Bonis. « Short-term treatment of gastroesophageal reflux disease »,J Gen Intern Med, vol. 18, no 9, 2003, p. 755-763. 9. ARMSTRONG, D., S. J. Veldhuyzen van Zanten, A. N. Barkun, et al. « Heartburn-dominant, uninvestigated dyspepsia: a comparison of ‘PPI-start’ and ‘H2-RA-start’ management strategies in primary care–the CADET-HR Study », Aliment Pharmacol Ther, vol. 21, no 10, 2005, p. 1189-1202. 10. BECHER, A. et H. El-Serag. « Systematic review: the association between symptomatic response to proton pump inhibitors and health-related quality of life in patients with gastro-oesophageal reflux disease », Aliment Pharmacol Ther, vol 34, no 6, 2011, p. 618-627. 11. FASS R. « Non-erosive reflux disease (NERD) and erosive esophagitis–a spectrum of disease or special entities? », Z Gastroenterol, vol. 45, no 11, 2007, p. 1156-1163. 12. MARTINEZ, S. D., I. B. Malagon, H. S. Garewal, H. Cui et R. Fass. « Non-erosive reflux disease (NERD)–acid reflux and symptom patterns », Aliment Pharmacol Ther, vol. 17, no 4, 2003, p. 537-545. 13. KNOWLES, C. H. et Q. Aziz. « Visceral hypersensitivity in non-erosive reflux disease », Gut, vol. 57, no 5, 2008, p. 674-683. 14. MIWA, H., T. Kondo, T. Oshima, H. Fukui, T. Tomita et J. Watari. « Esophageal sensation and esophageal hypersensitivity – overview from bench to bedside », J Neurogastroenterol Motil, vol. 26, no 4, 2010, p. 353-362. 15. FARRE, R., F. Fornari, K. Blondeau, et al. « Acid and weakly acidic solutions impair mucosal integrity of distal exposed and proximal non-exposed human oesophagus », Gut, vol. 59, no 2, 2010, p. 164-169. 16. ROMAN, S., F. Zerbib, K. Belhocine, S. B. des Varannes et F. Mion. « High resolution manometry to detect transient lower oesophageal sphincter relaxations: diagnostic accuracy compared with perfused-sleeve manometry, and the definition of new detection criteria », Aliment Pharmacol Ther, vol. 34, no 3, 2011, p. 384-393. 17. MINER, P., fils, P. O. Katz, Y. Chen et M. Sostek. « Gastric acid control with esomeprazole, lansoprazole, omeprazole, pantoprazole, and rabeprazole: a five-way crossover study », Am J Gastroenterol, vol. 98, no 12, 2003, p. 2616-2620. 18. GRALNEK, I. M., G. S. Dulai, M. B. Fennerty et B. M. Spiegel. « Esomeprazole versus other proton pump inhibitors in erosive esophagitis: a meta-analysis of randomized clinical trials », Clin Gastroenterol Hepatol, vol. 4, no 12, 2006, p. 1452-1458. 19. FASS, R. « Proton pump inhibitor failure–what are the therapeutic options? », Am J Gastroenterol, vol. 104 (suppl. 2), 2009, p. S33-S38. 20. MAINIE, I., R. Tutuian et D. O. Castell. « Addition of a H2 receptor antagonist to PPI improves acid control and decreases nocturnal acid breakthrough »,J Clin Gastroenterol, vol. 42, no 6, 2008, p. 676-679. 21. VAKILY, M., W. Zhang, J. Wu, S. N. Atkinson, D. Mulford. « Pharmacokinetics and pharmacodynamics of a known active PPI with a novel Dual Delayed Release technology, dexlansoprazole MR: a combined analysis of randomized controlled clinical trials », Curr Med Res Opin, vol. 25, no 3, 2009, p. 627-638. 22. KUKULKA, M., C. Eisenberg et S. Nudurupati. « Comparator pH study to evaluate the single-dose pharmacodynammics of dualy delayed-released dexlansoprazole 60 mg and delayed-release esomeprazole 40 mg. Clinical and Experimental Gastroenterology, vol. 4, 2011, p. 213-220. 23. FARUP, C., L. Kleinman, S. Sloan, et al. « The impact of nocturnal symptoms associated with gastroesophageal reflux disease on health-related quality of life », Arch Intern Med, vol. 161, no 1, 2001, p. 45-52. 24. BLONDEAU, K. « Treatment of gastro-esophageal reflux disease: the new kids to block », Neurogastroenterol Motil, vol. 22, no 8, 2010, p. 836-840. 25. GALMICHE, J. P., J. Hatlebakk, S. Attwood, et al. « Laparoscopic antireflux surgery vs esomeprazole treatment for chronic GERD: the LOTUS randomized clinical trial », JAMA, vol. 305, no 19, 2011, p. 1969-1977. 26. ANVARI, M., C. Allen, J. Marshall, et al. « A randomized controlled trial of laparoscopic Nissen fundoplication versus proton pump inhibitors for the treatment of patients with chronic gastroesophageal reflux disease (GERD): 3-year outcomes », Surg Endosc, vol. 25, no 8, 2011, p. 2547-2554.
Chapitre 1 : Les enjeux actuels dans la maîtrise du RGO
Les raisons pour lesquelles certains patients atteints de reflux gastro-œsophagien (RGO) ne réussissent pas à soulager leurs symptômes de manière satisfaisante au moyen des inhibiteurs de la pompe à protons (IPP) se sont révélées étonnamment complexes. Même si les doses classiques d’IPP à administration uniquotidienne permettent de guérir l’œsophagite érosive chez un grand nombre de patients, beaucoup d’entre eux continuent d’éprouver des symptômes une fois cette affection guérie. Comparativement aux patients atteints d’œsophagite, le pourcentage de ceux qui présentent un RGO donnant des résultats négatifs à l’endoscopie (RGO non érosif) et qui obtiennent un soulagement insuffisant de leurs symptômes est encore plus élevé. Les multiples travaux de recherche réalisés sur le lien entre le reflux, acide ou non, et les symptômes de RGO ont permis de mieux comprendre les mécanismes physiopathologiques qui entrent en jeu. Les nouvelles perspectives issues de ces travaux orientent maintenant les stratégies susceptibles de combler les lacunes des traitements actuels. En substance, il a été démontré que le RGO est une entité hétérogène caractérisée par d’autres facteurs étiologiques favorisants hormis la sécrétion excessive d’acide gastrique. Or une démarche systématique visant à mieux cerner les principaux mécanismes à l’origine des symptômes permettrait vraisemblablement d’améliorer l’issue des traitements.
Afficher la revue