Revue d’experts
Prise en charge de la baisse du désir sexuel chez la femme
Chapitre 3 : Traitements – Pharmacologie
James G. Pfaus, Ph. D., IF
Professeur, Département de psychologie
Chercheur, Groupe de recherche en neurobiologie comportementale (GRNC)
Université Concordia, Montréal, Québec
Atlanta – Selon les estimations, 1 femme sur 10 connaîtrait une baisse de désir sexuel1. Or plusieurs agents pharmacologiques prometteurs qui seraient utilisés en appoint aux sexothérapies classiques font présentement l’objet d’essais cliniques. Il s’agit d’hormonothérapies et d’agents qui ciblent le système nerveux central (SNC) afin de stimuler l’excitation sexuelle ou d’émousser l’inhibition sexuelle dans des régions particulières de l’encéphale qui jouent un rôle essentiel dans le désir sexuel. Ces agents pharmacologiques novateurs sont les nouveaux instruments d’une démarche plus globale et axée sur les patientes dans le traitement de la baisse du désir sexuel.
Introduction
La reconnaissance de la baisse de désir sexuel, une affection qui peut être traitée au moyen d’interventions psychologiques, d’agents pharmacologiques ou d’une combinaison des deux, passe obligatoirement par une entrevue d’approche clinique approfondie jumelée à des instruments tels que le questionnaire DSDS (Decreased Sexual Desire Screener)2. Or de nouveaux agents opposés aux anomalies neurobiologiques et aux mécanismes sous-jacents à la baisse de désir ont récemment fait leur apparition. Plus précisément, des agents qui ciblent le SNC et des régions de l’encéphale telles que le cortex préfrontal, le locus cœruleus, l’aire ventro-tegmentale ainsi que le noyau préoptique médial de l’hypothalamus, ont fait preuve d’efficacité dans le cadre d’essais cliniques. Au moins un de ces agents exerçant son action sur le SNC, la flibansérine, a été homologué par la Food and Drug Administration des États-Unis et a été soumis à Santé Canada aux fins d’examen3. Il est toutefois à prévoir que le brémélanotide et d’autres agents expérimentaux qui agissent sur le SNC et modulent les voies cérébrales jouant un rôle crucial dans le désir sexuel soient un jour disponibles pour les femmes ménopausées ou non. Les cliniciens disposeront ainsi d’un plus large éventail d’options pharmacologiques, ce qui leur permettra de mieux adapter leurs stratégies thérapeutiques aux besoins de chaque patiente présentant une baisse de désir sexuel.
La petite histoire des agents pharmacologiques opposés à la baisse de désir sexuel
L’arsenal pharmacologique ne leur proposant aucun agent expressément indiqué contre la baisse de désir sexuel, les cliniciens ont dû utiliser des médicaments qui n’étaient pas homologués pour le traitement de cette affection, notamment de la testostérone, une hormone offrant certains avantages, mais soulevant aussi quelques préoccupations à propos de son innocuité à long terme, quoique dans une moindre mesure lorsqu’elle est administrée par voie transdermique4. La buspirone, un agoniste partiel des récepteurs 5-HT1A qui est indiqué dans le traitement de l’anxiété généralisée, a connu un certain succès dans la prise en charge de la baisse de désir sexuel5, tout comme le bupropion6, un inhibiteur de la recapture de la noradrénaline et de la dopamine qui employé dans le traitement de la dépression et qui est aussi prescrit aux personnes souhaitant cesser de fumer. Bien que ces deux médicaments permettent d’agir sur le SNC, aucun d’eux n’a fait l’objet d’études sur son utilisation en monothérapie contre la baisse de désir sexuel, une indication qui de toute manière n’est pas homologuée. Qui plus est, nous ne disposons d’aucune donnée portant sur l’innocuité du bupropion et de la buspirone dans la prise en charge des femmes affligées d’une baisse du désir sexuel.
Justification de l’utilisation de médicaments agissant sur le SNC pour traiter la baisse de désir sexuel
Le dilemme de la baisse de désir tire son origine d’un « problème de réseau », a affirmé le Dr Irwin Goldstein, Professeur clinicien de chirurgie à l’École de médecine de San Diego à l’Université de Californie, Directeur du Service de médecine, de l’Hôpital Alvarado de San Diego et Directeur du San Diego Sexual Medicine, en Californie. Les voies intervenant dans le désir sexuel mettent en jeu des neurotransmetteurs excitateurs majeurs qui font partie intégrante des systèmes excitateurs de l’encéphale, dont la dopamine, les mélanocortines, l’oxytocine, la vasopressine et la noradrénaline. Ces transmetteurs agissent sur les voies neuronales de l’hypothalamus, du système limbique et du cortex. À l’opposé, les principaux neurotransmetteurs intervenant dans l’inhibition sexuelle comprennent les opioïdes et la sérotonine (5-HT). Les systèmes inhibiteurs peuvent émousser les systèmes excitateurs au point où l’excitation sexuelle qui serait normalement générée par des stimuli sexuels efficaces ne l’est pas1. « Nous avons affaire à des femmes peu excitées ou extrêmement inhibées, a expliqué le Dr Goldstein alors qu’il décrivait les patientes aux prises avec une baisse de désir sexuel. Les systèmes qui déclenchent l’excitation ne sont pas activés, alors que ceux qui l’inhibent le sont trop. C’est vraiment un problème de réseau (dans l’encéphale) que nous pouvons manipuler à notre avantage pour aider certaines de nos patientes ». Les clichés de l’encéphale obtenus à l’aide de techniques d’imagerie par résonance magnétique fonctionnelle dans le cadre d’une étude montrent à quel point ceux des femmes présentant une baisse de désir sexuel sont différents de ceux des témoins en santé7. Les chercheurs ont comparé la réaction de femmes n’ayant aucun antécédent de dysfonctionnement sexuel à des vidéos érotiques, des matches de sport ou des images apaisantes à celle de femmes aux prises avec une baisse de désir sexuel. Ils ont remarqué chez ces dernières une activation plus marquée de la circonvolution frontale moyenne et de la circonvolution frontale inférieure droite, ainsi qu’une activation bilatérale du putamen. Ils en sont venus à la conclusion que chez ces patientes, l’encodage des stimuli déclenchant l’excitation sexuelle et la récupération des expériences érotiques du passé, ou les deux, sont différents de ceux des femmes dont le désir sexuel est jugé normal7. « L’encéphale des femmes indemnes de cette anomalie s’illumine lorsqu’il est exposé à des stimuli sexuels, ce qui n’est pas le cas des femmes qui en sont atteintes », a affirmé le Dr Goldstein. En outre, lors d’une autre étude, les chercheurs ont exposé des femmes affligées d’une baisse de désir sexuel à deux extraits de films à saveur plus ou moins érotique (élevée et faible) et de films dénués d’érotisme (neutres). Ils ont constaté une diminution de la désactivation du côté gauche de la région cérébrale régulant le fonctionnement multitâche, conjuguée à une activation moins prononcée du côté droit du cerveau ou à une désactivation plus marquée du cortex orbitofrontal médian8. « Le sexe exige que les régions cérébrales régissant le fonctionnement multitâche soient mises en veilleuse, a déclaré le Dr Goldstein. Vous devez être en mesure de désactiver tout ce qui vient lui faire concurrence dans le cerveau. Il faut oublier la lessive, la préparation des repas, les enfants et vos finances ».
Pharmacothérapies opposées à la baisse de désir sexuel
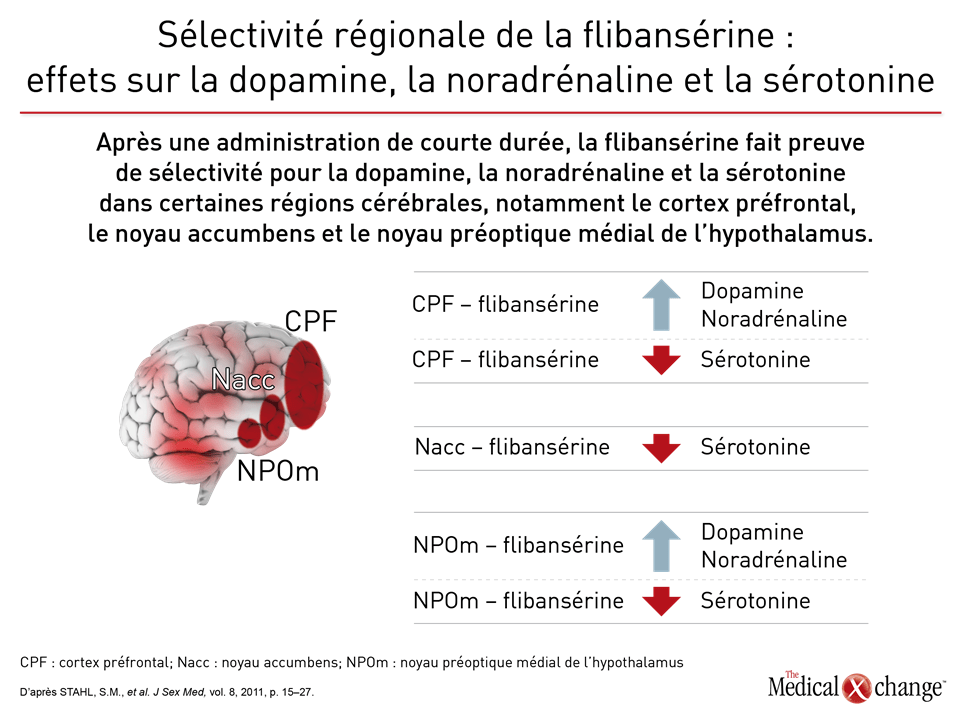
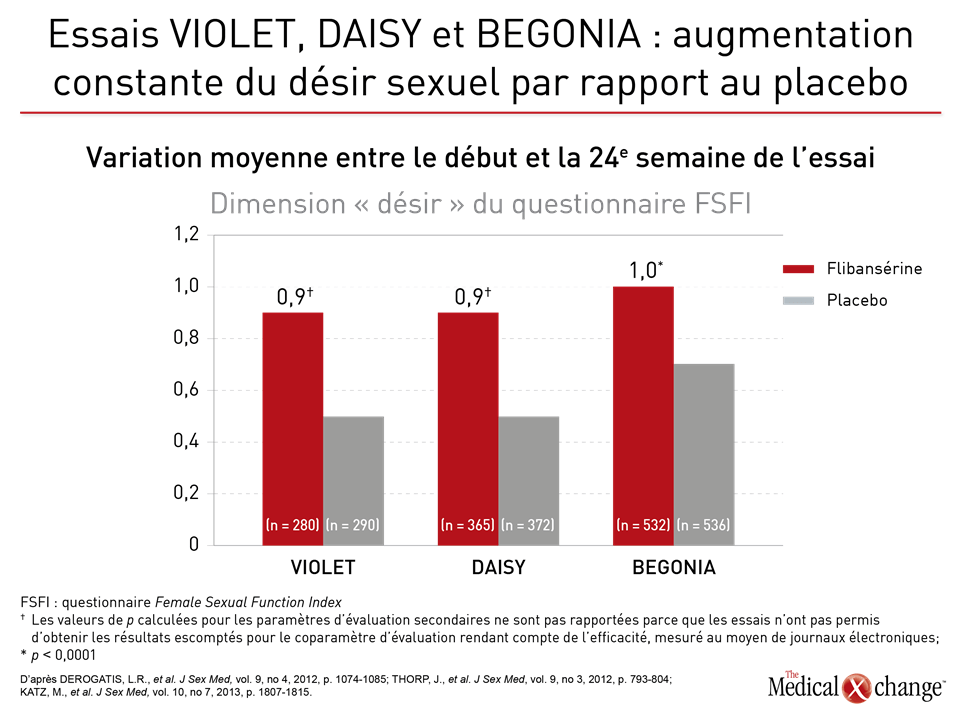
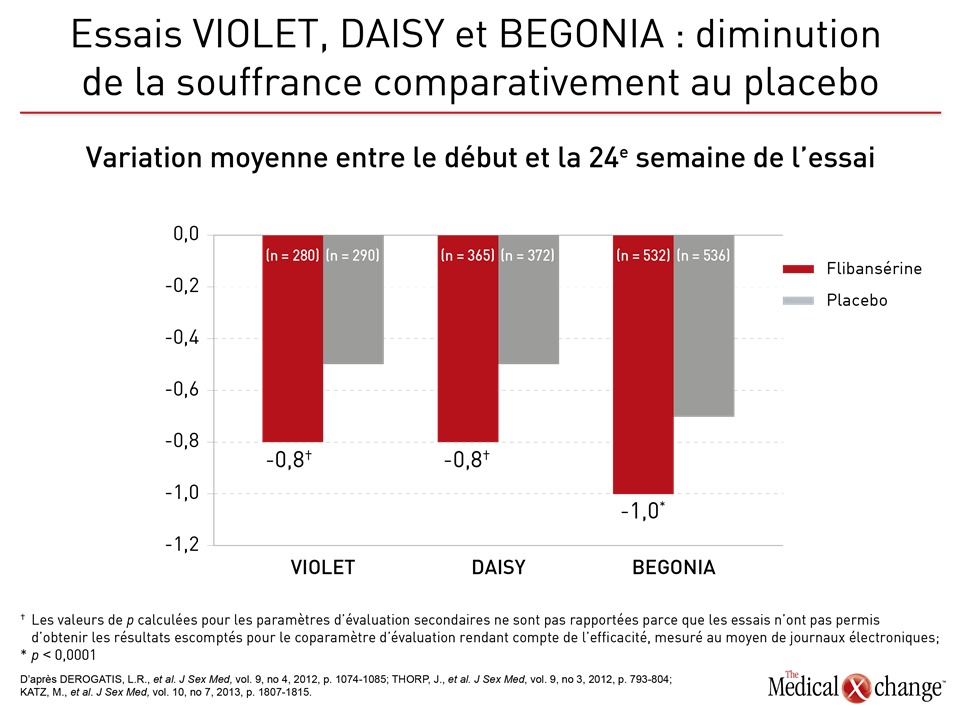
Flibansérine « Un agent comme la flibansérine régit l’activation du cortex préfrontal en l’atténuant, ce qui stoppe le fonctionnement multitâche du cerveau et élimine la distractibilité pendant les rapports sexuels. Tout est une question de réseaux cérébraux; la magie n’a rien à y voir », a expliqué le Dr Goldstein (Fig. 1)9. Le mode d’action de la flibansérine dans le traitement de la baisse de désir sexuel s’exercerait d’abord sur les récepteurs sérotoninergiques cérébraux. Pour être plus précis, disons que cet agent inhibe la libération de sérotonine en se liant aux autorécepteurs 5-HT1A tout en bloquant les effets postsynaptiques de la sérotonine sur les récepteurs 5-HT2A (Fig. 2)10. Résultat : la transmission dopaminergique hypothalamique et mésolimbique est amplifiée et empêche la sérotonine d’exercer son effet inhibiteur sexuel sur le cortex préfrontal. Trois essais menés à double insu et avec répartition aléatoire intitulés DAISY, VIOLET et BEGONIA ont servi à comparer l’efficacité et l’innocuité de la flibansérine à celle d’un placebo chez des femmes non ménopausées. La conclusion des chercheurs : la flibansérine s’est montrée supérieure au placebo pour de nombreux paramètres d’évaluation11, 12, 13. Lors de l’essai DAISY, des doses de 100 mg de flibansérine prises une fois par jour ont permis d’obtenir, par rapport au placebo, une amélioration statistiquement significative des paramètres d’évaluation suivants : rapports sexuels satisfaisants, désir sexuel (mesuré à partir des résultats enregistrés pour la dimension « désir » du questionnaire FSFI [Female Sexual Function Index]), fonction sexuelle et diminution de la souffrance ressentie par la femme en raison de sa vie sexuelle (évaluée d’après le score total et celui obtenu pour la dimension 13 du questionnaire FSDS-R [Female Sexual Distress Scale-Revised])11. L’essai VIOLET, qui a porté sur l’administration de doses quotidiennes de 100 mg de flibansérine, a aussi permis de constater une augmentation significative sur le plan statistique des rapports sexuels satisfaisants. Le score enregistré pour la dimension « désir » et le score total obtenus au questionnaire FSFI ont en effet augmenté d’une manière statistiquement significative, alors que le score total et celui enregistré pour la dimension 13 du questionnaire FSDS-R ont chuté de la même façon12. Par ailleurs, les données issues de l’essai BEGONIA cadraient avec celles collectées pendant les deux autres essais. Comparativement au placebo, la flibansérine y a permis d’objectiver des augmentations significatives du nombre de rapports sexuels satisfaisants et du désir sexuel comme en faisait foi le score enregistré pour la dimension « désir » du questionnaire FSFI, de même qu’une atténuation de la souffrance éprouvée par la femme en raison de sa vie sexuelle dysfonctionnelle et de la faiblesse de son désir sexuel, qu’ont particulièrement fait ressortir le score total et celui observé pour la dimension 13 du questionnaire FSDS-R (Figures 3 (Fig. 3) et 4 (Fig. 4))13. La flibansérine n’a pas soulevé de préoccupations majeures en matière d’innocuité, les effets indésirables documentés avec ce médicament étant des vertiges, des nausées, de l’insomnie, de la somnolence et de l’anxiété. Notons toutefois que la consommation d’alcool est contre-indiquée avec ce médicament en raison des risques d’hypotension ou de syncope au début du traitement. Une analyse réalisée a posteriori à partir des données issues des essais VIOLET, DAISY et BEGONIA présentée devant l’ISSWSH par le Dr James A. Simon, CCD, NCMP, FACOG, Professeur clinicien d’endocrinologie de la reproduction, d’infertilité, d’obstétrique et de gynécologie à l’École de médecine de l’Université George Washington, de Washington, D.C., a révélé que le taux de réaction favorable au traitement se situait entre 74,4 et 82,2 % chez les femmes non ménopausées affligées d’une baisse de désir sexuel et que le délai médian pour l’obtenir était de deux mois environ. « Ces résultats nous portent à croire qu’un traitement de courte durée est suffisant pour savoir s’il fonctionne ou non chez une patiente donnée, a affirmé le Dr Simon. À vrai dire, il est recommandé d’y mettre fin si la patiente ne constate aucune amélioration au bout de huit semaines ». Répondant aux questions sur les données et sur les quelques cas de femmes ayant eu besoin de plus de deux mois pour ressentir les bienfaits du traitement, le Dr Simon a précisé que, dans un contexte réel, la décision de poursuivre le traitement au-delà des huit semaines serait bien sûr laissée à la discrétion du médecin et de la patiente advenant qu’ils s’attendent à ce que les effets positifs de la flibansérine soient imminents. Brémélanotide Le brémélanotide, un agoniste des récepteurs de type 4 de la mélanocortine, est un autre agent ciblant le SNC qui est administré, au besoin, par voie sous-cutanée au moyen d’un auto-injecteur pour traiter la baisse de désir sexuel14. L’étude RECONNECT, qui était composée de deux essais multicentriques de phase III, a servi à évaluer l’efficacité et l’innocuité de cet agent dans le traitement de la baisse de désir sexuel chez les femmes non ménopausées. Les données tirées de ces deux essais ont révélé que comparativement à celles qui avaient reçu le placebo, les femmes qui avaient été traitées par le brémélanotide avaient obtenu des résultats significativement meilleurs pour ce qui était des paramètres d’évaluation tels que la dimension « désir » du questionnaire FSFI (p < 0,0001 pour les deux essais) et le score obtenu pour la dimension « désir, excitation/orgasme » du questionnaire FSDS (p < 0,0001 pour un des essais et p = 0,0007 pour l’autre). Les chercheurs ont également demandé aux patientes leur opinion à propos de ce médicament injectable. Pour ce faire, ils leur ont posé la question suivante : « Selon vous, dans quelle mesure ce médicament vous a-t-il été bénéfique? ». Pour être considérées comme ayant réagi favorablement au traitement, les femmes devaient avoir accordé aux bienfaits qu’elles en avaient retirés une note de 5 ou plus sur une échelle de Likert de 7 points. Or au total, 59 % et 58 % des patientes du premier et du deuxième essai respectivement ont été considérées comme telles. Les résultats enregistrés pour les paramètres d’évaluation secondaires ont aussi été documentés pendant ces deux essais. Lors de la réunion annuelle de l’ISSWSH, le Dr Leonard DeRogatis, Directeur du Centre de santé sexuelle du Maryland, situé à Baltimore, au Maryland, a présenté les données ayant permis d’établir un parallèle entre le brémélanotide et des améliorations significatives du score total obtenu au questionnaire FSFI et de ceux enregistrés pour les dimensions « excitation », « lubrification », « orgasme » et « satisfaction » de ce questionnaire (p ≤ 0,01 dans tous les cas).
Répercussions du traitement chez un petit effectif de patientes
Selon Sue Goldstein, CCRC, AASECT-CSC, IF, Chef de la Division de recherche clinique et de la programmation didactique de la San Diego Sexual Medicine, de Californie, les femmes d’un petit effectif de sujets, ménopausées ou non, qui s’étaient fait prescrire de la flibansérine et ayant fait l’objet d’une analyse thématique récente présentée lors de la réunion annuelle de l’ISSWSH, ont affirmé avoir constaté des changements de nature sexuelle et non sexuelle après avoir pris ce médicament. Les chercheurs n’ont pas posé de questions précises à ces femmes. Ils leur ont plutôt demandé de leur parler que leur expérience avec la flibansérine. Au total, 23 patientes traitées par ce médicament ont affirmé avoir constaté une augmentation de leur libido, une intensification de leurs orgasmes, une plus grande réceptivité envers l’activité sexuelle et avoir pris davantage l’initiative des rapports sexuels. Certaines d’entre elles ont également déclaré avoir remarqué des répercussions autres que sexuelles dans leur vie; elles se sentaient plus heureuses, moins stressées et moins anxieuses. « Pendant qu’elles prenaient ce médicament, elles se sentaient vraiment comme des êtres sexués et pleines d’énergie », a fait remarquer Sue Goldstein, en admettant toutefois que cette analyse comportait plusieurs lacunes, dont l’absence d’un protocole d’étude rigoureux et la petite taille de l’effectif de sujets.
Traitements actuellement à l’étude
D’autres agents destinés au traitement de la baisse de désir sexuel chez la femme non ménopausée et conçus pour une utilisation à la demande sont actuellement à l’étude. Parmi ces médicaments novateurs, on trouve un produit ayant comme principes actifs de la testostérone et du sildénafil (un inhibiteur de la phosphodiestérase de type 5 qui est utilisé pour traiter le dysfonctionnement érectile chez l’homme). La testostérone vise à amplifier la réceptivité du cerveau aux signaux sexuels et le sildénafil, à intensifier l’excitation génitale15. Un autre agent expérimental renferme de la testostérone et de la buspirone, un agoniste partiel des récepteurs 5‑HT1A16. La testostérone qu’il contient augmente la sensibilité du cerveau aux signaux sexuels alors que la buspirone bloque les mécanismes inhibiteurs dans le cortex préfrontal. L’association composée de trazodone, un anxiolytique, et de bupropion, un antidépresseur, est encore à l’étape expérimentale dans le traitement de la baisse de désir sexuel17. Cette association rendrait le passage d’un état d’excitation sexuelle à un autre, d’inhibition, plus facile, ce qui offrirait aux femmes la possibilité d’accueillir leur excitation sexuelle quand les circonstances s’y prêtent et au moment où elles le désirent.
Conclusion
Les femmes affligées d’une baisse du désir sexuel ont toutes les raisons d’être optimistes. En effet, l’avenir s’annonce très prometteur sur le plan thérapeutique. Les cliniciens disposent déjà de la flibansérine, l’arrivée du brémélanotide sur le marché est imminente et d’autres agents expérimentaux pourraient bien devenir les prochains outils des médecins appelés à traiter cette forme de dysfonctionnement sexuel. En outre, les médicaments qui ciblent le SNC fournissent de nouvelles stratégies pour la prise en charge de cette affection. Un des enjeux associés à la recherche de nouveaux agents pharmacologiques consiste à s’assurer que les patientes et les cliniciens aient non seulement accès à une information juste sur leur mode d’action et sur leur efficacité, mais aussi qu’ils puissent disposer de stratégies thérapeutiques plus globales de façon que l’option dont les patientes ont besoin soit à leur portée et qu’elles en retirent les meilleurs résultats possibles.
Références
- GOLDSTEIN, I., N. N. Kim, A. H. Clayton, et al. « Hypoactive Sexual Desire Disorder: International Society for the Study of Women’s Sexual Health (ISSWSH) Expert Consensus Panel Review », Mayo Clin Proc, vol. 92, no1, janvier 2017, p. 114-128.
- CLAYTON, A. H., E. R. Goldfischer, I. Goldstein, L. DeRogatis, D. J. Lewis-D’Agostino et R. Pyke. « Validation of the decreased sexual desire screener (DSDS) », J Sex Med, vol. 6, no3, mars 2009, p. 730-738.
- JOFFE, H. V., C. Chang, C. Sewell, et al. « FDA Approval of Flibanserin—Treating Hypoactive Sexual Desire Disorder », N Eng J Med, vol. 374, no2, 14 janvier 2016, p. 101-104.
- BRAUNSTEIN, G. D., D. A. Sundwall, M. Katz, et al. « Safety and efficacy of a testosterone patch for the treatment of hypoactive sexual desire disorder in surgically menopausal women: a randomized, placebo-controlled trial », Arch Intern Med, vol. 165, no14, juillet 2005, p. 1582-1589.
- LANDEN, M., E. Eriksson, H. Agren et T. Fahlen. « Effect of buspirone on sexual dysfunction in depressed patients treated with selective serotonin reuptake inhibitors », J Clin Psychopharmacol, vol. 19, no3, juin 1999, p. 268-271.
- SEGRAVES, R. T., A. Clayton, H. Croft, A. Wolf et J. Warnock. « Bupropion sustained release for the treatment of hypoactive sexual desire disorder in premenopausal women », J Clin Psychopharmacol, vol. 24, no3, juin 2004, p. 339-342.
- ARNOW, B. A., L. Millheiser, A. Garrett, et al. « Women with hypoactive sexual desire disorder compared to normal females: a functional magnetic resonance imaging study », Neuroscience, vol. 158, no2, 23 janvier 2009, p. 484-502.
- HUYNK, H. K., C. Beers, A. Willemsen, et al. « High-intensity erotic visual stimuli de-activate the primary visual cortex in women », J Sex Med, vol. 9, no6, juin 2012, p. 1579-1587.
- STAHL, S. M., B. Sommer et K. A. Allers. « Multifunctional pharmacology of flibanserin: possible mechanism of therapeutic action in hypoactive sexual desire disorder », J Sex Med, vol. 8, no1, janvier 2011, p. 15-27.
- PFAUS, J. G. « Treatment for hypoactive sexual desire », Cell, vol. 163, no3, 22 octobre 2015, p. 533.
- THORP, J., J. Simon, D. Dattani, et al. « Treatment of hypoactive sexual desire disorder in premenopausal women: efficacy of flibanserin in the DAISY study », J Sex Med, vol. 9, no3, mars 2012, p. 793-804.
- DEROGATIS, L. R., L. Komer, M. Katz, et al. « Treatment of hypoactive sexual desire disorder in premenopausal women: efficacy of flibanserin in the VIOLET study », J Sex Med, vol. 9, no4, avril 2012, p. 1074-1085.
- KATZ, M., L. R, DeRogatis, R. Ackerman, et al. « Efficacy of flibanserin in women with hypoactive sexual desire disorder: results from the BEGONIA trial », J Sex Med, vol. 10, no7, juillet 2013, p. 1807-1815.
- CLAYTON, A. H., J. Lucas, L. R. DeRogatis et R. Jordan. « Phase I Randomized Placebo-Controlled, Double-Blind Study of the Safety and Tolerability of Bremelanotide Coadministered with Ethanol in Healthy Male and Female Participants », Clin Ther, 9 février 2017.
- BIOEMERS, J., K. van Rooij, L. de Leede, et al. « Single dose sublingual testosterone and oral sildenafil vs. a dual route/dual release fixed dose combination tablet: a pharmacokinetic comparison », Br J Clin Pharmacol, vol. 81, no6, juin 2016, p. 1091-102.
- VAN ROOIJ, K., S. Poels, P. Worst, et al. « Efficacy of testosterone combined with a PDE5 inhibitor and testosterone combined with a serotonin (1A) receptor agonist in women with SSRI-induced sexual dysfunction. A preliminary study », Eur J Pharmacol, vol. 753, 15 avril 2015, p. 246-251.
- FARMER, M., H. Yoon et I. Goldstein. « Future Targets for Female Sexual Dysfunction », J Sex Med,13, no 8, août 2016, p. 1147-1165.
Chapitre 3 : Traitements – Pharmacologie
Atlanta – Selon les estimations, 1 femme sur 10 connaîtrait une baisse de désir sexuel1. Or plusieurs agents pharmacologiques prometteurs qui seraient utilisés en appoint aux sexothérapies classiques font présentement l’objet d’essais cliniques. Il s’agit d’hormonothérapies et d’agents qui ciblent le système nerveux central (SNC) afin de stimuler l’excitation sexuelle ou d’émousser l’inhibition sexuelle dans des régions particulières de l’encéphale qui jouent un rôle essentiel dans le désir sexuel. Ces agents pharmacologiques novateurs sont les nouveaux instruments d’une démarche plus globale et axée sur les patientes dans le traitement de la baisse du désir sexuel.
Afficher la revue