oncologie
15e réunion scientifique annuelle de la Society for Neuro-Oncology (SNO)
Aborder les enjeux complexes du glioblastome multiforme
Montréal – Une énergie et des ressources considérables sont déployées en recherche afin d’améliorer l’issue des glioblastomes multiformes nouvellement diagnostiqués ou récidivants. Les présentations dont il est question ci-apres témoignent de l’efficacité et de l’innocuité des traitements de première intention types (radiothérapie et/ou témozolomide) chez les personnes âgées, une population pour laquelle on a souvent limité les traitements par crainte de leurs effets toxiques. Les patients qui ne réagissent pas favorablement aux traitements existants ont grandement besoin de stratégies thérapeutiques efficaces. Pour ce faire, des chercheurs s’emploient actuellement à étudier le rôle du témozolomide dans le cadre de traitements plus intensifs, l’utilisation du bevacizumab et le rôle de nouvelles cibles moléculaires.
La liste des présentations données pendant la réunion de la SNO de cette année confirme qu’une énergie et des ressources considérables sont déployées en recherche pour tenter d’améliorer l’issue des glioblastomes multiformes nouvellement diagnostiqués ou récidivants. Dans le cadre de ces projets, on tente grosso modo de perfectionner les schémas thérapeutiques actuels ou de mieux les cibler, et de mettre au point de nouveaux agents et de nouvelles associations. Les données qui commencent à être diffusées des deux côtés sont prometteuses et laissent entrevoir que d’ici quelques années, les taux de survie au glioblastome multiforme grimperont de façon marquée grâce à des traitements efficaces et tolérables qui seront taillés sur mesure pour les patients et les tumeurs en cause.
La prise en charge des patients atteints d’un glioblastome multiforme nouvellement diagnostiqué comporte typiquement l’exérèse de la tumeur la plus complète possible, suivie de traitements de radiothérapie administrés de manière concomitante avec des doses quotidiennes de témozolomide (TMZ, à 75 mg/m2 pendant 6 semaines), puis l’administration adjuvante de TMZ (de 150 à 200 mg/m2 pendant 5 jours sur 28). Au cours de leur étude phare, Stupp et ses collègues (N Engl J Med, vol. 352, n° 10, 2005, p. 987-996) ont démontré que ce schéma thérapeutique avait permis de prolonger la survie médiane des patients d’à peu près 37 %, celle-ci se chiffrant à 15 mois environ. Le taux de survie à deux ans était plus de deux fois plus élevé chez les patients du groupe traité par le TMZ que chez les patients du groupe traité par radiothérapie (26,5 % vs 10,4 %). Selon les données présentées par des chercheurs suisses, des résultats similaires ont été obtenus en pratique oncologique « sur le terrain » (Neuro Oncol, vol. 12, n° 4, 2010, p. iv1-iv136, résumé EP-11). Par exemple, 21 % des 57 patients traités par radiochimiothérapie ont survécu pendant deux années, mais seulement 4 % des 47 témoins historiques recevant une radiothérapie (voir le graphique 1). De l’avis de ces chercheurs, le fait que les médecins traitants soient passés d’une démarche essentiellement palliative à une autre, plus musclée, pour lutter contre le glioblastome multiforme pourrait y être pour quelque chose.
L’efficacité des traitements utilisés actuellement en deuxième intention contre le glioblastome multiforme évolutif est limitée. Plusieurs facteurs y contribuent, d’une part la difficulté de mettre au point des agents capables de traverser la barrière hématoencéphalique et de triompher de l’hétérogénéité du glioblastome multiforme, et d’autre part, le microenvironnement complexe de la tumeur qui favorise la redondance et la résistance au traitement, a fait remarqué le Dr David Reardon, Sous-directeur délégué du Preston Robert Tisch Brain Tumor Center, de l’Université Duke qui est situé à Durham, en Caroline du Nord.
Les patients âgés aussi peuvent être traités
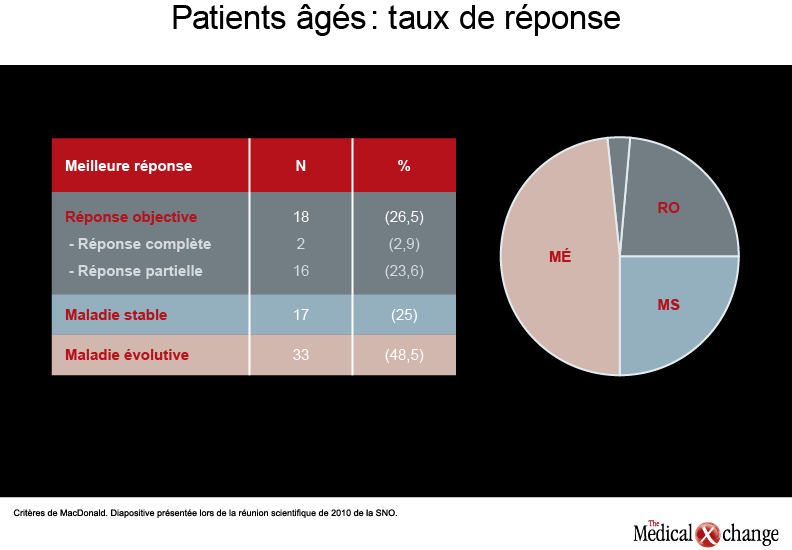
« Les cas de glioblastome multiforme chez les personnes âgées ont été beaucoup plus fréquents au cours des dix dernières années, mais on s’est souvent limité à des traitements de soutien en raison surtout de la piètre espérance de vie de ces patients et par crainte des effets toxiques », a affirmé le Dr Jaime Gállego Pérez de Larraya, neurologue à l’Hôpital La Pitié-Salpêtrière, à Paris. Divers rapports, dont certaines analyses rétrospectives mentionnées ici, ont établi que la radiothérapie avec ou sans TMZ peut être sûre et efficace chez les personnes âgées, notamment celles qui ont un indice fonctionnel raisonnable (Neuro Oncol, vol. 12, n° 4, 2010, p. iv1-iv136, résumés RT-21 et NO-25). Cela dit les données sur les patients âgés ayant un mauvais indice fonctionnel sont rares. Le Dr Gállego Pérez de Larraya et ses collègues ont évalué l’efficacité et l’innocuité du TMZ utilisé seul (de 150 à 200 mg/m2 pendant 5 jours toutes les 4 semaines, et ce, durant 12 cycles au maximum ou jusqu’à évolution de la maladie) chez 70 patients âgés de 70 ans au moins (Neuro Oncol, vol. 12, n° 4, 2010, p. iv1-iv136, résumé OT-28). La majorité d’entre eux (91,5 %) avait subi une biopsie. Les deux tiers des patients avaient un indice fonctionnel de 60, tandis que 20 %, 16 % et 1 % des patients avaient un indice fonctionnel de 50, 40 et 30, respectivement. La survie sans progression de la maladie et la survie globale médianes se sont chiffrées à 16 et à 25 semaines. À 6 mois, la maladie n’avait pas évolué chez 30 % des patients et 44 % des patients étaient toujours en vie. Une réponse objective et une stabilisation de la maladie ont été observées chez un peu plus de la moitié des sujets (voir le tableau 1).
Comme ce fut le cas dans d’autres études, la présence du gène de la MGMT méthylé s’est traduite par une amélioration de l’issue de la maladie : les tumeurs dépourvues de ce type de gène ont été associées à un risque de décès environ deux fois plus élevé pendant le déroulement de l’essai. Un peu plus de la moitié des sujets ont connu une réponse objective ou une stabilisation de leur maladie (26,5 % et 25 %, respectivement), tandis que 48,5 % des sujets ont vu leur tumeur évoluer. « Il convient de noter que ces résultats se sont également accompagnés d’améliorations significatives de l’indice fonctionnel et des paramètres de la qualité de vie », a ajouté le Dr Gállego Pérez de Larraya.
La MGMT et l’intensité du traitement
C’est un fait largement accepté que la méthylation du promoteur du gène de réparation de l’ADN par la méthylguanine méthyltransférase (MGMT) est un facteur prédictif favorable en ce qui concerne la radiothérapie et l’administration de TMZ, puisqu’elle est le signe de l’expression réduite de la MGMT, une enzyme de réparation de l’ADN. Les sujets de la plupart des études portant sur le TMZ sont maintenant stratifiés en fonction de l’état de méthylation de la MGMT. « D’après les travaux réalisés par nos chercheurs de l’Institut neurologique de Montréal (INM) (Neuro Oncol, vol. 12, n° 4, 2010, p. iv1-iv136, résumé CB-44), la méthylation du promoteur de la MGMT n’est pas simplement une fonction binaire, c’est-à-dire positive ou négative, mais plutôt une variable continue, a expliqué le Dr Rolando Del Maestro, professeur de neurochirurgie et d’oncologie à l’université McGill et Directeur du Centre de recherche sur les tumeurs cérébrales de l’INM. Une façon plus précise d’évaluer l’expression et l’activité de la MGMT pourrait être d’exprimer la méthylation sous forme de pourcentage », a-t-il ajouté. En effet, ces chercheurs ont constaté chez les 40 patients ayant pris part à leur étude que la méthylation de la MGMT était différente dans les quatre régions tumorales analysées pour la moitié environ des tumeurs examinées. Ces chercheurs en sont venus à la conclusion qu’il pourrait être préférable de calculer le pourcentage de méthylation moyen total des tumeurs et d’utiliser la région de la tumeur dont le pourcentage de méthylation est le plus faible comme indice de la réponse possible de la tumeur aux agents alkylants [TMZ]. Le Dr Del Maestro a en outre fait remarquer que pour consolider les prédictions quant à la réponse au traitement, il pourrait se révéler nécessaire d’évaluer l’activité de la MGMT dans le noyau cellulaire afin de déterminer si la tumeur sera en mesure de composer avec l’assaut du TMZ et les dommages qu’il provoquera côté méthylation.
Plusieurs études ont servi à évaluer si l’exposition continue au TMZ au moyen de schémas posologiques à doses rapprochées ou métronomiques pourrait permettre de briser la résistance au traitement en supprimant l’activité de la MGMT, sans compter que ce type de traitement pourrait aussi exercer des effets antiangiogéniques. Au cours de l’essai RESCUE que Perry et ses collaborateurs ont effectué récemment, ces chercheurs ont découvert que l’exposition continue au TMZ au moyen de schémas posologiques à doses rapprochées (50 mg/m2 tous les jours pendant 28 jours) est efficace et bien tolérée chez les patients chez lesquels un traitement classique administré 5 jours sur 28 a échoué, la survie sans progression de la maladie à 6 mois s’étant chiffré, en moyenne, à 24 % environ et la survie à 1 an, à 27 % (J Clin Oncol, vol. 28, n° 12, 2010, p. 2051-2057).
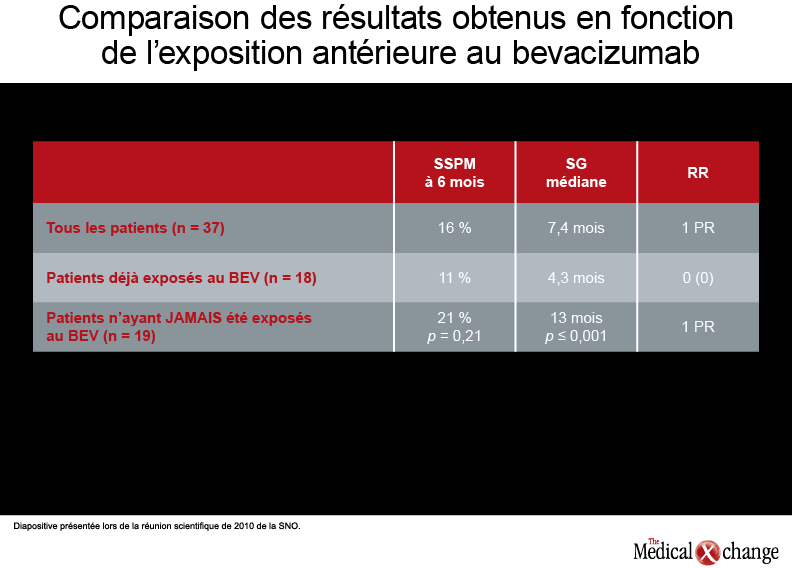
Selon les résultats périodiques issus d’une étude prospective de Phase II effectuée chez 47 patients atteints d’un glioblastome multiforme récidivant, le taux de survie sans progression de la maladie enregistré à 6 mois s’élevait à 23 % chez les sujets traités par le TMZ administré à raison de 75 à 100 mg/m2 21 jours sur 28, et ce, pendant 12 cycles au maximum (Neuro Oncol, vol. 12, n° 4, 2010, p. iv1-iv136, résumé OT-09). La survie sans progression de la maladie médiane s’est établie à 10 semaines et la survie globale, à 13 mois. Lors d’une autre étude de Phase II dont a parlé le Dr Mustafa Khasraw, du Memorial Sloan-Kettering Cancer Center de New York, 37 patients atteints d’un glioblastome multiforme récidivant ou évolutif ont reçu du TMZ à raison de 50 mg/m2/jour jusqu’à la progression de la maladie (Neuro Oncol, vol. 12, n° 4, 2010, p. iv1-iv136, résumé OT-14). La plupart d’entre eux avaient été exposés au bevacizumab et à d’autres agents, de même qu’à une association radiothérapie et TMZ. Le schéma posologique à doses rapprochées utilisé au cours de cette étude a été bien toléré, les effets indésirables les plus fréquents ayant été une lymphopénie et de la fatigue. Le taux de survie sans progression de la maladie à 6 mois, principal critère de jugement, était de 16 % et la survie globale médiane, de 7,4 mois. Fait intéressant à noter, les chercheurs de cette étude ont constaté que la survie globale était significativement meilleure et que la survie sans progression de la maladie avait eu tendance à s’améliorer chez les patients qui n’avaient jamais été traités par le bevacizumab (voir le tableau 2).
« Nous croyons qu’une fois que la maladie évolue, elle le fait rapidement chez les patients qui avaient déjà été exposés au bevacizumab, tandis que les patients qui n’y ont jamais été exposés peuvent espérer vivre plus longtemps grâce aux autres traitements, a expliqué le Dr Khasraw. Nos résultats mettent en lumière la nécessité de stratifier les patients en fonction de leur exposition antérieure au bevacizumab, ce qui permettra de recueillir des données qui pourront être utilisées dans les essais cliniques à venir », a-t-il ajouté.
Dans une autre présentation de l’INM, les chercheurs ont posé le postulat voulant qu’une chimiothérapie néoadjuvante reposant sur l’administration de TMZ administré à doses rapprochées avant la chirurgie pourrait être une méthode cytoréductive efficace dans les cas de glioblastome multiforme et d’autres gliomes. Lors de leur étude, 34 patients ont choisi de recevoir une dose quotidienne de 75 mg/m2 pendant 14 jours avant l’exérèse de leur tumeur, tandis que six autres patients ont préféré servir de sujets témoins. Aucune complication majeure telle qu’une infection ou une hémorragie survenue pendant ou après l’intervention n’a été observée chez les patients traités par le TMZ. Le seul effet toxique de grade 3 rapporté dans le groupe traité par le TMZ a été une lymphopénie (3 %) (Neuro Oncol, vol. 12, n° 4, 2010, p. iv1-iv136, résumé ST-12).
« Même si les résultats obtenus avec les schémas posologiques à doses rapprochées sont encourageants, a fait remarquer le Dr Del Maestro, les données recueillies dans le cadre de l’essai de Phase III RTOG-0525 (qui devraient être publiées l’année prochaine) ne seront pas de trop pour nous aider à préciser l’utilité de cette stratégie. Il faut que la méthylation atteigne l’ADN. Si nous utilisons des doses très faibles de TMZ, il nous est difficile de l’évaluer avec facilité. Devons-nous donner une surcharge ou des doses élevées de TMZ pour obtenir le degré de méthylation permettant d’endommager l’ADN? Si nous n’envoyons pas assez de TMZ dans la cellule, il se peut que l’ADN soit endommagé quand même, mais il sera réparé très rapidement. »
L’angiogenèse dans la mire
Le glioblastome se caractérise par une prolifération microvasculaire importante. Or les résultats provisoires issus des essais cliniques portant sur le bevacizumab, qui inhibe le facteur de croissance de l’endothélium vasculaire (VEGF), sont prometteurs. « Nous avons constaté une réponse rapide chez les patients aux prises avec une tumeur de stade III ou IV, ainsi qu’une amélioration significative de la survie sans progression de la maladie comparativement aux données de référence historiques », a indiqué le Dr Reardon. Alors qu’on craignait que l’inhibition du VEGF permette seulement de perturber la perméabilité vasculaire et d’empêcher la prise de contraste, certaines données sont venues démontrer que le bevacizumab exerce un effet antitumoral notable. « Les clichés obtenus en IRM ont effectivement montré une amélioration cadrant avec un effet antitumoral durable chez de 15 à 20 % des patients ayant participé à cette étude initiale. [En outre], un aspect important du traitement axé sur le VEGF, c’est que nous voyons une amélioration clinique chez beaucoup de patients… Certains sont même capables d’interrompre leur corticothérapie chronique [en raison de l’assèchement de l’oedème, ce qui] a un retentissement majeur sur leur qualité de vie », a ajouté le Dr Reardon. Selon le Dr Del Maestro, le bevacizumab permet aussi de prévenir les radiolésions, ce qui aide les patients à poursuivre leur traitement dans son intégralité.
L’aptitude du bevacizumab de prolonger la survie est encore à l’étude. D’après les résultats de l’essai RTOG 0625 rapportés par le Dr Gilbert, 117 adultes atteints de glioblastome multiforme récidivant antérieurement traités par radiothérapie et par le TMZ ont reçu du bevacizumab à 10 mg/kg en association avec soit de l’irinotécan à 200 mg/m2 toutes les 2 semaines, soit des doses rapprochées de TMZ (de 75 à 100 mg/m2 pendant 21 jours sur 28) (Neuro Oncol, vol. 12, n° 4, 2010, p. iv1-iv136, résumé NO-14). Selon le Dr Gilbert, les résultats obtenus portent à croire que ces deux schémas thérapeutiques peuvent être employés de façon sûre chez les patients dont le glioblastome multiforme évolue après qu’ils aient reçu les soins types. La survie sans progression de la maladie à 6 mois et la survie globale étaient similaires dans les deux groupes de sujets (voir le tableau 3). Le Dr Gilbert a toutefois tenu à préciser que bien qu’une tendance vers une meilleure survie se soit dessinée chez les patients recevant le traitement à base de TMZ, il ne s’agissait pas là du principal critère de jugement de l’étude et cette amélioration pourrait s’expliquer par l’inégalité de la répartition aléatoire des sujets.
On est actuellement à étudier l’emploi du bevacizumab allié aux traitements types utilisés en première intention dans le cadre de l’essai de Phase III RTOG 0825. Les résultats d’un essai de Phase II qui ont été présentés par la Dre Annick Desjardins, du Centre médical universitaire Duke, de Durham, en Caroline du Sud (Neuro Oncol, vol. 12, n° 4, 2010, p. iv1-iv136, résumé OT34) portent à croire que, dans les cas de glioblastome multiforme nouvellement diagnostiqué, l’ajout de bevacizumab (à raison de 10 mg/kg toutes les 2 semaines, en commençant au moins 28 jours avant l’intervention chirurgicale) à un traitement alliant le TMZ à la radiothérapie est bien toléré et permet de prolonger la survie (voir le tableau 4).
De l’avis du Dr Reardon, dans un tel contexte, les données dont nous disposons actuellement laissent entrevoir un effet toxique similaire à celui observé dans les cas de glioblastome multiforme récidivant, « quoique dans le cas des patients qui viennent de subir une craniotomie… vous devez suivre très attentivement la cicatrisation de la plaie avant d’administrer du bevacizumab pour réduire au minimum le risque de déhiscence de la plaie ou de complications. »
Les raisons d’espérer
« À l’avenir, les chercheurs cliniciens et les neurooncologues devront idéalement tenir compte des variables pronostiques, qui laissent entrevoir comment le patient s’en sortira, et des facteurs de prédiction qui les renseigneront sur les probabilités qu’un patient réagisse favorablement à un traitement en particulier ou qu’il en subisse les effets toxiques, a affirmé le Dr Gilbert. Nous devons définir quelles sont les populations de patients… qui réagiront le mieux avec le moins d’effets toxiques possible… Espérons qu’un jour nous serons capables de mieux prédire la tolérance des patients au traitement envisagé d’après leurs propres caractéristiques génomiques. » « Au stade préclinique, il faut mettre tous les efforts nécessaires pour déterminer laquelle parmi le large éventail de nouvelles cibles thérapeutiques convient le mieux, que ce soit pour tous les patients ou pour ceux qui ont des caractéristiques personnelles ou tumorales particulières », a déclaré le Dr Patrick Wen, Professeur de neurologie à l’École de médecine de Harvard et Directeur du Service de neurooncologie à l’Institut de cancérologie Dana Farber, à Boston, au Massachusetts. Il a ajouté que les chercheurs doivent explorer de nouvelles avenues pour évaluer le glioblastome multiforme et son traitement, compte tenu des limites que l’on reconnaît aux critères de McDonald dans l’évaluation des lésions ne prenant pas le contraste et des pseudoévolutions et pseudoréponse. Dans le cadre de leurs essais cliniques, les chercheurs devront aussi se pencher sur la qualité de vie et non plus uniquement sur la survie des patients.