Hematologie
59es réunion et exposition annuelles de l’American Society of Hematology (ASH)
La myélofibrose : les gains réalisés en matière de survie et de qualité de vie en intervenant tôt
Atlanta – Les données définitives des essais cliniques sur l’inhibition de la JAK appliquée à la myélofibrose ont transformé l’algorithme de traitement de cette affection. Selon une analyse effectuée par un expert et de nombreuses nouvelles données présentées lors de la réunion annuelle de 2017 de l’ASH, il faut envisager de recourir à un inhibiteur de la JAK comme traitement de première intention dès l’apparition des symptômes. Les autres agents habituellement utilisés pour maîtriser ces derniers, tels que l’hydroxyurée, ne peuvent être jugés équivalents, puisqu’ils sont moins efficaces et qu’ils ne s’attaquent pas au mécanisme sous-jacent de la maladie.
Le système de transduction du signal JAK-STAT, moteur de la myélofibrose
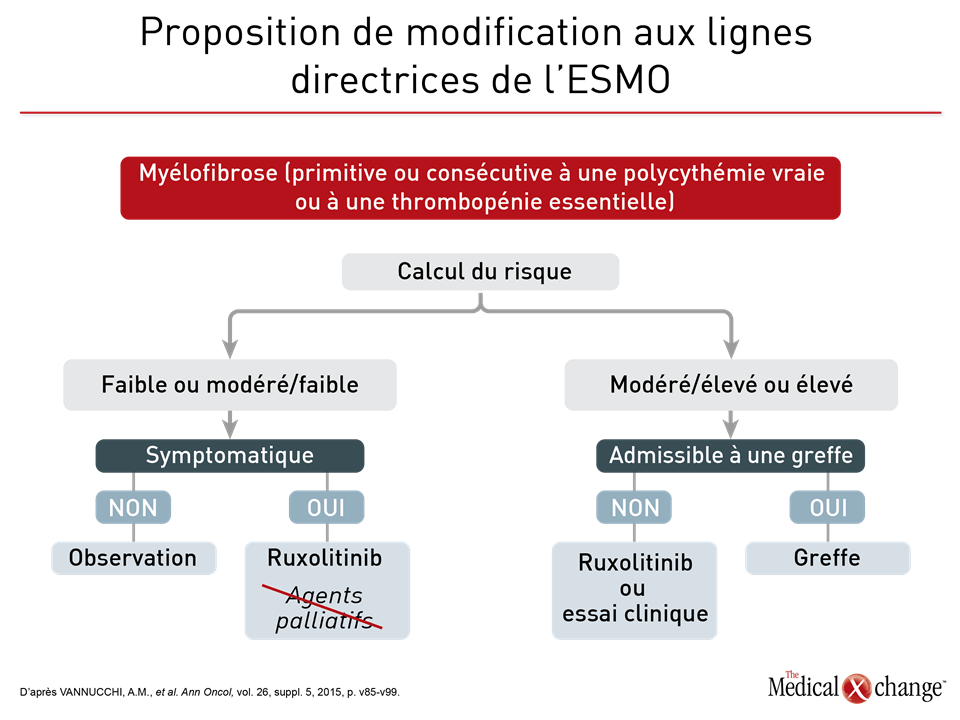
La myélofibrose, qu’elle soit consécutive à une expansion clonale de lignées myéloïdes ou à une évolution vers la malignité d’une polycythémie vraie ou d’une thrombopénie essentielle, s’explique en grande partie par un dérèglement de la transduction du signal JAK (Janus kinase) en réponse aux cytokines et aux facteurs de croissance. La mutation du gène V617F codant pour la JAK2 en est la cause sous-jacente la plus fréquente, mais elle n’est pas la seule. La mutation survenant dans l’exon 12 de la JAK2 et celle du gène CALR, le gène codant pour la calréticuline, sont également responsables d’anomalies du signal JAK-STAT qui sous-tend l’évolution pathologique et l’expression des symptômes. L’explication des changements apportés à la façon d’aborder la myélofibrose passe obligatoirement par la compréhension de ces notions. Si depuis 2015, de nombreuses lignes directrices, dont celles de la Société européenne de médecine interne cancérologique (ESMO; VANNUCCHI, A.M. et al. Ann Oncol, vol. 26, suppl. 5, 2015, p. v85-v99), préconisent l’emploi du ruxolitinib, un inhibiteur de la JAK1 et de la JAK2, en première intention chez les patients symptomatiques faiblement ou modérément exposés à la myélofibrose, il reste que les agents classiques étaient encore vus comme des solutions de rechange. Or ce n’est plus le cas, selon la Dre Claire Harrison, Professeure, Néoplasmes myéloprolifératifs, à la Guy’s and St. Thomas’ NHS Foundation Trust, de Londres, au R.-U. (Fig. 1) Prenant en compte les gains réalisés au chapitre du soulagement des symptômes et de l’amélioration de la survie en inhibant la JAK, la Dre Harrison a affirmé : « J’utilise rarement ces agents [palliatifs] dans ma pratique clinique ». Elle faisait alors référence à l’hydroxyurée et aux corticostéroïdes, mais aussi aux médicaments utilisés hors indication, notamment les interférons. Expert mondial de la myélofibrose et maître d’œuvre d’une séance de formation de l’ASH portant sur ce sujet, la Dre Harrison a insisté sur le fait que les avantages de l’inhibition de la JAK lorsqu’elle est indiquée, comprennent une meilleure qualité de vie et une prolongation de la survie.
L’inhibition de la JAK se traduit par une prolongation de la survie
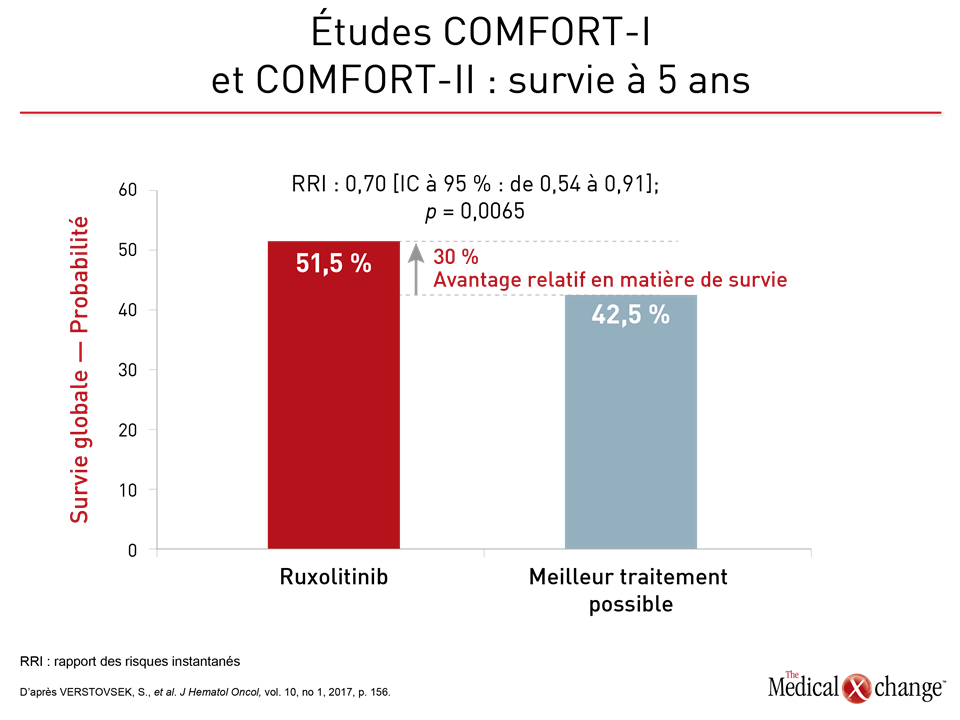
Selon la Dre Harrison, il n’y a pas lieu d’amorcer un traitement chez les patients peu exposés à la myélofibrose tant qu’ils ne présentent aucun symptôme. Cela dit, les données issues des études de phase III COMFORT-I et COMFORT-II sur l’inhibition de la JAK sont très parlantes. Les premiers articles publiés sur ces études faisaient état d’atténuations importantes des symptômes comparativement au meilleur traitement possible (MTP). Par la suite, les chercheurs de ces deux études ont établi un parallèle entre le ruxolitinib et une prolongation de la survie, et ce même en tenant compte du nombre élevé de patients qui étaient passés du MTP au ruxolitinib au terme de ces études. Or une analyse des données groupées de ces études citée par la Dre Harrison aurait révélé que le recours au ruxolitinib d’emblée avait été relié à une baisse de 30 % des décès.
« La monographie du ruxolitinib fait bel et bien mention d’une prolongation de la survie, mais ce n’est pas la principale raison, du moins en ce qui me concerne, pour amorcer un traitement par cet agent. »
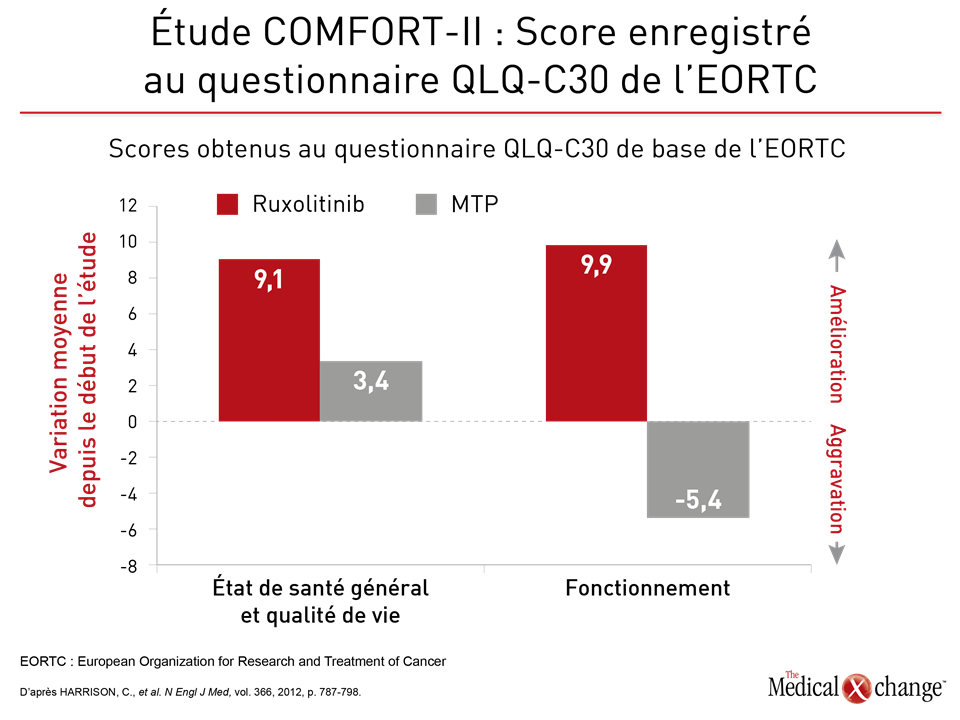
« La monographie du ruxolitinib fait bel et bien mention d’une prolongation de la survie, mais ce n’est pas la principale raison, du moins en ce qui me concerne, pour amorcer un traitement par cet agent », a déclaré la Dre Harrison. Ce serait plutôt l’allègement soutenu du fardeau des symptômes que cet agent procure qui justifierait son utilisation (Fig. 2). La prolongation de la survie est certes importante, mais la Dre Harrison a ajouté que la possibilité d’offrir aux patients une qualité de vie acceptable mérite d’être soulignée. Quelque 2233 patients de 26 pays ont été recrutés dans l’étude JUMP présentée au cours de la réunion de cette année de l’ASH, ce qui en fait l’une des plus vastes jamais réalisées sur la myélofibrose. À la 48e semaine de cette étude, la rate de 61,4 % des patients traités par le ruxolitinib avait perdu au moins la moitié (≥ 50 %) de sa longueur à la palpation. Cette atténuation de la splénomégalie était assortie d’une réduction des symptômes généraux caractéristiques (p. ex., fatigue, prurit, arthralgie et myalgie), qui s’est traduite par une amélioration des résultats obtenus pour la qualité de vie évaluée au moyen d’instruments validés.
Recrutement d’un large éventail de sujets dans l’étude JUMP
« Comme ce fut le cas pendant les études antérieures, l’anémie et la thrombopénie ont été les effets indésirables les plus fréquents, mais elles ont rarement commandé l’abandon du traitement par le ruxolitinib », a affirmé la Dre Haifa Kathrin Al-Ali, du Service d’hémato-oncologie, de l’Hôpital universitaire de Halle, en Allemagne. En fait, en plus de ressembler énormément à celles faites pendant les deux études COMFORT de phase III, les observations recueillies confirment les effets exercés par cet agent dans une population beaucoup plus vaste et pendant un laps de temps beaucoup plus long. Dans son analyse, la Dre Harrison, qui a cité les données de l’étude JUMP et des études de phase III publiées antérieurement (elle était la chercheuse principale de l’étude COMFORT-II), a ajouté que les effets indésirables du ruxolitinib sont traitables. Bien qu’elle doive être surveillée, la thrombopénie est habituellement asymptomatique. L’anémie quant à elle risque davantage de provoquer des symptômes, surtout pendant les 12 à 16 premières semaines, « mais ensuite, l’hémoglobinémie se met à remonter vers les valeurs préthérapeutiques ». La Dre Harrison a indiqué qu’un traitement de soutien à l’aide de danazol ou d’un agent stimulant l’érythropoïèse pourrait être utile pendant cette période. À l’apparition des premiers symptômes, il faut avoir recours au ruxolitinib d’emblée et le plus tôt possible, même chez les patients peu exposés à la myélofibrose, puisque cette maladie évolue rapidement et que la maîtrise des symptômes qui l’accompagnent ne doit pas être le seul facteur dont il faut s’occuper. En effet, près de 90 % des patients qui en sont atteints succombent aux complications qu’elle provoque. Une fois que les symptômes se sont manifestés, c’est l’inhibition rapide et soutenue de la voie JAK-STAT qui offre les meilleures chances de retarder la phase terminale de la maladie. « Si vous décidez de mettre fin au traitement par le ruxolitinib chez vos patients, gardez à l’esprit qu’en règle générale, le pronostic est alors extrêmement sombre », a ajouté la Dre Harrison.
Conclusion
Avant l’arrivée sur le marché de l’inhibiteur de la voie JAK-STAT, la survie médiane était estimée à six ans chez les patients atteints de myélofibrose symptomatique. Or il a été démontré qu’en ayant recours rapidement à un agent ciblant cette voie, il est non seulement possible d’offrir aux patients une survie plus longue qu’avec les traitements classiques, mais aussi de leur donner une bien meilleure qualité de vie en atténuant considérablement leurs symptômes.