Neurologie
8e réunion conjointe de l’ACTRIMS et de l’ECTRIMS de 2020
Protection prolongée contre l’invalidité et le dysfonctionnement cognitif dans des cas de SPPS évolutive
Réunion en ligne – De nouvelles données concernant un médicament homologué récemment pour la sclérose en plaques progressive secondaire (SPPS) corroborent l’obtention d’une protection prolongée contre l’invalidité et le dysfonctionnement cognitif. Elles établissent aussi un lien entre cet effet et une protection contre la perte de myéline, un acteur majeur dans l’évolution de la maladie. Ces observations ont été tirées de nouvelles analyses d’un essai déterminant et de son essai de prolongation. L’une d’elles a confirmé que la protection conférée contre l’invalidité et le déclin des fonctions cognitives est optimisée quand le traitement est entrepris rapidement. Un autre essai a révélé que ce sont les sujets aux prises avec une maladie évolutive qui ont été les mieux protégés contre le déficit cognitif.
De nouvelles données de l’essai EXPAND, le plus grand essai thérapeutique jamais réalisé sur la SPPS, et de son essai de prolongation confirment que le siponimod, un agent à prise orale homologué récemment pour le traitement de la SPPS dans de nombreux pays, dont le Canada, permet de protéger les patients plus longtemps contre les principales manifestations cliniques de l’évolution de la maladie. Le parallèle établi par ces données entre le siponimod et une remyélinisation permet de comprendre la protection importante observée contre l’aggravation de l’invalidité et le déclin des fonctions cognitives.
Pour une entrevue exclusive avec la Dre Sarah Morrow sur l’impact sur la pratique clinique, cliquez ici
L’évolution de la SPPS est ralentie
Avant l’essai de phase III EXPAND, aucun agent n’avait permis de ralentir systématiquement l’évolution de la maladie au sein d’un effectif représentatif de patients atteints de SPPS. Dans l’essai EXPAND, 1651 patients atteints de SPPS ont été répartis aléatoirement de façon à recevoir du siponimod, un modulateur des récepteurs de la sphingosine-1-phosphate (S1P), ou un placebo. Même si leur maladie était avancée (plus de 50 % des sujets recrutés avaient besoin d’une aide à la marche), les chercheurs ont vu le paramètre d’évaluation principal, soit l’aggravation de l’invalidité confirmée à 3 mois (AIC3m), baisser de plus de 20 % (p = 0,013) (Kappos, L. et al. Lancet 2018;391:1263-1273).
Plus tôt cette année, des données issues de l’essai de prolongation de longue durée de l’essai EXPAND mené en mode ouvert ont été présentées lors de la réunion en ligne de 2020 de l’Académie européenne de neurologie (EAN) (Fox, L., et al. EAN 2020, résumé EPR2128). Au début de cet essai, les témoins de l’essai contrôlé initial sont passés au siponimod. Après 45 mois de suivi en moyenne, la réduction du risque d’aggravation de l’invalidité confirmée à 6 mois (AIC6m) était de 22 % (p = 0,0026) chez les patients ayant reçu du siponimod en continu par rapport aux témoins. Les calculs faits du 25e au 50e percentile d’aggravation ont relié le siponimod en continu à un délai relatif moyen de 49,3 % pour l’invalidité confirmée à 6 mois (AIC6m).
Selon les données de l’essai EXPAND initial et de l’essai de prolongation de longue durée présentées lors de la réunion de 2020 de l’ACTRIMS et de l’ECTRIMS, ce sont les patients dont la maladie évoluait (≥ 1 poussée dans les deux années ayant précédé le recrutement ou présence d’au moins 1 lésion prenant le gadolinium en T1) qui ont été les mieux protégés contre l’aggravation de l’invalidité (Giovannoni, G., et al. ACTRIMS-ECTRIMS 2020, résumé P0238). Ce net avantage du siponimod chez les patients atteints de SPPS évolutive avait déjà été rapporté lors de l’essai déterminant, mais l’analyse des données à long terme recueillies sur l’AIC6m a révélé que les patients atteints de SPPS évolutive traités par le siponimod en continu avaient plus bénéficié de leur traitement que les témoins qui étaient passés à cet agent.
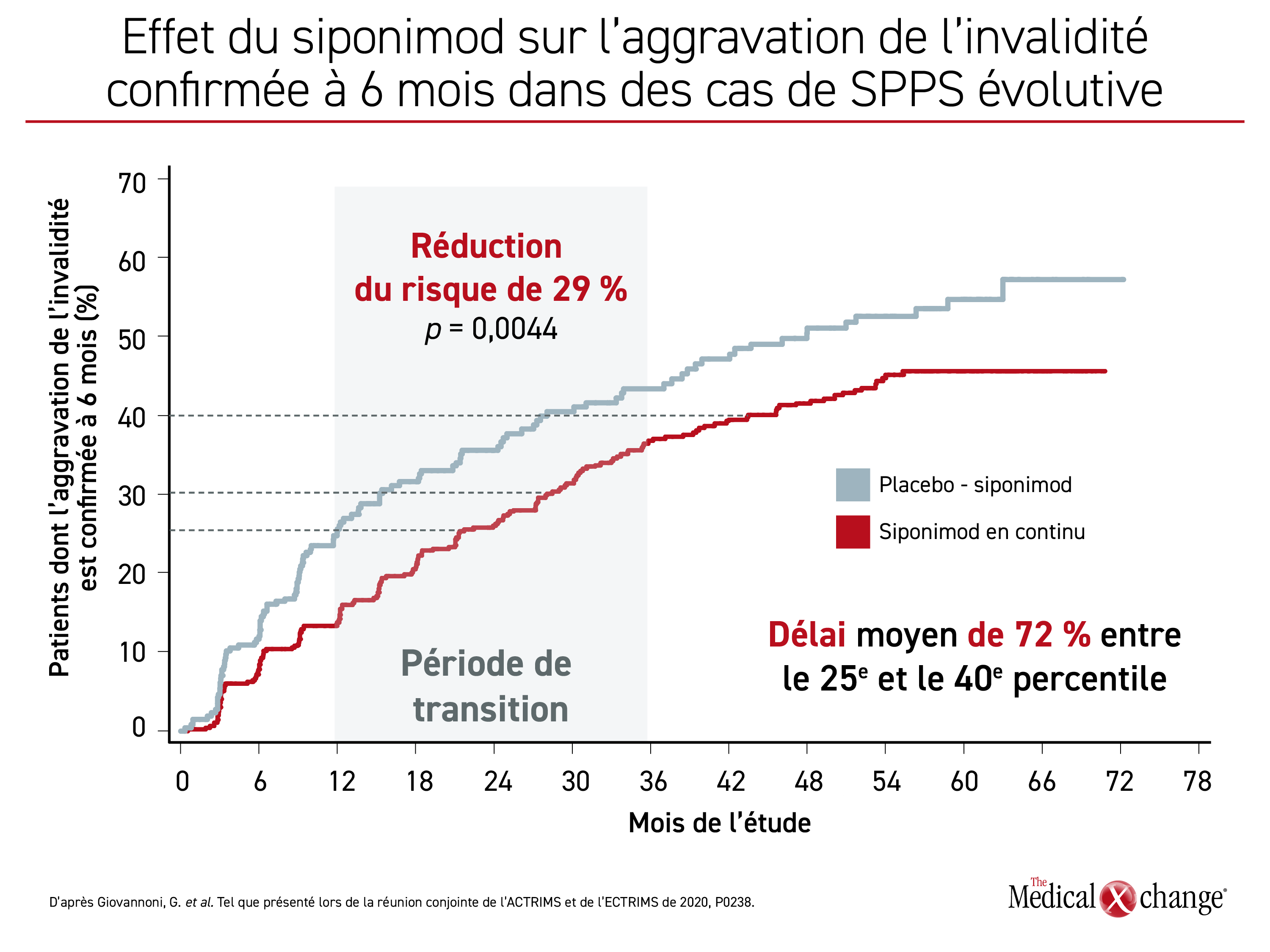
Comparativement à ces derniers, « les sujets atteints de SPPS évolutive ayant pris du siponimod en continu étaient exposés à un risque d’aggravation de l’invalidité confirmée à 6 mois de 29 % plus faible [p = 0,0044] », a affirmé le Dr Gavin Giovannoni, de la Chaire de neurologie, de l’Institut Blizard de Barts et de l’École de médecine de Londres, au R.-U. Chez les sujets du 25e au 40e percentile, l’AIC6m était retardée de 72 % en moyenne (Figure 1).
« Les sujets atteints de SPPS évolutive ayant pris du siponimod en continu étaient exposés à un risque d’aggravation de l’invalidité confirmée à 6 mois de 29 % plus faible [p = 0,0044]. »
Ont été admis à l’essai de prolongation 1224 des 1651 patients évaluables ayant participé jusqu’à la fin à l’essai EXPAND initial de 36 mois mené à l’insu tout comme 582 des 779 patients dont la maladie évoluait au début de l’essai initial. Dans l’analyse présentée par le Dr Giovannoni, le suivi médian (essais initial et de prolongation) était de 53,8 mois.
Dans le groupe dont la SPPS n’évoluait pas, la réduction du risque d’AIC6m pendant le suivi de l’essai de prolongation s’élevait à 12,5 % chez les patients traités par le siponimod en continu par rapport aux témoins passés à cet agent, ce qui correspond à un délai de 30 % du 25e au 40e percentile, a déclaré le Dr Giovannoni.
Selon lui, le risque relatif de détérioration des fonctions cognitives était à l’image du gain relatif et de l’importance d’un traitement par le siponimod amorcé tôt dans les cas de maladie évolutive. Cette analyse portait sur la variation du score obtenu au test SDMT (Symbol Digit Modalities Test), un outil rigoureusement validé servant à évaluer les fonctions cognitives et la vitesse de traitement de l’information (Benedict, R.H.B. et al. Mult Scler 2017;23:721-723). Une baisse minimale de 4 points à 6 mois confirmait la détérioration cognitive (DCC6m).
Jusqu’à présent, il ressort de la période de suivi de l’essai de prolongation de longue durée que « le risque de DCC6m a diminué de 33 % et que cette dernière a été retardée de 70 % chez les patients atteints de SPPS évolutive recevant du siponimod en continu comparativement aux témoins », a rapporté le Dr Giovannoni. Quant aux patients dont la SPPS n’évoluait pas, la réduction a été de 12,3 % et la DCC6m a été retardée de 45 % environ (48,5 vs 33,4 mois) dans le groupe du 40e percentile.
D’après lui, il y avait aussi un lien entre le fait d’amorcer tôt un traitement par le siponimod dans les cas de SPPS évolutive au lieu de le différer (témoins passés du placebo au siponimod) et un taux de poussées annuel (TPA) plus bas. L’ensemble des données des essais EXPAND initial et de prolongation de longue durée ont mis au jour un TPA de 0,07 chez les patients de ce sous-groupe traités par le siponimod en continu, soit une réduction de 39,7 % (p = 0,0023) par rapport à 0,11 chez les témoins.
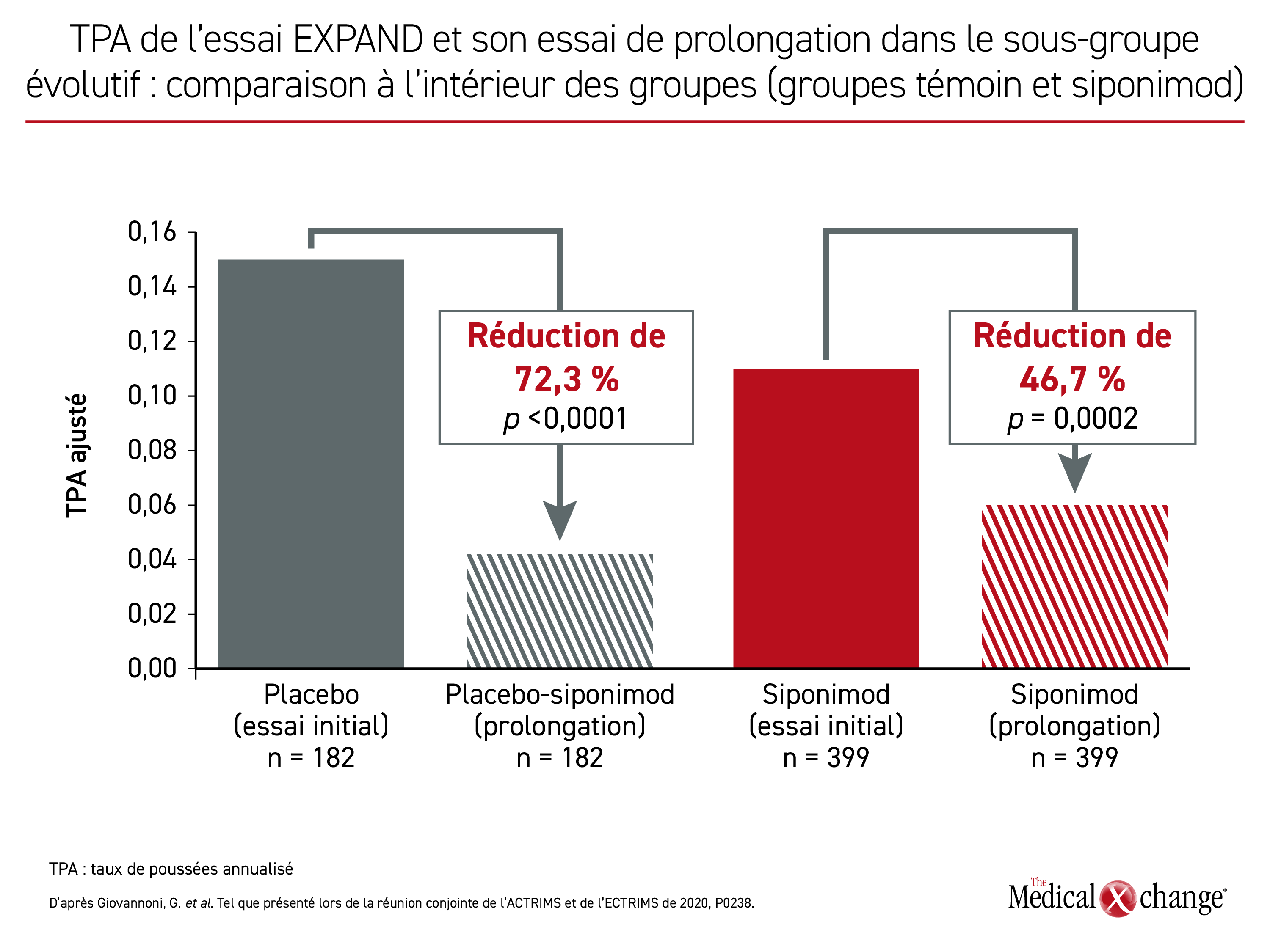
Avec le siponimod, le TPA est passé de 0,11 pendant l’essai EXPAND initial à 0,06 pendant celui de prolongation (baisse de 46,7 %; p = 0,0002). Durant ce dernier, des baisses significatives ont été observées dans les deux groupes de sujets comparativement aux valeurs calculées pendant l’essai initial (Figure 2).
Meilleure protection des fonctions cognitives dans les cas de SPPS évolutive
Une autre sous-étude a révélé que la supériorité de la préservation des fonctions cognitives obtenue avec le siponimod sur celle observée avec le placebo était encore plus marquée quand la maladie évoluait (Penner, I. K. et al. ACTRIMS-ECTRIMS 2020, résumé P0806).
Comme l’essai déterminant EXPAND avait permis de le constater, la détérioration des fonctions cognitives a touché moins de patients traités par le siponimod que de témoins si l’on se fie sur la baisse minimale de 4 points au test SDMT (24,6 % vs 31,2 %; p = 0,005). Les patients traités par le siponimod avaient plus de chances de voir leurs fonctions cognitives s’améliorer s’ils gagnaient au moins 4 points à ce test (34,8 % vs 27,1 %; p = 0,002).
La sous-étude publiée récemment a servi à comparer pendant les 24 mois de suivi de l’essai EXPAND la vitesse de traitement de l’information et les fonctions cognitives des patients aux prises avec une maladie évolutive ou non à partir de la variation du score obtenu au test SDMT.
Le siponimod a apporté une protection relative de près de 30 % contre la détérioration des fonctions cognitives (27,3 % vs 38,2 %; p = 0,002) dans le sous-groupe évolutif tout en y augmentant la proportion de sujets dont les fonctions cognitives s’étaient améliorées de 50 % (34,1 % vs 22,9 %; p = 0,001). En revanche, dans le sous-groupe non évolutif, l’avantage numérique du siponimod sur le placebo n’a atteint la signification statistique ni pour la détérioration (21,2 % vs 23,7 %) ni pour l’amélioration des fonctions cognitives (35,6 % vs 31,2 %).
« Ces données confirment que les effets relatifs aux variations d’importance clinique [dans les fonctions cognitives] étaient plus prononcés dans les cas de SPPS évolutive », a affirmé la Dre Iris Katharina Penner, du Département de neurologie, de l’université Heinrich Heine, à Dusseldorf, en Allemagne.
« Ces données confirment que les effets relatifs aux variations d’importance clinique [dans les fonctions cognitives] étaient plus prononcés dans les cas de SPPS évolutive. »
Selon elle, étant donné l’évolution lente de la maladie, « il faudra peut-être suivre pendant plus longtemps les patients atteints de SPPS qui commencent à prendre du siponimod à un moment où leur maladie n’évolue pas » pour déceler des changements importants chez eux.
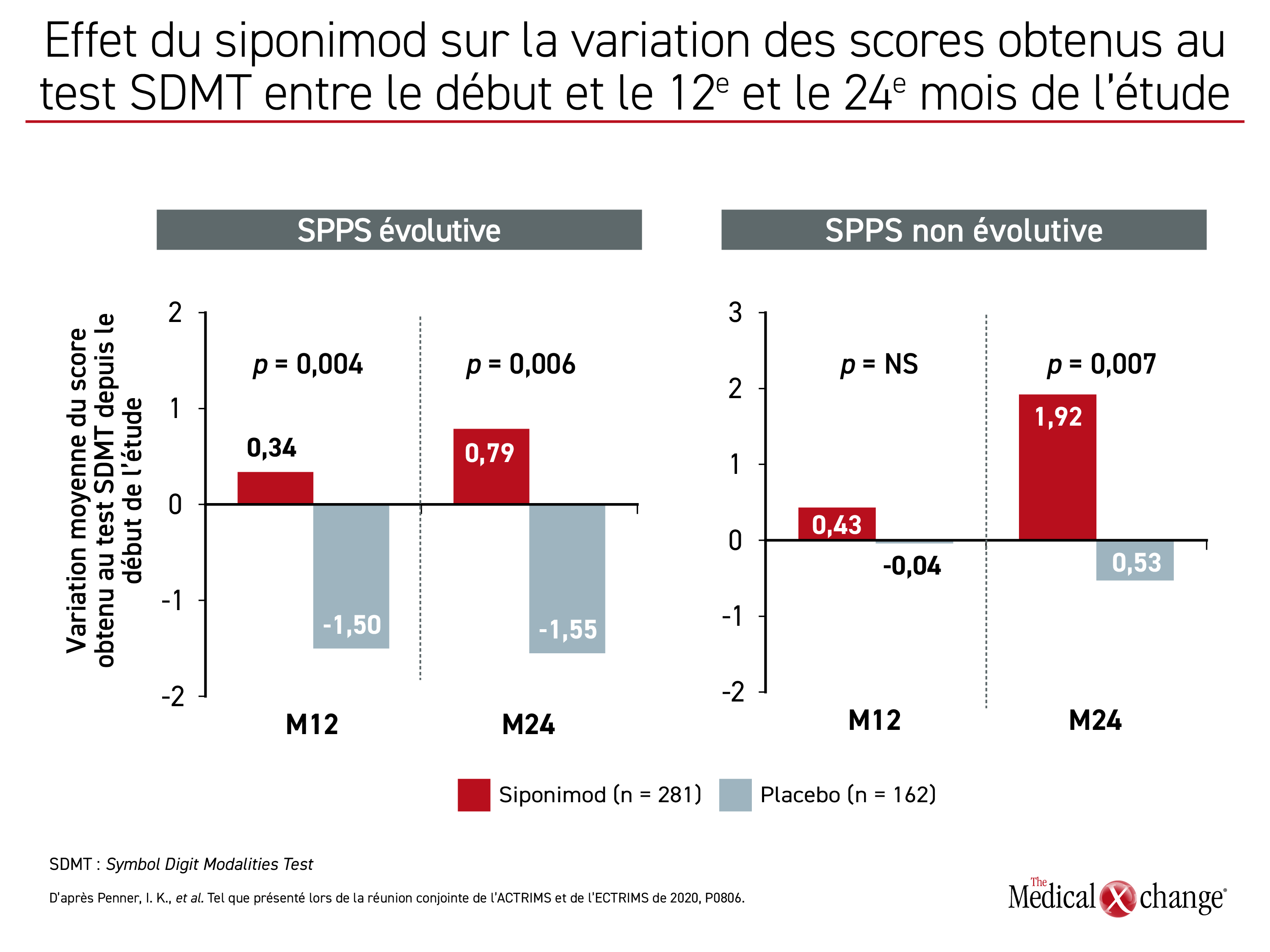
Les courbes des variations observées dans les fonctions cognitives par rapport aux valeurs de référence dans les cas de maladie évolutive et non évolutive ont permis de voir un lien entre le siponimod et des variations moyennes des résultats au test SDMT significativement meilleures sur 2 ans qu’avec le placebo, que la maladie évolue ou pas (Figure 3). Selon la Dre Penner, ces résultats cadraient avec ceux enregistrés dans l’ensemble de l’effectif à l’étude.
Les gains cliniques obtenus lors des essais EXPAND et de prolongation de longue durée pourraient s’expliquer par l’effet favorable du siponimod sur la densité et l’intégrité de la myéline selon les résultats d’une toute récente sous-analyse a posteriori de l’essai EXPAND (Arnold, D. L. et al. ACTRIMS-ECTRIMS 2020, résumé P0587) qui a servi à mesurer les changements subis par la myéline à l’aide du ratio de transfert d’aimantation (RTA), un marqueur de la démyélinisation et de la perte axonale.
Comparativement aux observations faites dans le tissu cérébral d’aspect normal (TCAN), la matière grise corticale (MGc) et la matière blanche d’aspect normal (MBAN) des témoins, les sujets affectés au siponimod ont connu une hausse de leur RTA par rapport à leurs valeurs de référence ou un ralentissement du déclin du RTA relatif, signes d’une remyélinisation ou d’une protection contre la perte de myéline. Ces écarts, quoique pas tous significatifs sur le plan statistique, étaient constants d’un sous-groupe à l’autre stratifié en fonction de l’âge, de l’ancienneté de la maladie, du score de référence à l’échelle EDSS (Expanded Disability Status Scale) et de l’évolution ou non de la SPPS.
Autre bienfait : la réparation de la myéline
Dans l’ensemble, « ces données étayent un bienfait du siponimod sur les mécanismes centraux de réparation de la myéline et corroborent les résultats des essais précliniques qui avaient aussi révélé un effet favorable sur la remyélinisation », a déclaré le Dr Douglas L. Arnold, professeur à l’Institut et hôpital neurologiques de Montréal, au Québec.
« Ces données étayent un bienfait du siponimod sur les mécanismes centraux de réparation de la myéline et corroborent les résultats des essais précliniques qui avaient aussi révélé un effet favorable sur la remyélinisation. »
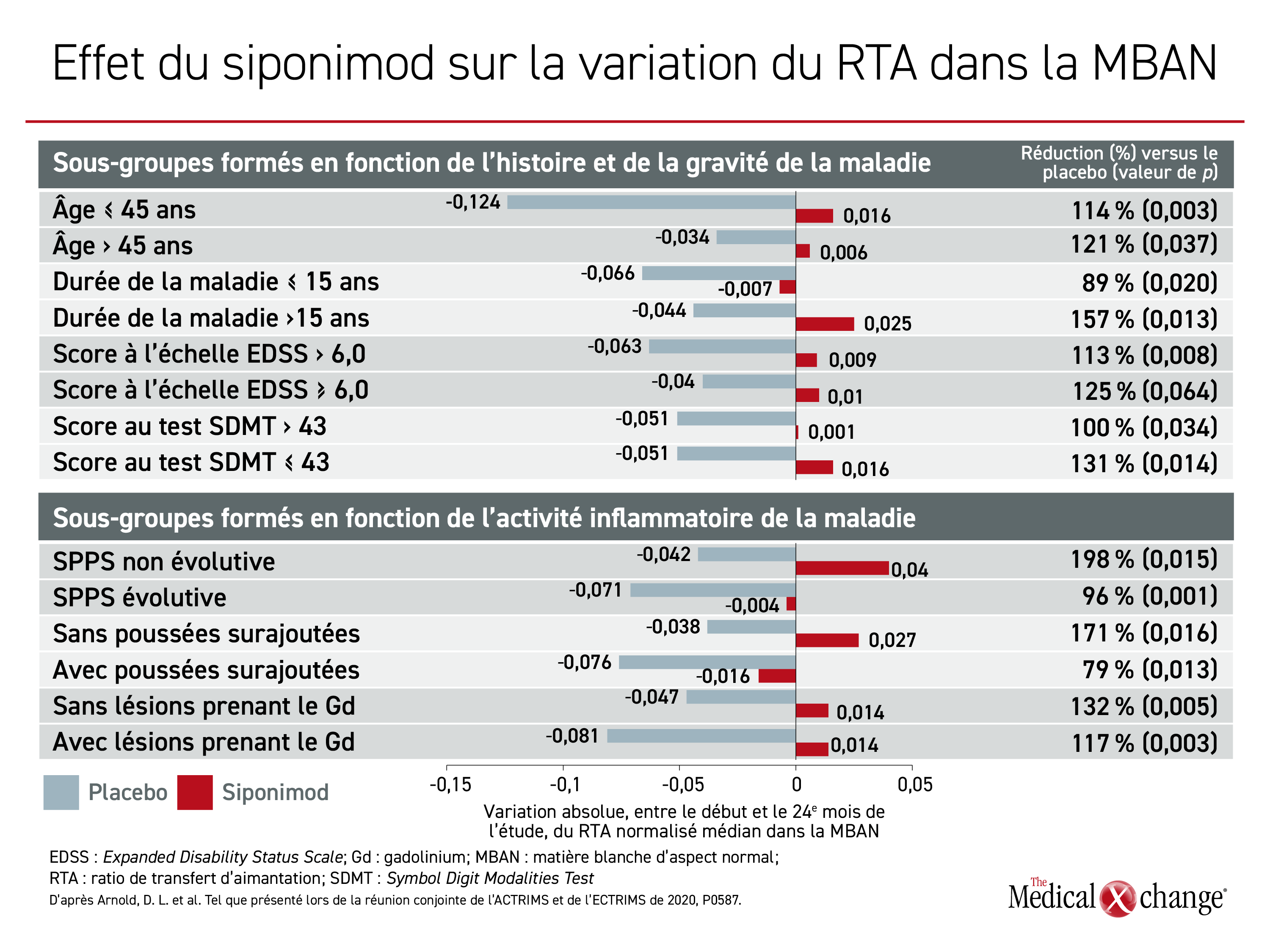
En 24 mois, le siponimod a ralenti la diminution du RTA de 70 à 170 % dans le TCAN, de 44 à 188 % dans la MGc et de 79 à 198 % dans la MBAN dans ces sous-groupes par rapport au placebo. Dans les divers sous-groupes, l’effet le plus constant a été observé dans la MBAN, où la plupart des écarts entre le siponimod et le placebo calculés à 2 ans ont atteint la signification statistique. Il n’y a eu aucune hausse du RTA dans le TCAN, mais le siponimod a bel et bien empêché la baisse importante de ce ratio observée chez les témoins.
Ces écarts n’ont atteint la signification statistique que dans certains sous-groupes pour ce qui est du TCAN et dans une moindre mesure pour la MGc, bien que cet effet ait été constant. Tant pour le TCAN que la MGc, l’avantage relatif du siponimod s’est révélé significatif chez les patients aux prises avec une SPPS évolutive. Quant à la MBAN, où l’effet du siponimod sur le RTA a été le plus marqué, tous les écarts, sauf un, ont atteint la signification statistique et ont été à l’avantage du siponimod (Figure 4).
La préservation de la myéline explique les bienfaits cliniques du siponimod observés pendant l’essai EXPAND et celui de prolongation en mode ouvert.
Au final, les données groupées de l’essai EXPAND initial et de l’essai de prolongation confirment l’effet favorable durable du siponimod sur la SPPS.
Dr Giovannoni : « Ces données nous ont appris que les effets du siponimod sur l’invalidité, la vitesse de traitement de l’information et l’issue des poussées dans les cas de SPPS évolutive se maintiennent pendant une période allant jusqu’à 5 ans ».
Ces effets positifs étaient assortis d’une tolérabilité et d’une innocuité acceptables. Dans l’essai déterminant EXPAND, le taux d’effets indésirables graves chez les patients affectés au siponimod était à peine plus élevé que chez les témoins (18 % vs 15 %), et les symptômes des effets indésirables les plus répandus, comme une hausse des enzymes hépatiques, l’hypertension et la bradycardie, étaient supportables.
Selon le Dr Giovannoni, le bilan d’innocuité du siponimod au cours de l’essai de prolongation de longue durée « était calqué sur celui dressé pendant l’essai initial ». Il a ajouté : « Les données sur son innocuité tirées du suivi de longue durée soulignent l’avantage d’amorcer le traitement tôt et confirment l’intérêt du siponimod pour le traitement des formes évolutives de SPPS ».
Conclusion
Le siponimod a été homologué pour le traitement de la SPPS à la lumière des résultats de l’essai de phase III déterminant ayant révélé qu’il ralentit significativement l’aggravation de l’invalidité. De nouvelles données issues de la sous-étude EXPAND portent à croire que ses effets positifs viennent de la préservation de la myéline comme en fait foi le RTA. Ces données cadrent bien avec le plus grand avantage relatif offert par cet agent dans les cas de maladie évolutive et avec celui d’amorcer le traitement par le siponimod au tout début de la SPPS.