Neurologie
8e réunion conjointe de l’ACTRIMS et de l’ECTRIMS de 2020
Un agent ciblé se montre supérieur à un immunomodulateur dans le traitement de première ligne de la SP cyclique
Congrès en ligne – De nouvelles analyses de deux essais de phase III confirment la supériorité d’un agent ciblé sur un immunomodulateur classique contre la sclérose en plaques (SP) cyclique. Selon une nouvelle analyse de sous-groupe réalisée à partir des données des deux essais, un anticorps monoclonal auto-injectable ciblant les lymphocytes B a été nettement plus efficace et aussi sûr que l’immunomodulateur auquel il était comparé dans le traitement de patients atteints de SP cyclique jamais traitée auparavant, ce qui pourrait bien transformer le paradigme thérapeutique pour le traitement de première ligne de cette maladie.
Les médecins prescrivent de plus en plus des traitements de fond très efficaces dès les débuts d’une SP cyclique fortement évolutive. Or de nouvelles données indiquent que cette stratégie peut être appliquée en première ligne. Selon une analyse des essais multinationaux ASCLEPIOS I et II publiés dernièrement, l’ofatumumab, un anticorps monoclonal ciblé, l’a nettement emportésur le tériflunomide, un immunomodulateur, pour d’importants paramètres d’évaluation de l’efficacité dans le sous-groupe de sujets jamais traités auparavant, les gains réalisés étant calqués sur ceux obtenus pour l’effectif entier.
Pour une entrevue exclusive avec la Dre Julie Prévost sur l’impact sur la pratique clinique, cliquez ici
« L’ofatumumab a été plus efficace que le tériflunomide chez les sujets dont la SP avait été diagnostiquée depuis peu et n’avait jamais été traitée, d’où de faibles taux absolus de poussées, une très faible activité lésionnelle à l’IRM, une aggravation de l’invalidité retardée et un bilan d’innocuité favorable », a rapporté le Dr Stephen L. Hauser, Directeur de l’Institut des Weill des Neurosciences, de l’Université de Californie, à San Francisco, pendant sa présentation des analyses des essais ASCLEPIOS lors de la réunion en ligne de l’ACTRIMS et de l’ECTRIMS (résumé P0192).
Publiés ensemble en août (Hauser, S. L. et al. N Engl J Med 2020;383:546-557) et menés selon une méthodologie identique, les essais ASCLEPIOS I et II ont servi à comparer l’ofatumumab, un anticorps monoclonal anti-CD20 que les patients devaient s’injecter toutes les quatre semaines, au tériflunomide, qui semble-t-il inhibe la SP grâce à son effet anti-inflammatoire. Dans ces deux essais, l’efficacité de l’ofatumumab l’a nettement emporté sur celle du tériflunomide, et ce à plusieurs niveaux. Une nouvelle analyse diffusée récemment a révélé que cet avantage de l’ofatumumab était au moins aussi marqué dans le sous-groupe de patients dont la SP était diagnostiquée depuis peu et n’avait jamais été traitée.
« [L’agent ciblé] a été plus efficace chez les sujets dont la SP avait été diagnostiquée depuis peu et n’avait jamais été traitée, d’où de faibles taux absolus de poussées, une très faible activité lésionnelle à l’IRM et une aggravation de l’invalidité retardée. »
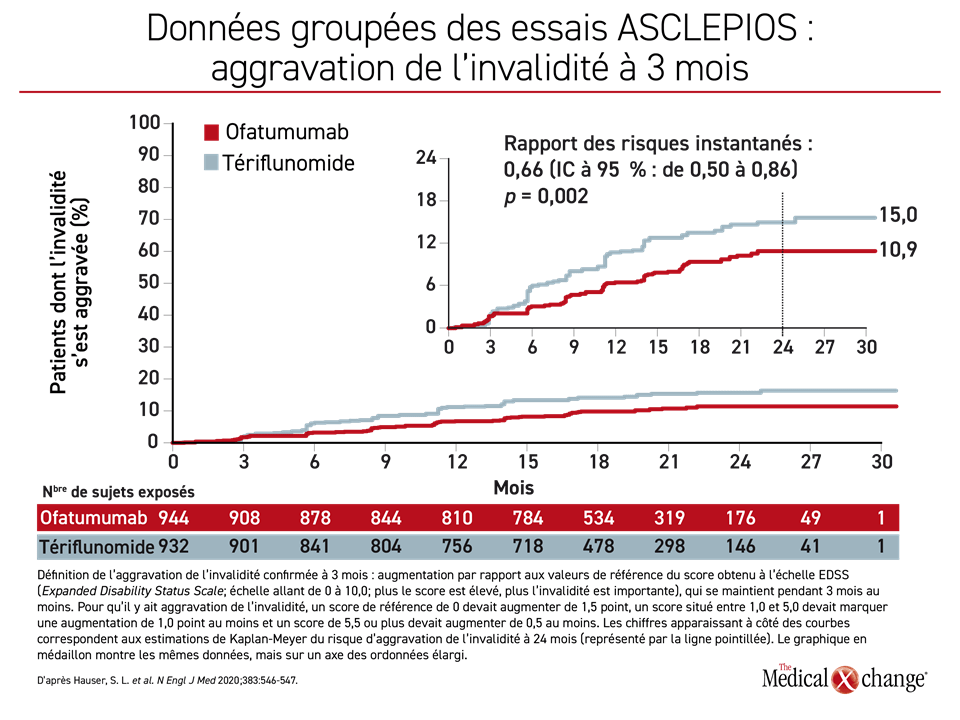
Il ressort des données des essais que, comparativement au tériflunomide, l’ofatumumab a permis de couper de moitié le taux de poussées annualisé (TPA), principal paramètre d’évaluation (0,11 vs 0,22; p < 0,001), lors de l’essai ASCLEPIOS I et de plus de la moitié pendant l’essai ASCLEPIOS II (0,10 vs 0,25; p < 0,001). Il a également été relié à une baisse de 34 % (p = 0,002) du rapport des risques instantanés (RRI) calculé pour l’aggravation de l’invalidité confirmée à trois mois (AIC3m) (Figure 1) et de 32 % de celui obtenu pour l’aggravation de l’invalidité confirmée à six mois (AIC6m) (RRI : 0,68; p = 0,01). L’ofatumumab a également eu nettement l’avantage sur le tériflunomide du côté de l’imagerie médicale, notamment pour les lésions prenant le gadolinium (Figure 1).
Pendant la période de suivi des essais ASCLEPIOS I et II, le volume cérébral a très peu changé dans les deux groupes de sujets, mais l’ofatumumab a fait preuve d’une protection significativement plus marquée pour ce qui est des nouvelles lésions prenant le gadolinium sur chaque cliché d’IRM en pondération T1 (Gd+T1) (p < 0,001) et du taux annuel de lésions de novo ou plus volumineuses sur les clichés d’IRM en pondération T2 (p < 0,001). La réduction relative des taux sériques de neurofilament à chaîne légère (NfL), un biomarqueur de l’atteinte axonale, a également été significative pendant ces deux essais (p = 0,01 et p < 0,001, respectivement). La FDA a homologué l’ofatumumab pour le traitement de la SP cyclique, y compris dans les cas de syndrome clinique isolé, à la lumière des résultats des essais ASCLEPIOS.
Dans le sous-groupe de 615 sujets jamais traités auparavant, soit près du tiers (32,7 %) des 1882 patients des essais ASCLEPIOS I et II répartis aléatoirement, les avantages de l’ofatumumab sur le tériflunomide ont été similaires, voire plus marqués. Dans l’ensemble de l’effectif de ces deux essais, un peu moins de 6 % des sujets étaient atteints de sclérose en plaques progressive secondaire (SPPS), les autres étant aux prises avec une SP récurrente-rémittente (SP-RR). Pour faire partie du sous-groupe de sujets jamais traités auparavant, les patients devaient avoir reçu un diagnostic de SP cyclique dans les 3 années ayant précédé la sélection des sujets et ne pas avoir suivi de traitement de fond.
Selon le Dr Hauser, qui a présenté les données recueillies dans ce sous-groupe lors de la réunion de 2020 de l’ACTRIMS et de l’ECTRIMS, les caractéristiques de référence des sujets jamais traités auparavant répartis aléatoirement dans les groupes de traitement étaient bien appariées. Ainsi, 4 mois en moyenne séparaient le diagnostic et leur admission à l’essai, un peu plus de la moitié d’entre eux ne présentaient aucune lésion Gd+T1, le nombre moyen de poussées au cours des 12 mois ayant précédé leur admission à l’essai était de 1,4 environ et leur score moyen de référence sur l’échelle EDSS (Expanded Disability Status Scale) s’élevait à 2,3.
Des différences relatives considérables pour le TPA dans le sous-groupe de sujets jamais traités auparavant
Le TPA relatif a baissé de 50,3 % (0,09 vs 0,18; p < 0,001) chez les sujets jamais traités auparavant qui ont été affectés à l’ofatumumab plutôt qu’au tériflunomide. La réduction relative de 38 % (p = 0,65) de l’AIC3m obtenue chez eux, bien que légèrement supérieure numériquement parlant à celle calculée à partir des données des deux essais ASCLEPIOS, a frôlé la signification statistique. La baisse de 46 % (p = 0,044) de l’AIC6m à l’avantage de l’ofatumumab a également excédé celle rapportée dans l’analyse globale publiée et cette différence a cette fois-ci bel et bien franchi le seuil de la signification statistique.
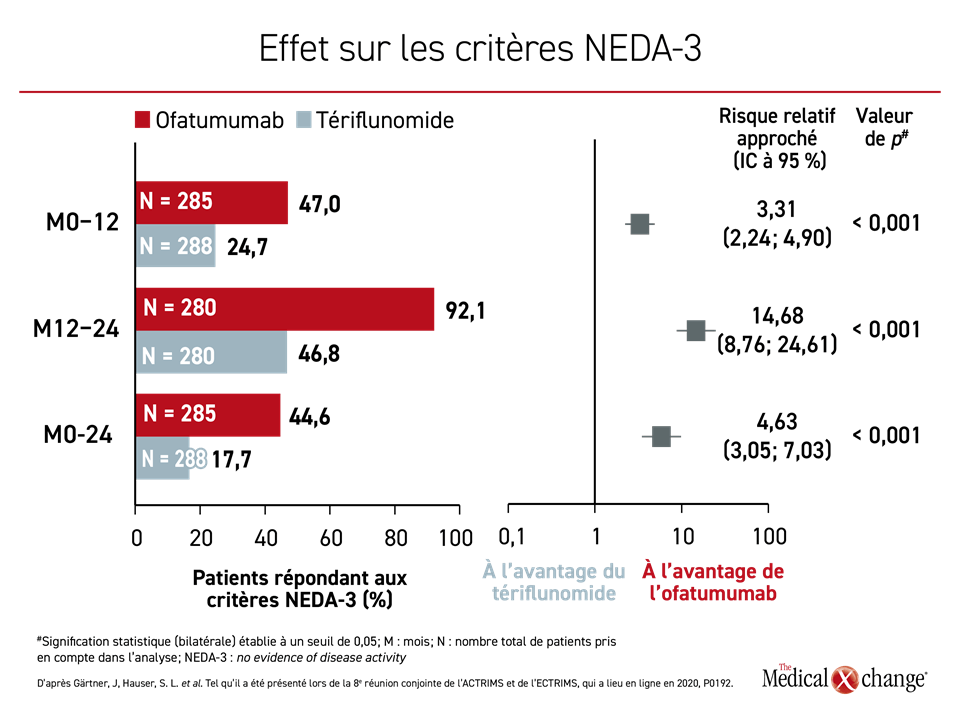
En outre, l’ofatumumab s’est aussi révélé plus efficace à tous les intervalles de mesure pour le respect des 3 critères témoignant de la non-évolution de la maladie (NEDA-3), soit l’absence totale de poussées évolutives, d’aggravation de l’invalidité et d’activité pathologique visible à l’IRM au cours d’une période donnée. Dans l’année qui a suivi la répartition aléatoire, les risques relatifs approchés calculés pour le respect des critères NEDA-3 avec l’ofatumumab correspondaient à plus du triple de ceux calculés pour le tériflunomide (p < 0,001) et ils étaient 14 fois plus élevés entre les 12e et 24e mois (p < 0,001). Or cet avantage était toujours significatif au 24e mois (Figure 2).
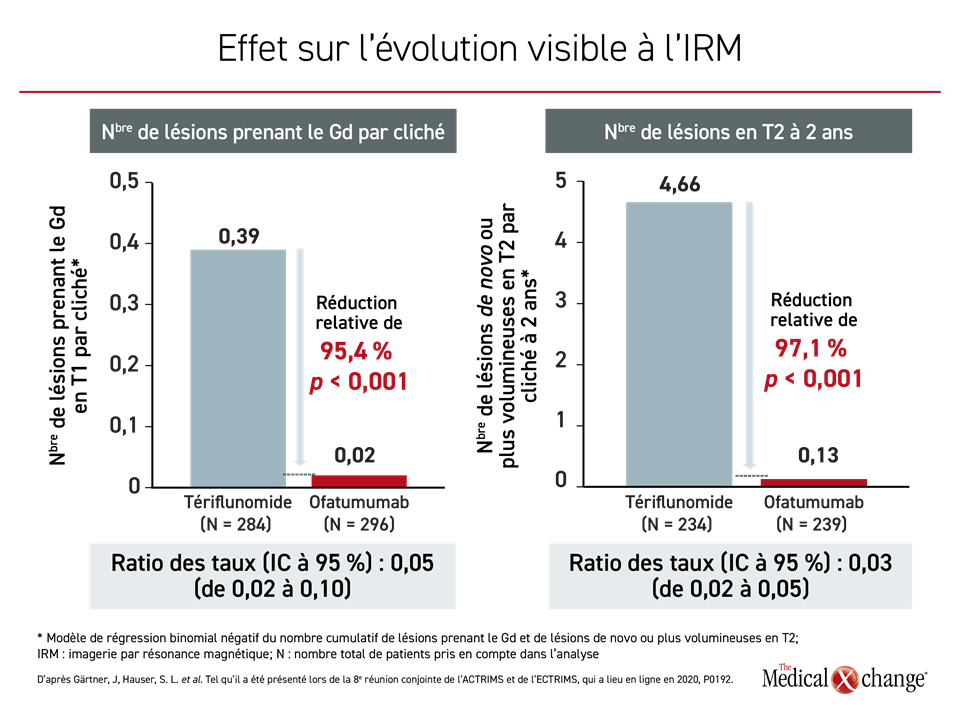
Si on la compare à celle obtenue dans tout l’effectif des essais ASCLEPIOS, la diminution de l’activité pathologique cérébrale visible à l’IRM dans les groupes traités par l’ofatumumab plutôt que par le tériflunomide était extrêmement significative chez les patients jamais traités auparavant aussi. Par exemple, la baisse relative des lésions visibles en T2 chaque année se chiffrait à 82 % (0,86 vs 4,78; p < 0,001) avec l’ofatumumab comparativement au tériflunomide. Chez les sujets traités par l’ofatumumab, les réductions observées au chapitre des lésions prenant le Gd sur chaque cliché et des lésions en T2 à 2 ans étaient encore plus marquées que chez ceux ayant reçu le tériflunomide en plus d’être extrêmement significatives sur le plan statistique (Figure 3).
D’après le Dr Hauser, l’efficacité supérieure de l’ofatumumab sur le tériflunomide constatée dans l’effectif des essais ASCLEPIOS au complet et dans le sous-groupe de sujets jamais traités auparavant n’a apparemment pas été obtenue au prix d’une moins bonne innocuité. Résumant les données recueillies sur ce paramètre lors de la réunion de l’ACTRIMS et de l’ECTRIMS, il a affirmé : « L’incidence des effets indésirables était similaire d’un groupe de traitement à l’autre et correspondait à celle observée dans l’effectif des essais ASCLEPIOS ».
« [Chez les patients jamais traités auparavant,] l’incidence des effets indésirables était similaire d’un groupe de traitement à l’autre et correspondait à celle observée dans l’effectif des essais ASCLEPIOS. »
Seules exceptions, les réactions au point d’injection survenues au début des essais, qui étaient plus fréquentes avec l’ofatumumab. Cela ne s’est toutefois pas reproduit au-delà de la première injection. En général, les effets indésirables graves ont été un peu plus fréquents avec l’ofatumumab qu’avec le tériflunomide dans l’ensemble de l’effectif des essais (9,1 % vs 7,9 %) et dans le sous-groupe de sujets jamais traités auparavant (7,0 % vs 5,3 %), mais aucune tendance soutenue vers un risque accru que l’un ou l’autre d’entre eux se manifeste ne s’est dessinée (p. ex., la rhinopharyngite, les infections des voies respiratoires supérieures, les céphalées ou la fatigue).
Le respect du traitement par l’ofatumumab dans le sous-groupe de sujets jamais traités auparavant a été comparable à celui de l’effectif des essais ASCLEPIOS dans son ensemble (98,8 % vs 98,3 %). Après la quatrième injection et jusqu’à la fin de l’essai, plus de 70 % des sujets se le sont injecté eux-mêmes.
Les agents ciblant les lymphocytes B ont déjà prouvé leur efficacité contre la SP. Par exemple, l’ocrélizumab, qui cible lui aussi les CD20 pour affaiblir l’activité des lymphocytes B, est un autre agent très actif indiqué contre la SP progressive primaire et les autres formes de SP cyclique, mais contrairement à lui, l’ofatumumab n’a pas besoin d’être injecté par voie intraveineuse (i.v.). En effet, l’ofatumumab « est le premier traitement de fond injectable très actif que les patients peuvent s’administrer eux-mêmes à la maison », a déclaré le Dr Hauser pendant sa présentation des données collectées chez les patients dont la maladie diagnostiquée depuis peu n’avait jamais été traitée auparavant. Dans l’ensemble, ces données appuient l’utilisation d’un traitement très actif dès le début de la SP cyclique afin d’en ralentir l’évolution.
Confirmation du NfL sérique au titre de biomarqueur à visée pronostique
Une autre analyse des données des essais ASCLEPIOS présentée lors de la réunion de 2020 de l’ACTRIMS et de l’ECTRIMS a porté tout spécialement sur le NfL sérique, un biomarqueur témoignant d’une atteinte neuro-axonale cadrant avec celle provoquée par la SP et d’autres maladies neurodégénératives. Si les résultats des essais ASCLEPIOS publiés dans le New England Journal of Medicine faisaient déjà état d’une baisse des concentrations sériques de NfL, la nouvelle analyse visait quant à elle à cerner l’intérêt pronostique des concentrations sériques élevées de NfL, surtout chez les sujets jamais traités auparavant.
Indépendamment du groupe de traitement, il ressort que les concentrations de référence de NfL sérique ont fait office de facteur pronostic pour la formation de lésions et la perte de volume cérébral tout au long des essais, selon l’auteur principal de cette analyse, le Dr Jens Kuhle, de la Clinique de neurologie et de la Polyclinique médicale de l’Hôpital universitaire de Bâle, en Suisse, qui en a présenté les résultats (réunion de 2020 de l’ACTRIMS et de l’ECTRIMS, résumé P0033).
D’après cette analyse, « les concentrations de NfL sérique peuvent nous renseigner prospectivement sur les risques d’une activité pathologique en cours et à venir, et d’aggravation subclinique de la SP cyclique », a-t-il précisé. Il a également ajouté que ce biomarqueur « pourrait compléter les évaluations cliniques et par imagerie » de l’évolution de la maladie et de l’effet positif du traitement.
Cette analyse a servi à comparer les patients dont les concentrations de référence de NfL sérique étaient faibles ou élevées. Les concentrations étaient considérées comme faibles si elles ne dépassaient pas la concentration médiane de 9,3 pg/mL, et élevées si elles y étaient supérieures. Les comparaisons ont porté sur l’ensemble de l’effectif à l’étude de même que chez les patients dont la maladie diagnostiquée depuis peu n’avait jamais été traitée auparavant.
Les chercheurs ont établi une corrélation entre une forte concentration de NfL sérique de référence et un plus grand risque d’activité pathologique visible aux examens par imagerie, et ce que les sujets aient été affectés à l’ofatumumab ou au tériflunomide et qu’ils aient déjà été traités ou non. Par exemple, le risque de lésions de novo ou plus volumineuses en T2 était environ le double de celui des patients dont la concentration de NfL sérique de référence était faible.
Il ressort de la comparaison des groupes de traitement que le risque de lésions de novo ou plus volumineuses en T2 pendant l’essai était plus grand chez ceux affectés au tériflunomide que chez ceux affectés à l’ofatumumab, que leurs concentrations de référence de NfL sériques aient été faibles ou élevées, ce qui cadre avec l’effet protecteur inférieur de l’immunomodulateur par rapport à celui de l’anticorps monoclonal. Cela dit, l’augmentation relative du risque quant aux lésions en T2 était plus prononcée chez les sujets affichant des concentrations de NfL sériques de référence élevées, peu importait l’agent auquel ils étaient affectés et que l’évaluation ait porté sur tous les patients ou sur le sous-groupe de sujets dont la SP était diagnostiquée depuis peu et n’avait jamais été traitée.
D’ailleurs, dans ce sous-groupe, la hausse relative du taux annuel de lésions de novo ou plus volumineuses en T2 s’est chiffrée à 98 % lorsque les concentrations de NfL sériques de référence étaient élevées plutôt que faibles (5,41 vs 2,73; p < 0,001) chez les sujets traités par le tériflunomide, alors qu’elle s’établissait à 103 % (0,78 vs 0,39; p < 0,001) chez ceux ayant reçu l’ofatumumab. La hausse du taux annuel de perte de volume cérébral était comparable que les concentrations de NfL sériques de référence aient été fortes ou faibles.
Quant aux paramètres d’évaluation cliniques, tels que le TPA et l’AIC3m, leur incidence était généralement plus marquée dans les cas où les concentrations de NfL sériques étaient élevées, quoique les différences enregistrées n’aient pas franchi le seuil de la signification statistique.
Protection contre l’évolution de la maladie indépendamment des concentrations de NfL sériques
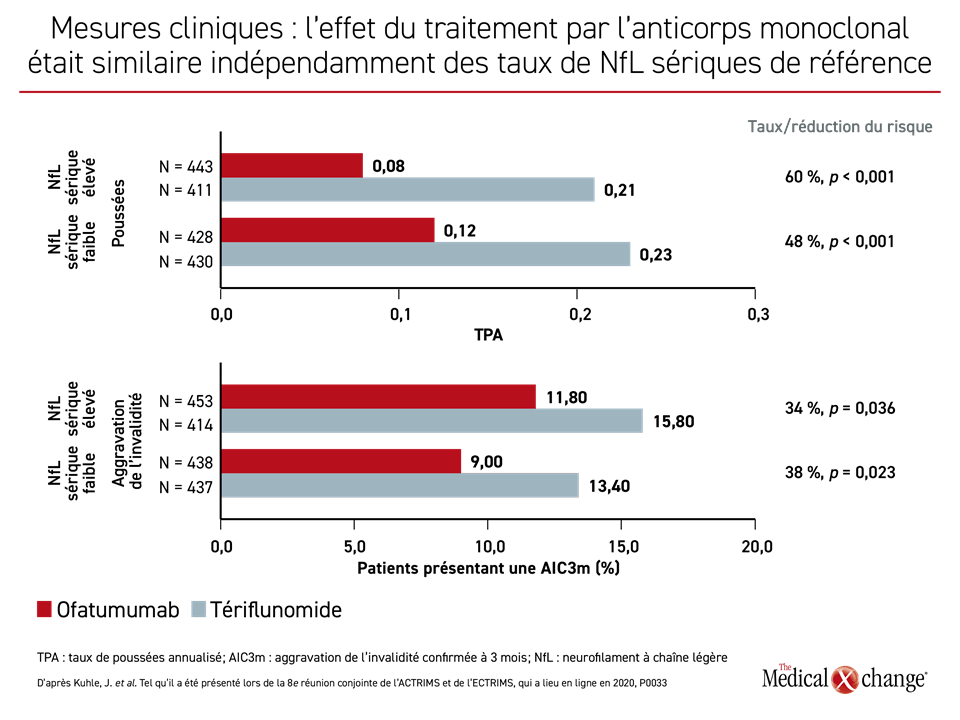
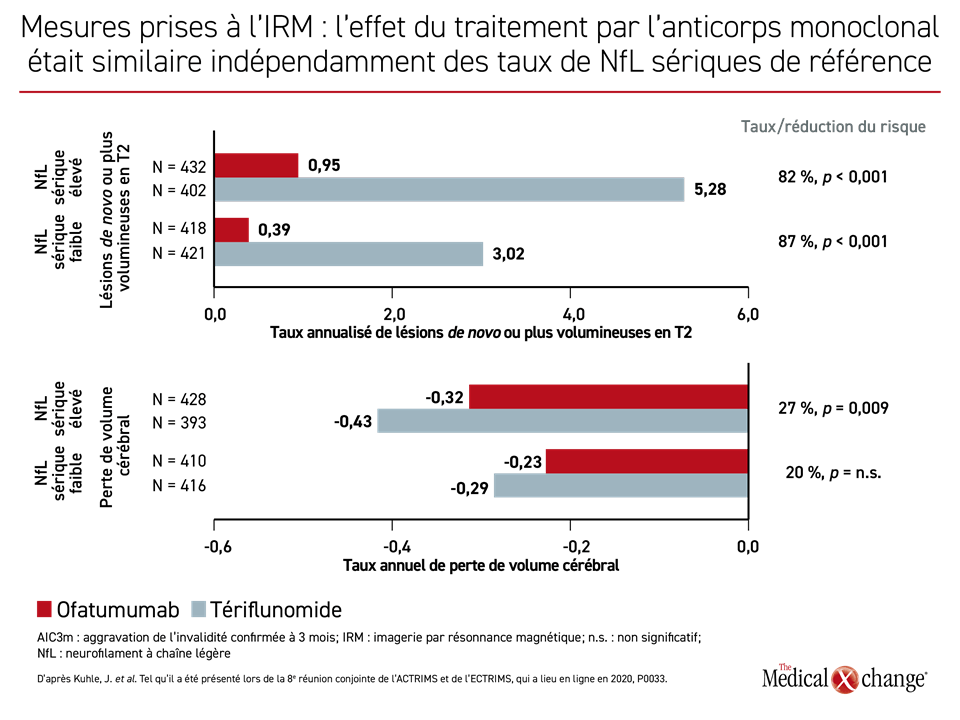
Peu importait les concentrations de NfL sériques de référence, l’ofatumumab a été relié à une réduction relative significative des taux (RT) pour de nombreuses mesures de l’évolution de la SP par rapport au tériflunomide. Après rapprochement en fonction des concentrations de NfL sériques de référence élevées ou faibles, les chercheurs se sont penchés sur les taux de poussées (RT : 60 %; p < 0,001 et 48 %; p < 0,001, respectivement), l’aggravation de l’invalidité (RT : 34 %; p = 0,036 et 38 %; p = 0,023, respectivement) et les lésions de novo ou plus volumineuses en T2 (RT : 82 %; p < 0,001 et 87 %; p < 0,001, respectivement) (Figure 4a) et (Figure 4b).
Une forte concentration de NfL sérique de référence s’est généralement révélée un facteur prévisionnel d’une activité pathologique plus intense sur les clichés d’imagerie qu’une faible concentration. En dépit de l’utilité du NfL sérique comme facteur prévisionnel d’une telle activité, l’ofatumumab a fait preuve d’une plus grande efficacité que le tériflunomide pour la plupart des paramètres. Il faudra réaliser de nouvelles études pour évaluer l’intérêt clinique de dosages sériels du NfL sérique dans la surveillance de la maladie et pour savoir si l’ajustement du traitement en fonction des concentrations obtenues permet d’en améliorer l’issue. Dans l’affirmative, le NfL sérique pourrait permettre de préciser le pronostic, l’état d’avancement de la maladie et la réponse au traitement.
Comparativement au tériflunomide, la protection conférée par l’ofatumumab chez les patients affichant des concentrations de NfL sériques élevées ou faibles cadrait généralement avec les observations rapportées pendant les essais ASCLEPIOS, que l’évaluation ait porté sur l’ensemble de l’effectif à l’étude ou sur les patients jamais traités auparavant.
Conclusion
Les données recueillies au cours des essais de phase III ASCLEPIOS I et II chez les patients atteints de SP cyclique jamais traitée auparavant indiquent qu’un anticorps monoclonal ciblé et très actif permet d’obtenir de meilleurs résultats qu’un immunomodulateur dans le traitement de première ligne de la SP cyclique. Le principe voulant que le recours rapide au traitement le plus efficace se traduise par des taux d’évolution plus bas, qu’ils soient mesurés d’après des paramètres cliniques ou d’après l’activité pathologique objectivée par IRM, pourrait bien transformer le paradigme thérapeutique. Lors des essais ASCLEPIOS, l’innocuité et la tolérabilité de l’ofatumumab, l’agent ciblé auto-injectable, se comparaient à celles du tériflunomide, l’immunomodulateur. Le respect du traitement par les patients affectés à l’ofatumumab a été supérieur à 98 %.