Rhumatologie
Réunion Convergence de l’American College of Rheumatology (ACR) de 2021
Des données prometteuses sur l’emploi des inhibiteurs de JAK contre la spondylarthrite ankylosante
Réunion en ligne – Les essais de phase III sur le traitement de la spondylarthrite ankylosante (SpA) par deux inhibiteurs de Janus kinases (JAK) à prise orale indiqués contre la polyarthrite rhumatoïde sont terminés. Aucun essai n’a encore été mené pour comparer ces agents aux inhibiteurs du facteur de nécrose tumorale (iTNF) ou à d’autres agents biologiques dans le traitement de la SpA, mais le taux élevé de réponse soutenue observé par rapport au placebo rivalise avec ceux des agents injectables les plus efficaces. L’homologation de ces inhibiteurs de JAK contre la SpA modérée ou grave serait imminente. Les données probantes montrant qu’ils sont dotés d’une efficacité au moins comparable à celles d’agents biologiques viennent entre autres d’un suivi de 2 ans.
Les toutes dernières données sur ces inhibiteurs de JAK présentées lors de la réunion Convergence de 2021 de l’ACR, qui sont notamment tirées d’un essai à répartition aléatoire ayant relié le tofacitinib à une baisse marquée de l’inflammation de la colonne vertébrale, s’inscrivent dans la continuité d’un essai de phase III publié plus tôt cette année, qui avait déjà fait état des bienfaits cliniques de cet agent (Deodhar A. et al., Ann Rheum Dis 2021;80:1004-1013). Quant à l’upadacitinib, les données issues d’une phase de prolongation de 2 ans de l’essai SELECT-AXIS 1 (van der Heijde, D. et al. Lancet 2019;394:2108-2117) ont confirmé les gains durables enregistrés pour les paramètres d’évaluation principal et secondaires, un faible taux de progression à la radiographie et un bilan d’innocuité à long terme similaire à celui dressé pendant la phase à l’insu de l’essai.
Pour une entrevue exclusive avec le Dr Walter P. Maksymowych couvrant l’impact sur la pratique clinique, cliquez ici
Étude des inhibiteurs de JAK contre plusieurs arthropathies
« Les inhibiteurs de JAK sont déjà homologués ou sont à l’étude pour plusieurs arthropathies inflammatoires d’origine immunitaire, dont la SpA », a déclaré le Dr Atul Deodhar, directeur médical des Cliniques de rhumatologie de la Division de l’arthrite et des maladies rhumatismales de l’Université des sciences de la santé de l’Oregon, à Portland. Le Dr Deodhar, qui a parlé de la phase de prolongation de l’étude sur l’emploi de l’upadacitinib contre la SpA, était aussi un des chercheurs principaux des études sur le tofacitinib. Il a affirmé que ces deux agents « ont nettement affaibli l’activité pathologique et amélioré le fonctionnement des patients et les résultats des examens par imagerie » au cours des essais multicentriques déterminants à l’appui des demandes d’homologation.
« Les inhibiteurs de JAK sont déjà homologués ou sont à l’étude pour plusieurs arthropathies inflammatoires d’origine immunitaire, dont la SpA. »
Lors de l’essai de phase III sur le tofacitinib dont le Dr Deodhar a parlé durant la réunion Convergence de l’ACR de l’an dernier et dont les résultats ont été publiés en 2021, 269 patients chez lesquels un traitement par des anti-inflammatoires non stéroïdiens (AINS) avait échoué et qui n’avaient jamais reçu d’agents biologiques ont été affectés aléatoirement au tofacitinib ou au placebo. À 16 semaines, trois fois plus de patients traités par cet inhibiteur de JAK que de témoins ont affiché une amélioration d’au moins 40 % de leur état selon les critères de l’Assessment of SpondyloArthritis international Society (ASAS40) (40,6 % vs 12,5 %; p < 0,0001).
Aucune perte de réponse en 104 semaines
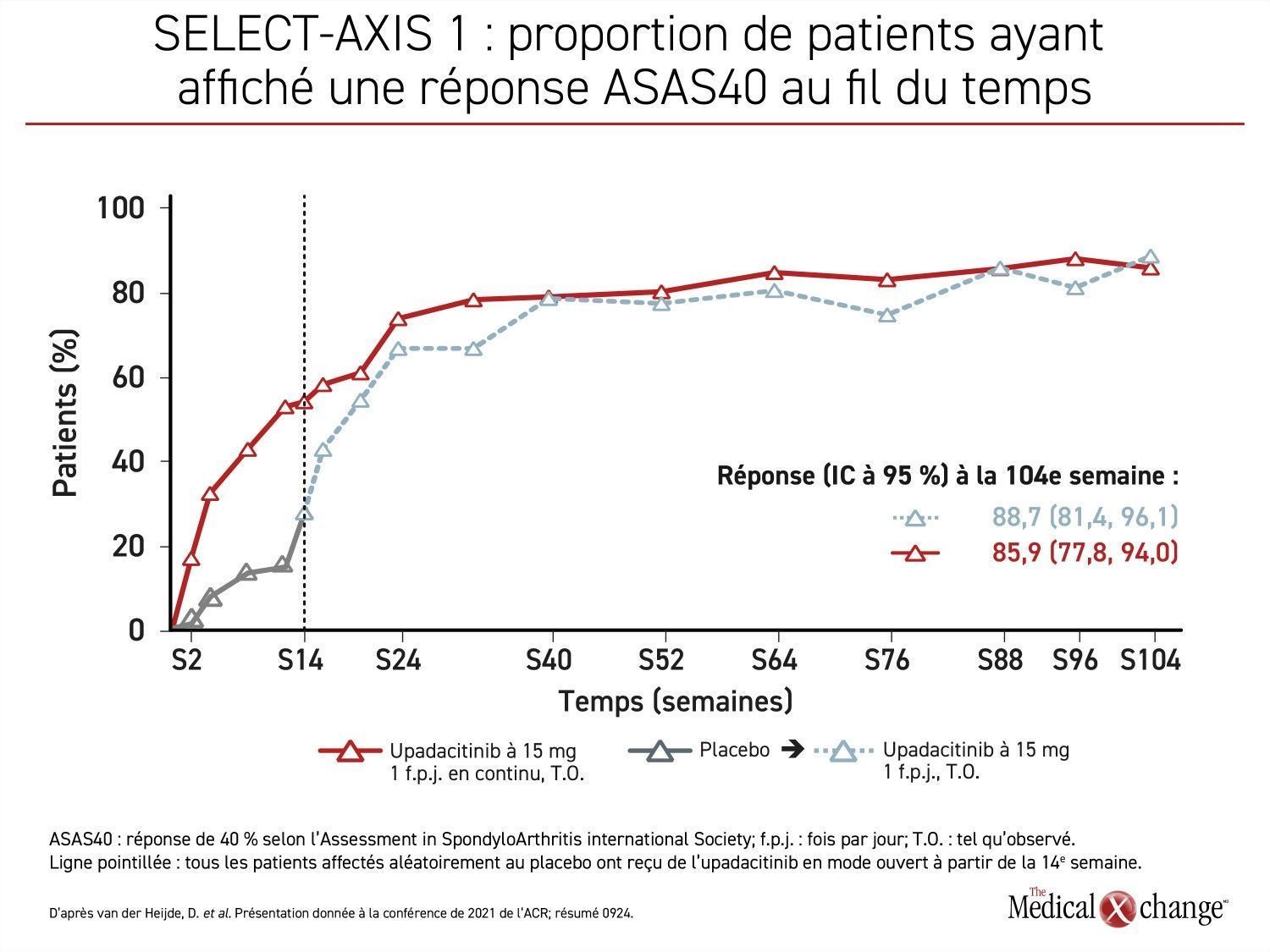
Selon les résultats de l’essai de phases II/III SELECT-AXIS 1 que le Dr Deodhar a aussi présentés à la conférence de cette année, la proportion de patients traités par l’upadacitinib ayant affiché une réponse ASAS40 à la 14e semaine s’est non seulement maintenue jusqu’à la fin de la période de 16 semaines, mais a continué d’augmenter pendant les 104 semaines de suivi (Figure 1).
« Le taux de réponse ASAS40, le paramètre d’évaluation principal, a constamment augmenté en 2 ans, sans jamais fléchir, et aucune nouvelle inquiétude du côté de l’innocuité n’a été soulevée par rapport à la 16e semaine. »
Le Dr Deodhar ajouté : « Le taux de réponse ASAS40, le paramètre d’évaluation principal, a constamment augmenté en 2 ans, sans jamais fléchir, et aucune nouvelle inquiétude du côté de l’innocuité n’a été soulevée par rapport à la 16e semaine ».
La famille des JAK et l’inflammation vertébrale causée par la SpA
Les JAK sont une famille de 4 tyrosines kinases intracellulaires (JAK1, JAK2, JAK3 et TYK2) qui font office de transducteurs de signaux pour un large éventail de cytokines pro-inflammatoires, dont celles qui sont particulièrement impliquées dans la SpA, telles que l’interleukine-12 (IL-12) et l’IL-23. C’est l’inhibition relative que chaque inhibiteur de JAK exerce sur les divers membres de cette famille qui fera probablement en sorte qu’il se démarque par ses bienfaits et les risques qu’il comporte. La régulation négative des signaux inflammatoires observés avec les agents qui en sont aux derniers stades de leur développement n’a pas seulement été reliée à la maîtrise des symptômes, mais aussi à un ralentissement de l’évolution de la SpA à la radiographie.
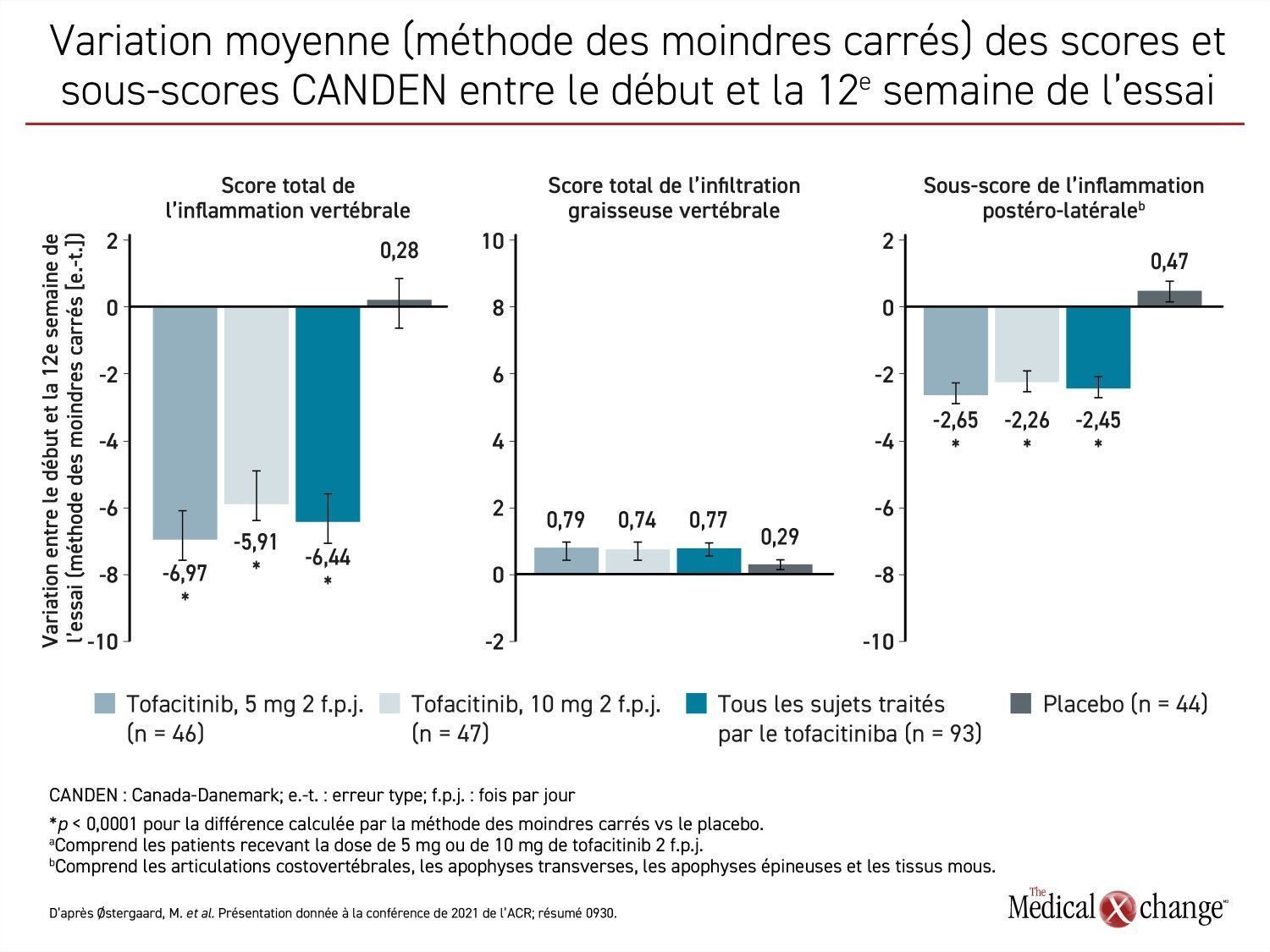
Une étude dont il a aussi été question à la conférence et qui a mis au jour l’effet positif de l’inhibition des JAK sur l’inflammation de la colonne vertébrale reposait sur le système d’évaluation par IRM CANDEN (Canada-Denmark). Elle a été menée chez 137 patients atteints de SpA jamais traitée par des agents biologiques, qui ont été affectés aléatoirement à une des deux doses de tofacitinib (5 ou 10 mg) administrées deux fois par jour ou à un placebo. Au bout de 12 semaines de traitement par les deux doses de tofacitinib, les baisses des sous-scores enregistrés pour l’inflammation du corps vertébral étaient très significatives comparativement au placebo. C’était aussi le cas des réductions objectivées pour plusieurs autres mesures de l’inflammation de la colonne vertébrale et des facettes articulaires lombaires, y compris pour l’inflammation postérolatérale (Figure 2).
« Le système d’évaluation des clichés d’IRM CANDEN a été créé pour permettre d’évaluer en détail les lésions inflammatoires et structurales des corps vertébraux et des structures postérieures chez les patients atteints de SpA à partir de données anatomiques », a expliqué le Dr Mikkel Østergaard, président du Centre de recherche sur l’arthrite de Copenhague, au Danemark, avant d’ajouter que la réduction de l’inflammation visible sur les clichés à 12 semaines était compatible avec l’inhibition des JAK objectivée en clinique et en recherche.
Régulation négative de l’inflammation dans la colonne vertébrale
« Le tofacitinib a atténué l’inflammation des structures postérolatérales de la colonne vertébrale et des facettes articulaires, ce qui est sans précédent », a affirmé le Dr Østergaard.
« [Il y avait une] inflammation des structures postérolatérales de la colonne vertébrale et des facettes articulaires, ce qui est sans précédent. »
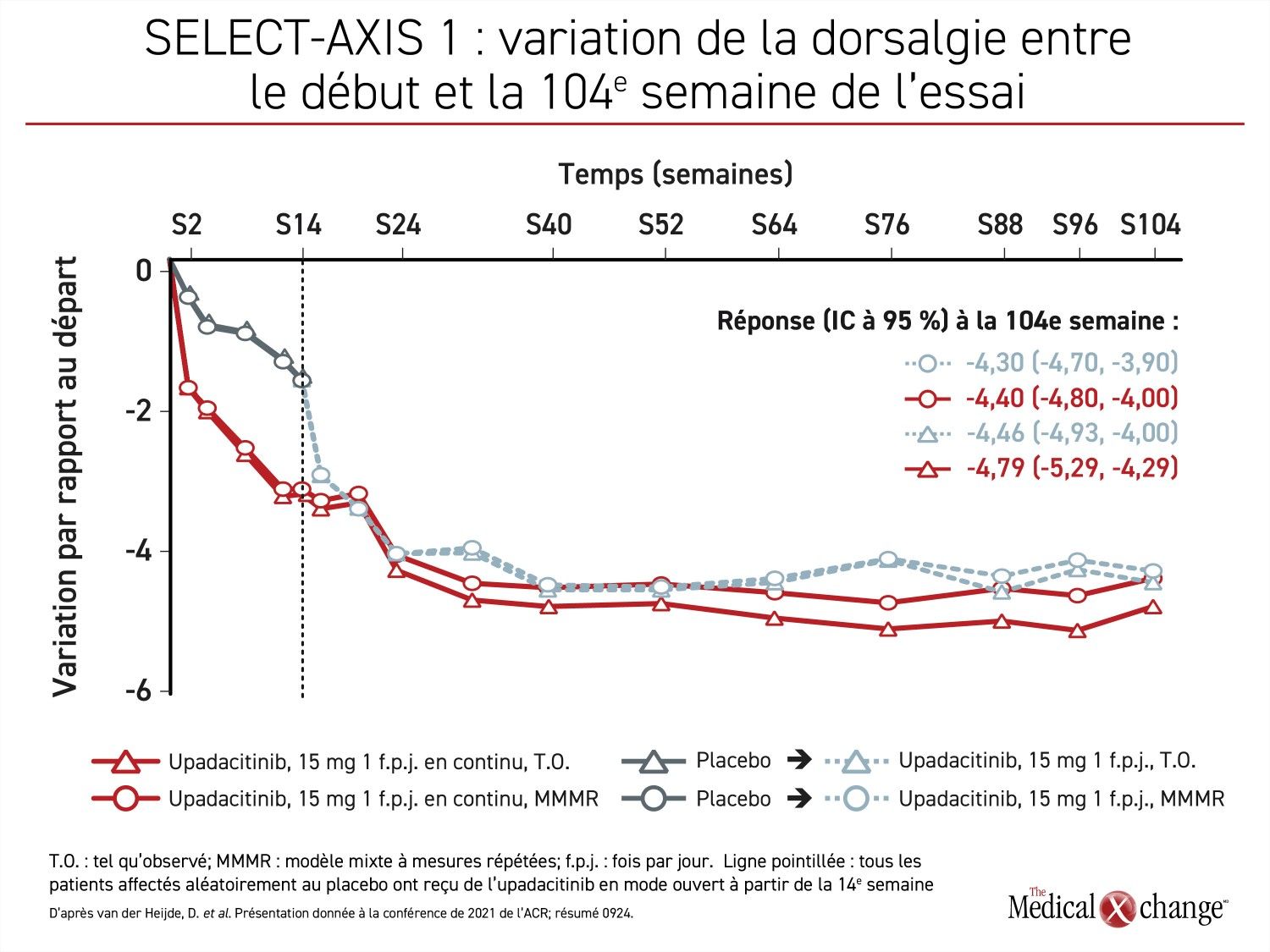
Un des paramètres évalués pendant la phase de prolongation de longue durée de l’essai SELECT-AXIS 1 sur l’upadacitinib était la maîtrise de la dorsalgie. Au terme des 16 premières semaines menées à l’insu, lorsque le placebo a été remplacé par l’upadacitinib chez les témoins, les scores attribués aux symptômes de dorsalgie ont continué de baisser pendant 4 autres mois au moins dans le groupe upadacitinib avant d’atteindre un plateau et de s’y maintenir pendant le reste des 104 semaines. Quant aux sujets d’abord affectés au placebo, leur dorsalgie a diminué abruptement après leur passage à l’upadacitinib. Environ 2 mois après le début de la phase de prolongation, les sujets des deux groupes bénéficiaient d’une maîtrise similaire de leur dorsalgie (Figure 3).
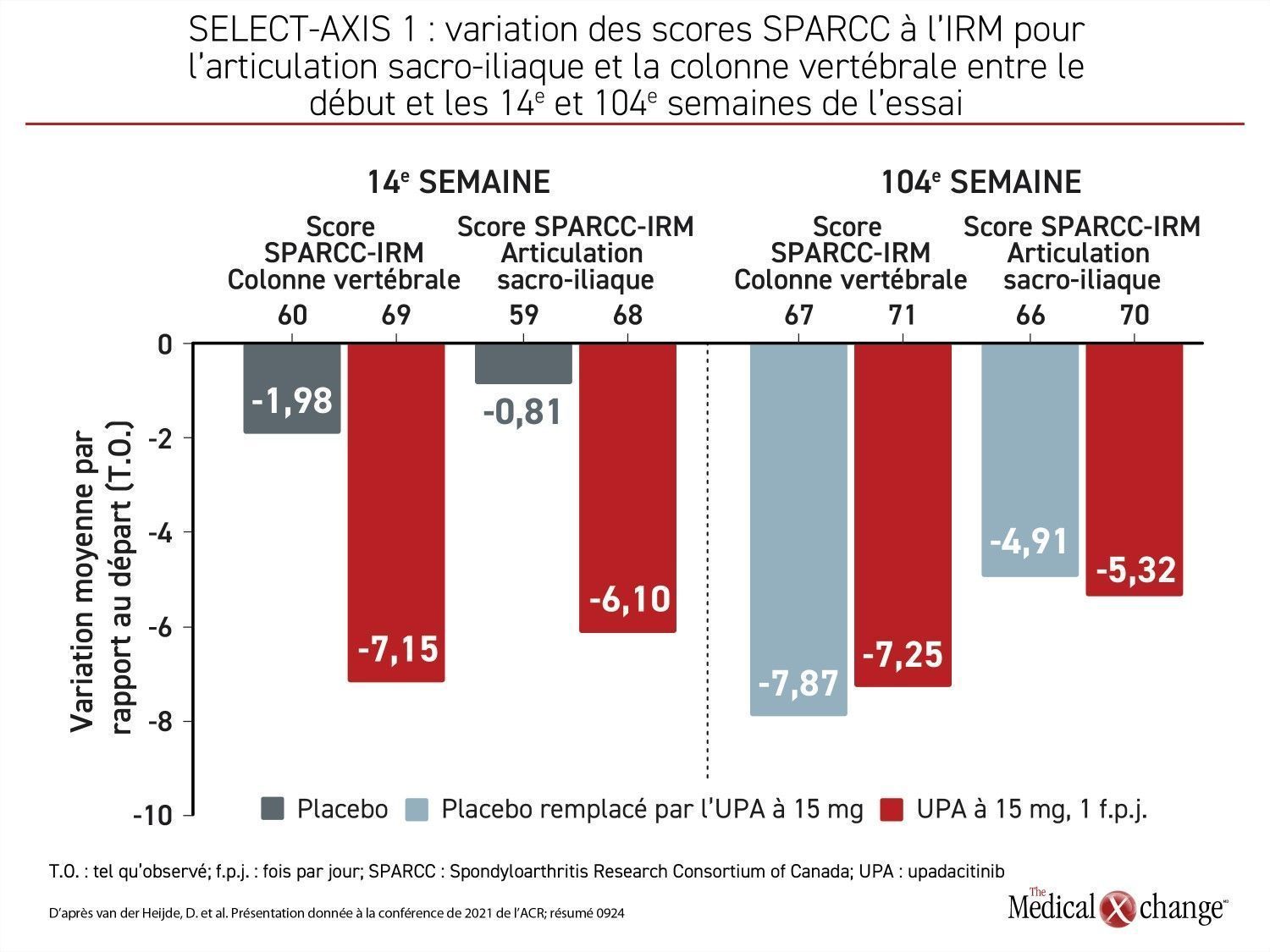
Des examens par imagerie ont aussi été réalisés pendant le suivi de longue durée de l’essai SELECT-AXIS 1. L’analyse des clichés d’IRM au moyen du système d’évaluation de l’articulation sacro-iliaque et de la colonne vertébrale du Consortium canadien de recherche sur la spondylarthrite (SPARCC) a permis de constater que les importantes baisses moyennes des scores enregistrés entre le début et la 14e semaine étaient toujours présentes à la 104e. Chez les sujets passés du placebo à l’upadacitinib à la 16e semaine, les baisses obtenues entre le début et la 104e semaine de l’essai étaient à peu près les mêmes que celles observées dans le groupe traité par l’upadacitinib en continu (Figure 4).
« Les scores les plus bas attribués à la dorsalgie ont généralement persisté pendant le reste des 104 semaines (essai SELECT-AXIS 1). »
Les données sur l’efficacité et l’innocuité obtenues à la 104e semaine sont connues
Lors de l’essai SELECT-AXIS 1, 187 patients ont été affectés aléatoirement à l’upadacitinib à 15 mg une fois par jour ou au placebo. À la 104e semaine, 144 (77 %) participaient toujours à l’essai et ont pu fournir des données pour l’analyse de l’efficacité et de l’innocuité. Les mesures de la réponse clinique prises pendant l’essai ont suivi le même scénario. De façon très similaire à ce qui s’était passé avec la réponse ASAS40, une fois la phase à l’insu terminée, les gains cliniques ont continué de s’accumuler pour plusieurs paramètres d’évaluation, notamment pour les scores d’activité pathologique (< 2,1) et d’inactivité pathologique (< 1,3) évalués respectivement d’après les critères ASDAS (Ankylosing Spondylitis Disease Score) et ASDAS ID.
Le tofacitinib et l’upadacitinib ont été bien tolérés pendant les essais multicentriques d’envergure menés avec contrôle placebo. Lors de l’essai de phase III sur le tofacitinib dirigé par le Dr Deodhar, le taux global d’effets indésirables calculé à 16 semaines était à peu près le même dans le groupe de traitement actif et dans le groupe témoin. Après 48 semaines de suivi, des effets hépatotoxiques avaient été rapportés chez 3 patients, mais aucun n’a été imputé au traitement; même chose pour un cas de méningite. L’incidence du zona, qui a maintes fois été relié aux inhibiteurs de JAK dans des essais cliniques, était de 2,3 % dans le groupe tofacitinib. Aucun cas de psoriasis ou de maladie inflammatoire chronique de l’intestin (MICI) n’a été imputé au traitement. Deux cas d’uvéite ont été recensés, mais les deux patients concernés avaient des antécédents de cette affection. Il n’y a eu aucun cas de cancer, d’incident cardiovasculaire majeur, de thromboembolie veineuse (TEV) ou de pneumopathie interstitielle.
Au terme des 104 semaines de suivi de l’essai SELECT-AXIS 1, aucun cas d’infection grave, d’incident cardiovasculaire majeur, de lymphome, de cancer de la peau avec mélanome bénin, de dysfonctionnement rénal ou de perforation gastro-intestinale n’avait été observé chez les patients traités par l’upadacitinib. L’incidence du zona a été de 2,7 %. On a noté des cas d’uvéite, mais la plupart se sont produits chez des patients ayant des antécédents de cette affection. Le lien de causalité entre les seuls cas de TEV et de MICI survenus pendant le suivi et le traitement est incertain.
Des données substantielles sur l’innocuité
Les données tirées des essais cliniques à propos de l’innocuité du tofacitinib et de l’upadacitinib utilisés contre la SpA concordent avec les très abondantes données collectées depuis le temps que ces agents sont employés contre plusieurs autres maladies. À preuve, l’analyse ayant porté sur plus de 3000 patients atteints de polyarthrite rhumatoïde (PR), sur près de 1000 patients aux prises avec le rhumatisme psoriasique (RP) et sur 182 patients affligés de SpA qui a été présentée à la réunion Convergence de 2021 de l’ACR par le Dr Gerd Burmester, directeur du Département de rhumatologie et d’immunologie clinique, à l’Hôpital de la Charité, à Berlin, en Allemagne.
Cette analyse a servi à comparer l’innocuité de l’upadacitinib à celle du méthotrexate ou de l’adalimumab après ajustement en fonction de l’exposition. Encore là, le zona, comme ce fut le cas dans de nombreux autres essais cliniques, a été plus répandu avec l’inhibiteur de JAK. Cela dit, l’incidence des effets indésirables, comme les incidents cardiovasculaires majeurs, la TEV et les infections respiratoires supérieures, était semblable.
« Quoique faibles, les taux de zona sont significativement plus élevés avec les inhibiteurs de JAK qu’avec les autres agents couramment employés pour traiter les arthropathies inflammatoires », a rapporté le Dr Burmester, qui a avancé que l’administration d’un vaccin contre cette maladie avant le début d’un traitement par un inhibiteur de JAK devrait réduire ce risque, voire l’éliminer. Si les inhibiteurs de JAK sont homologués dans le traitement de la SpA comme prévu, il s’attend à ce que leur bilan d’innocuité soit comparable.
Il faut trouver des solutions de rechange aux agents biologiques dirigés contre la SpA
Il faut trouver des solutions de rechange aux agents biologiques comme les inhibiteurs de l’IL-17 et les iTNF pour les cas modérés ou graves de SpA. Les agents biologiques sont très efficaces, mais une minorité notable de patients n’y répondent pas de façon suffisante, alors que beaucoup d’autres cessent d’y répondre au fil du temps. Contrairement aux agents biologiques, les inhibiteurs de JAK s’administrent par voie orale, ce qui peut être vu comme un avantage pour les patients qui souhaitent éviter les médicaments injectables ou qui les supportent mal. Les taux d’efficacité élevés obtenus avec les inhibiteurs de JAK lors des essais cliniques portent à croire qu’ils pourraient concurrencer les agents biologiques comme option de traitement de première intention quand les AINS et les antirhumatismaux de fond ne permettent pas de maîtriser la maladie.
Dans les cas de PR, des comparaisons directes donnent à penser que les inhibiteurs de JAK sont au moins aussi actifs que les iTNF. Lors d’un essai contrôlé par placebo où le tofacitinib a été comparé à l’adalimumab dans le traitement de la PR, l’objectif principal, soit l’obtention d’une réponse ACR20, a été atteint chez 52,6 % et 47,2 % des sujets affectés respectivement au tofacitinib et à l’adalimumab. La différence relative par rapport au placebo (28 %; p < 0,001) était très significative (van Vollenhoven, R.F. et al. N Engl J Med 2012;367:508-519). Le tofacitinib a eu un avantage numérique, mais pas statistique, sur l’adalimumab pour ce qui est de l’amélioration relative des résultats au questionnaire HAQ-DI (Health Assessment Questionnaire-Disability Index) et du score DAS28-ESR (score de l’activité pathologique dans 28 articulations calculé d’après la vitesse de sédimentation érythrocytaire [VSE]).
Lors d’un essai semblable sur l’upadacitinib, cet inhibiteur de JAK et l’adalimumab se sont encore montrés supérieurs au placebo pour la réponse ACR20 à 12 semaines (p < 0,001), mais l’upadacitinib a eu un avantage significatif sur l’adalimumab pour la réponse ACR50, pour l’obtention d’un score DAS28-CRP ≤ 3,2 et pour l’atténuation de la douleur (Fleischmann, R. et al. Arthritis Rheumatol 2019;71:1788-1800). Sur fond de méthotrexate, seul l’upadacitinib s’est révélé supérieur au placebo pour ralentir l’évolution de la maladie visible à la radiographie.
Conclusion
À la lumière des données présentées lors de la réunion Convergence de 2021 de l’ACR, l’homologation des inhibiteurs de JAK pour le traitement de la SpA semble imminente. Les essais de phase III sur le tofacitinib et l’upadacitinib qui ont été publiés ont mis au jour un rapport favorable entre leurs bienfaits et les risques qu’ils comportent, tandis que les données présentées dernièrement ont confirmé la durabilité de leur efficacité et de leur innocuité. Ces données sont entre autres tirées d’études d’imagerie qui ont confirmé une diminution de l’inflammation de la colonne vertébrale compatible avec une atténuation de la dorsalgie. Compte tenu des faiblesses des agents biologiques contre la SpA, notamment l’épuisement de leur effet au fil du temps, les inhibiteurs de JAK pourraient constituer une solution de rechange majeure advenant qu’ils soient homologués comme prévu.