Hématologie
63e réunion annuelle et exposition de l’American Society of Hematology (ASH)
Implications cliniques d’un changement de paradigme attribuable à un inhibiteur de la BTK dans la maladie de Waldenström
Atlanta – Un inhibiteur de la tyrosine kinase de Bruton (BTK) de nouvelle génération force un changement de paradigme dans le traitement de la maladie de Waldenström (MW). Nombreux sont ceux qui avaient déjà jugé révolutionnaire l’essai déterminant sur un inhibiteur de la BTK de première génération employé contre la MW, mais les études suivantes ont montré l’importance de la spécificité pour la BTK, un fait confirmé il y a plus d’un an par un essai de phase III au cours duquel un inhibiteur de la BTK de première génération a été opposé à un autre, de nouvelle génération celui-là. Présentée à la réunion de 2021 de l’ASH, une étude sur l’intolérance menée avec ce dernier a confirmé qu’il est avantageux d’éviter les effets hors cible.
En confirmant l’efficacité de l’ibrutinib, un inhibiteur de la BTK à prise orale de première génération, l’essai déterminant mené chez des patients jamais traités contre une forme récidivante ou réfractaire de la MW a fait évoluer la pratique clinique (TREON, S. P., et al. N Engl J Med, 2015;372:1430-1440). Le zanubrutinib, un inhibiteur de la BTK de nouvelle génération doté d’une activité intense et d’une meilleure tolérabilité que l’ibrutinib auquel il a été opposé durant l’essai de phase III ASPEN (TAM, C. S., et al. Blood 2020;136:2038-2050) a rejoint ce dernier comme agent indiqué contre la MW et a fait preuve d’une plus grande spécificité pour la BTK.
Pour une entrevue exclusive avec le Dr Rayan Kaedbey couvrant l’impact sur la pratique clinique, cliquez ici
Les résultats prometteurs obtenus pour la tolérabilité pendant l’essai ASPEN ont été étayés par les données d’une étude de phase II sur l’intolérance (BGB-3111-215) dirigée par le Dr Mazyar Shadman, du Centre de recherche sur le cancer Fred Hutchinson, de l’Université de l’état de Washington, à Seattle. Cette étude présentée lors de la réunion de 2021 de l’ASH révèle que la plupart des patients intolérants ou réfractaires à l’ibrutinib ou à l’acalabrutinib, un autre inhibiteur de la BTK de nouvelle génération, répondent durablement au zanubrutinib. Attribué au moins grand nombre d’effets hors cible, cet avantage confirme que la sélectivité relative de ces agents est déterminante tant pour leurs bienfaits que pour leur innocuité.
Les effets indésirables des inhibiteurs de la BTK et leurs différences
« Après un suivi médian de 12 mois [patients traités par le zanubrutinib], 70,4 % des manifestations d’intolérance à l’ibrutinib et 83,3 % de celles à l’acalabrutinib ne sont toujours pas réapparues », a affirmé le Dr Shadman.
Ces données s’expliquent par la sélectivité relative de ces trois inhibiteurs de la BTK. Selon une étude ayant servi à comparer leur activité inhibitrice contre 370 kinases au moyen d’une méthode de mesure normalisée de la concentration inhibitrice, l’ibrutinib a inhibé 17 kinases et l’acalabrutinib en a inhibé 15. Or le zanubrutinib n’en a inhibé que 7. L’activité du zanubrutinib, qui est plus forte contre la kinase ciblée et plus faible contre les autres, explique probablement que cet inhibiteur de la BTK plus sélectif que les autres agents actuellement offerts provoque moins d’effets indésirables. Le Dr Shadman croit que l’effet moindre exercé sur les kinases non ciblées explique la plus faible incidence d’effets indésirables.
Comparativement à l’ibrutinib, un inhibiteur de la BTK de première génération, le zanubrutinib a été « conçu de manière à optimiser sa sélectivité et à maximiser sa liaison à la BTK », a déclaré le Dr Shadman. Il s’agissait là d’une lacune à combler. La cardiotoxicité de l’ibrutinib est l’une des raisons qui en a restreint l’usage chez beaucoup de patients atteints de la MW.
Les effets indésirables des inhibiteurs de la BTK moins sélectifs en limitent l’usage
« L’inhibition de la BTK est efficace contre plusieurs hémopathies malignes à lymphocytes B, mais la durée du traitement est limitée en raison des effets indésirables qui en forcent l’interruption », a souligné le Dr Shadman.
Le Dr Shadman a parlé des résultats obtenus à 12 mois chez les 67 premiers patients recrutés dans l’étude en cours sur l’intolérance après qu’ils aient tous abandonné leur traitement par un inhibiteur de la BTK pour cause d’effets indésirables. Ils y forment deux cohortes, une de 57 patients ayant cessé de prendre de l’ibrutinib et l’autre, de 10 patients ayant mis fin à leur traitement par l’acalabrutinib ou par l’ibrutinib et par l’acalabrutinib.
L’inhibition de la BTK est efficace contre plusieurs hémopathies malignes à lymphocytes B, mais la durée du traitement est limitée en raison des effets indésirables qui en forcent l’interruption.
Parmi les principaux critères d’admissibilité, on trouve les suivants : réaction défavorable non hématologique de grade 2 ou plus ayant duré plus de 7 jours ou réaction défavorable hématologique de grade 3 ou plus, sans égard à sa durée.
Le recrutement n’est pas réservé aux patients atteints de la MW, puisqu’ils représentent environ 16,4 % de l’effectif. Des patients auxquels un inhibiteur de la BTK pouvait convenir sont en effet suivis depuis qu’ils sont traités par le zanubrutinib. Ils sont atteints d’un lymphome à cellules du manteau (LCM), d’un lymphome de la zone marginale, d’une leucémie lymphoïde chronique (LLC) ou d’un lymphome à petits lymphocytes (LPL).
Tolérabilité : des résultats prometteurs à la suite de l’abandon de l’ancien inhibiteur de la BTK
Au terme d’un suivi médian de 12,0 mois et d’une exposition maximale au zanubrutinib de 20,3 mois, le traitement se poursuivait toujours chez 84,2 % des sujets qui s’étaient montrés intolérants seulement à l’ibrutinib et chez 80 % de ceux qui n’avaient pas supporté l’acalabrutinib seulement ou l’acalabrutinib et l’ibrutinib. Dans la 1re cohorte, la durée médiane du traitement par l’inhibiteur de la BTK antérieur était de 10,6 mois comparativement à 3,3 mois seulement dans la 2e. Pendant cette étude, 63 % des patients ont pris des doses de 160 mg de zanubrutinib deux fois par jour; les autres ont pris des doses de 320 mg une fois par jour.
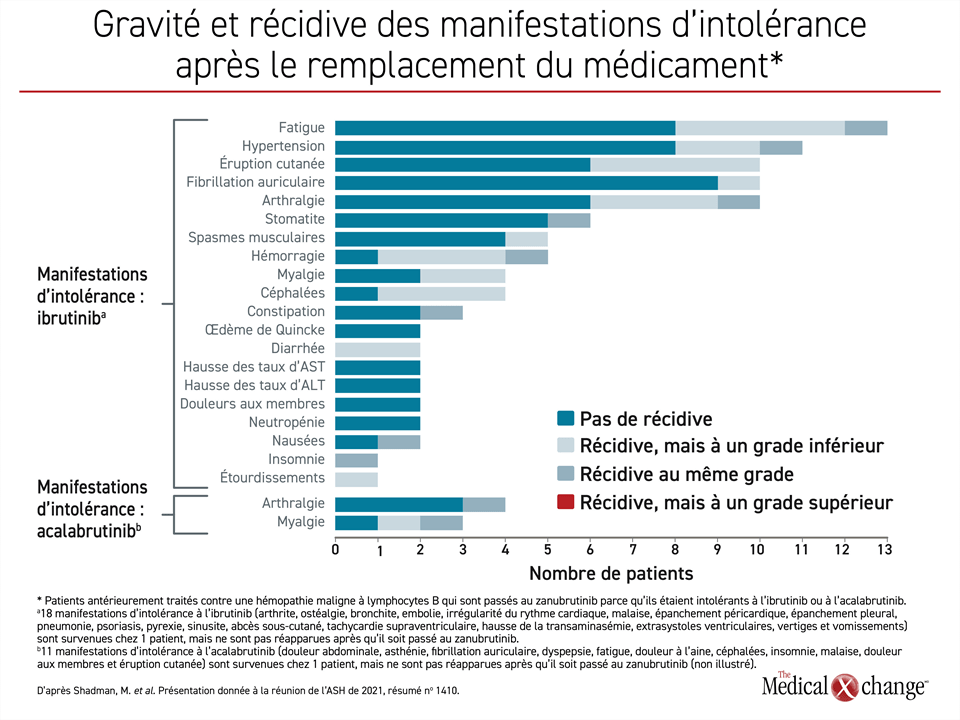
« Parmi les manifestations d’intolérance qui sont réapparues, 76,5 % et 33,3 % de celles survenues respectivement pendant les traitements antérieurs par l’ibrutinib et par l’acalabrutinib se sont reproduites avec la même intensité, mais aucune ne s’est révélée plus grave », a rapporté le Dr Shadman (Figure 1).
Parmi les plus de 80 % des patients qui, à 12 mois, prenaient toujours du zanubrutinib après avoir cessé de prendre de l’ibrutinib, de l’acalabrutinib ou ces deux agents, l’inhibiteur de la BTK plus sélectif « a permis à tout le moins de préserver la réponse de 93,8 % des patients, voire de l’améliorer chez 64,1 % d’entre eux par rapport au départ », a affirmé le Dr Shadman. Un seul patient a mis un terme au traitement par le zanubrutinib en raison d’une manifestation d’intolérance qu’il avait déjà subie avec un autre inhibiteur de la BTK. Des effets secondaires ont motivé l’arrêt du traitement par le zanubrutinib avant la fin de la période de suivi chez 7,5 % des patients.
Les avantages notés en matière d’intolérance concordent avec les résultats de l’essai ASPEN
Après l’arrêt de leur traitement par l’ibrutinib ou l’acalabrutinib, les sujets de cette étude de phase II ont affiché une tolérance relative similaire envers le zanubrutinib, quelle que soit l’hémopathie maligne à lymphocytes B dont ils étaient atteints. Cette tolérabilité supérieure du zanubrutinib par rapport à celle de l’ibrutinib cadre avec les résultats de l’essai comparatif à répartition aléatoire ASPEN. Selon le chercheur principal de cet essai, le Dr Constantine S. Tam, directeur du Service d’hématologie de l’Hôpital universitaire Saint-Vincent de Melbourne, en Australie, le zanubrutinib pourrait bien être à la fois plus efficace et plus sûr que l’ibrutinib, non seulement parce qu’il est plus sélectif, mais aussi en raison de ses caractéristiques pharmacocinétiques et pharmacodynamiques.
Pendant l’essai de phase III ASPEN qui s’est déroulé dans 58 établissements, 164 patients affligés d’une MW récidivante (après au moins un traitement) et 37 patients atteints d’une MW jamais traitée auparavant ont été répartis aléatoirement de façon à prendre de l’ibrutinib ou du zanubrutinib. La maladie était symptomatique et mesurable chez tous les patients qui étaient tous admissibles au traitement selon des critères définis par consensus. Le paramètre d’évaluation principal de l’efficacité comportait deux critères : la réponse complète (RC) et la très bonne réponse partielle (TBRP). Les effets indésirables ajustés en fonction de l’exposition et leur incidence globale ont aussi été comparés.
« Nous avons relevé plusieurs différences d’importance clinique dans le tableau d’innocuité et de tolérabilité des deux inhibiteurs de la BTK, qui s’expliquent probablement par le fait que le zanubrutinib a une plus grande sélectivité pour la BTK que pour les autres kinases », a signalé le Dr Tam.
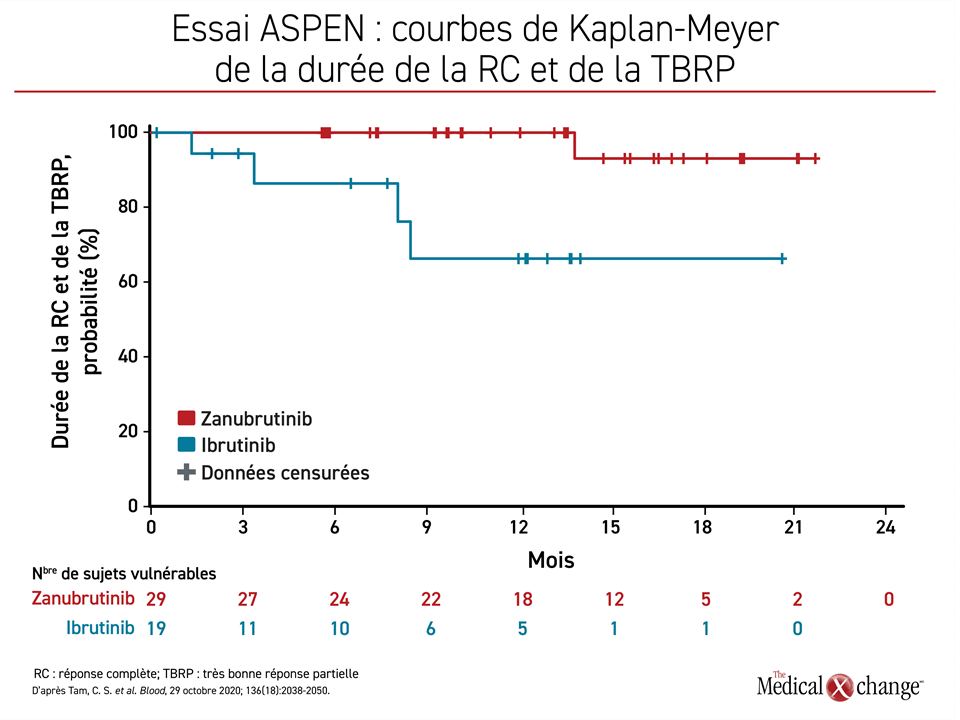
Au terme d’un suivi médian de 19,4 mois, aucun sujet des deux groupes n’avait obtenu une RC, mais le taux plus élevé de TBRP obtenu avec le zanubrutinib (28 % vs 19 %; p = 0,09) frôlait la signification statistique. De plus, la supériorité du zanubrutinib pour le taux de TBRP a été observée dans les deux groupes de sujets, celui des patients en rechute (29 % vs 20 %) et celui des patients jamais traités auparavant (26 % vs 17 %). La courbe tracée en fonction du temps a montré que les réponses marquées obtenues avec le zanubrutinib ont duré plus longtemps (Figure 2).
À 18 mois, le taux de survie sans progression (SSP) et la durée des réponses marquées n’avaient pas beaucoup changé. Cela dit, le zanubrutinib a semblé avoir l’avantage pour ce qui est du taux de patients indemnes de tout incident à la lumière des résultats obtenus pour le paramètre d’évaluation principal (taux de RC et de TBRP) dans les deux groupes de sujets, soit celui des patients atteints d’une MW récidivante (90 % vs 64 %) et celui des patients jamais traités auparavant (100 % vs à déterminer).
Effets indésirables : une tendance se dessine
Autre point important, l’essai ASPEN a aussi fait ressortir des différences d’innocuité entre les deux inhibiteurs de la BTK. Bien que les effets indésirables de grade 3 ou plus n’aient été que légèrement plus répandus dans le groupe ibrutinib (63 % vs 58 %), il n’en demeure pas moins que la fibrillation auriculaire, la diarrhée, les spasmes musculaires et la pneumonie s’y sont tous produits à une fréquence plus élevée d’au moins 10 %. Le seul effet indésirable s’étant manifesté à une fréquence de 10 % ou plus dans le groupe zanubrutinib a été la neutropénie. Notons toutefois qu’elle n’a entraîné aucune hausse du taux d’infection.
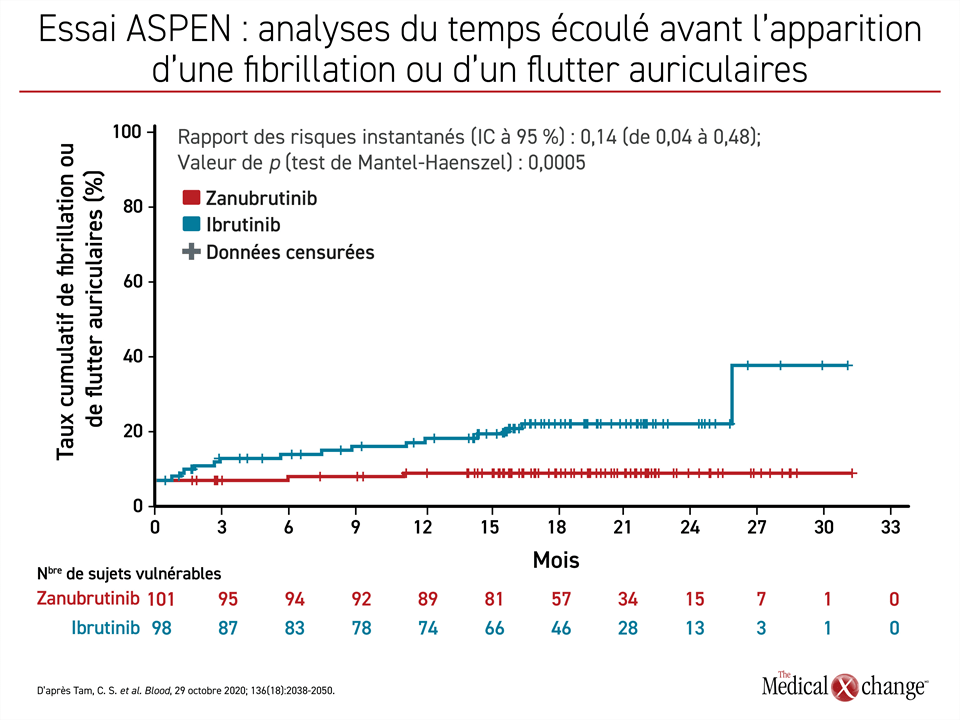
Nombreux sont les écarts calculés pour les effets indésirables qui ont franchi le seuil de la signification statistique. Notons plus particulièrement le taux de fibrillation ou de flutter auriculaires qui a été significativement plus élevé avec l’ibrutinib (p = 0,0005) (Figure 3), ce qui cadre avec l’expérience clinique acquise avec cet agent. La cardiotoxicité a constitué un motif majeur d’interruption de ce traitement. Lors de l’essai ASPEN, le taux de fibrillation auriculaire tous grades confondus par tranche de 100 mois-patients s’est chiffré à 0,1 dans le groupe zanubrutinib et aucun cas d’effet cardiotoxique de grade 3 n’y a été enregistré, alors que dans le groupe ibrutinib, on en a signalé à un taux de 0,2/100 mois-patients.
Bien que les taux globaux d’infections et d’infections de grade 3 ou plus aient été similaires dans les deux groupes, la neutropénie a été plus répandue avec le zanubrutinib (p = 0,007). En revanche, la pneumonie l’a été davantage dans le groupe ibrutinib (p = 0,004). Les cas d’hémorragie tous grades confondus ont été significativement moins fréquents avec le zanubrutinib (p = 0,04), mais l’écart enregistré pour les cas d’hémorragie majeure, qui étaient moins nombreux, n’a pas franchi le seuil de la signification statistique. À 15 mois environ, les taux d’hypertension ont grimpé et sont restés élevés dans le groupe ibrutinib comparativement au groupe zanubrutinib, quoique l’écart entre les deux groupes n’ait pas franchi le seuil de la signification statistique à la fin de l’essai (p = 0,16).
Le rôle du gène MYD88 dans la MW
Une mutation du gène MYD88, dont plus de 90 % des patients atteints de MW sont porteurs, est vue comme la principale source d’activation de la BTK, ce qui pourrait expliquer pourquoi les patients qui n’en sont pas porteurs répondent mal à l’ibrutinib. Or selon une sous-étude de l’essai ASPEN maintenant publiée (DIMOPOULOS, M. et al. Blood Adv, 2020;4:6009-6018), ce ne serait pas le cas du zanubrutinib. En effet, 27 % des 28 patients d’une cohorte dont le gène MYD88 n’était pas muté ou dont le statut mutationnel était inconnu, qualifié de gène de type sauvage (MYD88WT), ont affiché une TBRP et 50 %, une réponse majeure définie comme une réponse partielle ou mieux lorsqu’ils ont été traités par le zanubrutinib. Selon les quelques données dont nous disposons sur l’ibrutinib, peu de patients atteints de la MW à gène MYD88WT obtiennent une réponse marquée avec cet agent.
« Notre étude montre clairement que le zanubrutinib est efficace quand il est utilisé seul chez des patients atteints de la MW et porteurs d’un gène MYD88WT », a déclaré le Dr Meletios Dimopoulos, directeur du Département de thérapeutique clinique, à l’Université nationale et capodistrienne d’Athènes, en Grèce, et chercheur principal de la sous-étude ASPEN. Il a ajouté que ces patients étaient difficiles à traiter compte tenu de leur réponse médiocre à la plupart des médicaments et pas juste à l’ibrutinib.
Comme la surproduction d’IgM est le signe d’appel de la MW, la possibilité d’en réduire la concentration devient un critère de plus pour évaluer l’efficacité des inhibiteurs de la BTK.
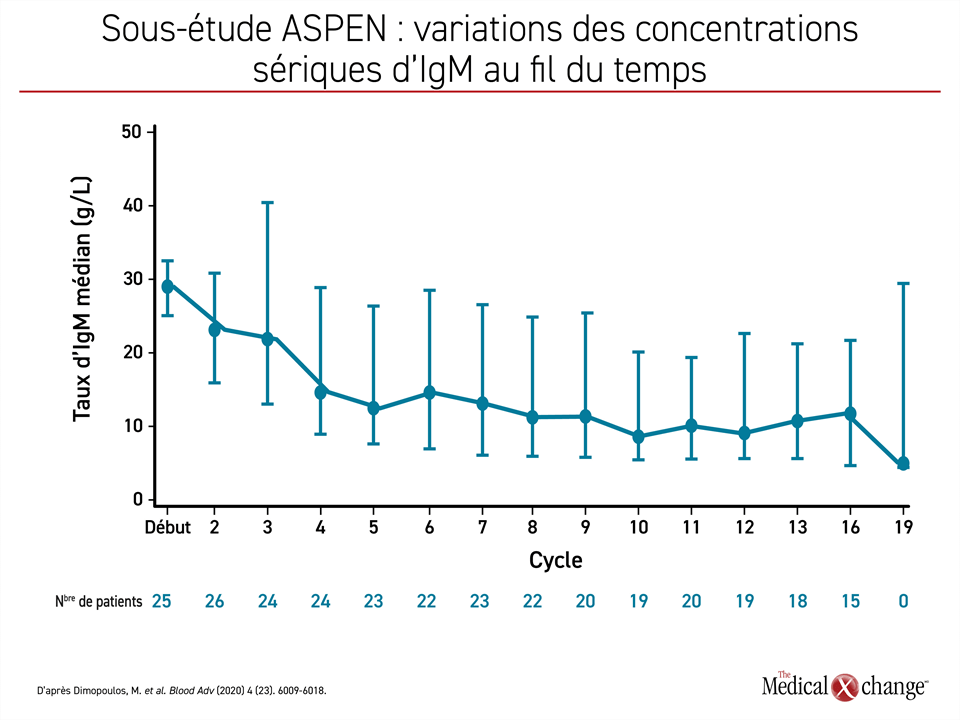
On ne sait pas trop pourquoi le zanubrutinib semble plus actif que l’ibrutinib contre la MW à gène MYD88WT, mais le Dr Dimopoulos a souligné que ces deux agents affichaient d’autres différences quant à leur effet clinique. Pendant l’essai ASPEN, le zanubrutinib a notamment été relié à des baisses plus fortes et plus soutenues des taux d’IgM que l’ibrutinib, une observation qui pourrait aussi avoir un lien avec son activité clinique (Figure 4).
« Comme la surproduction d’IgM est le signe d’appel de la MW, la possibilité d’en réduire la concentration devient un critère de plus pour évaluer l’efficacité des inhibiteurs de la BTK, a renchéri le Dr Tam. À ce chapitre, les résultats de 2 analyses distinctes ont montré que le zanubrutinib avait abaissé les concentrations d’IgM de façon beaucoup plus prononcée et durable que l’ibrutinib ».
Un essai de phase I/II distinct sur le zanubrutinib, dont la période de suivi prolongée a révélé un taux de SSP de 80,5 % et un taux de survie global de 84,8 % à 3 ans (TROTMAN, J. et al. Blood 2020;136:2027-2037), a aussi témoigné de l’efficacité de cet agent contre la MW à MYD88WT. Sur les 8 patients qui en étaient atteints, 5 (62,5 %) ont obtenu une réponse majeure, dont une RC. Autrement dit, ces données portent à croire que le zanubrutinib est une option de traitement approprié, peu importe le statut mutationnel du gène MYD88.
Conclusion
De nouvelles données sur la tolérabilité du zanubrutinib, un inhibiteur de la BTK de nouvelle génération, chez des patients atteints de la maladie de Waldenström (MW) viennent de confirmer l’importance de la sélectivité des inhibiteurs à l’égard de la BTK. Consécutivement à un traitement par le zanubrutinib, près de 65 % des patients qui s’étaient montrés intolérants à un inhibiteur de la BTK moins sélectif ont affiché une meilleure réponse. Par ailleurs, après une année de suivi, la majorité des effets indésirables intolérables n’étaient toujours pas réapparus. Ces résultats concordent avec ceux de l’essai ASPEN et les confirment. L’essai ASPEN était le plus important essai de phase III qui ait été mené à ce jour sur les inhibiteurs de la BTK contre la MW. Or il a établi un parallèle entre la plus grande sélectivité du zanubrutinib pour la BTK et un rapport plus favorable entre les risques et les avantages du traitement.