Gastroentérologie
Colite ulcéreuse : revue d'experts et commentaires tirés de la littérature
Persistance et observance du traitement par le 5-ASA dans la maîtrise à long terme de la colite ulcéreuse légère à modérée
Talat Bessissow, MDCM, MSc, FRCPC
Professeur agrégé de médecine
Division de gastroentérologie, département de médecine, Hôpital général de Montréal
Centre universitaire de santé McGill
Montréal, Québec
Chez les patients atteints de colite ulcéreuse (CU) légère à modérée, l’acide 5-aminosalicylique (5-ASA) est une option de première ligne efficace pour l’objectif de la rémission clinique et endoscopique. Le défi est l’observance quotidienne stricte. L’inobservance du traitement quotidien pendant les périodes de quiescence de la CU est fréquente. Même si les stéroïdes ou d’autres immunomodulateurs complémentaires sont efficaces pour rétablir la maîtrise en cas de poussées, l’observance quotidienne du 5-ASA est une importante défense contre la réactivation de la maladie et des cycles d’activité récurrents avec le potentiel de stimuler la progression de la maladie. Pour guider les patients, il est important de tenir compte des différences entre les produits 5-ASA en ce qui concerne les caractéristiques telles que la formulation, l’administration du médicament et, dans le cas des thérapies orales, le fardeau des comprimés. L’éducation des patients sur le rôle vital joué par l’observance du 5-ASA pour obtenir une maîtrise soutenue de la maladie doit inclure une discussion sur une stratégie qui est susceptible d’être optimalement efficace pour intégrer le traitement dans une routine quotidienne.
Contexte
La gravité de la CU est définie par des facteurs comme le nombre de selles par jour, le saignement, l’étendue et la gravité de l’inflammation des muqueuses à l’endoscopie et l’élévation des marqueurs inflammatoires comme la protéine de calprotectine fécale (PCF).1 Les différences dans l’évolution et le traitement de la CU légère à modérée par rapport à une atteinte plus grave sont importantes. Dans les lignes directrices, la CU légère à modérée et modérée à grave est généralement considérée comme un phénotype distinct. Dans le cas de l’American Gastroenterological Association (AGA), des lignes directrices ont été émises séparément pour la CU légère à modérée et la CU modérée à grave2,3.
Pour une entrevue exclusive avec le Dr Talat Bessissow couvrant l’impact sur la pratique clinique, cliquez ici
Contrairement à la CU modérée à grave, pour laquelle les agents biologiques sont maintenant le traitement de première ligne dans plusieurs lignes directrices, y compris l’AGA, le 5-ASA est uniformément identifié comme étant la pierre angulaire de la prise en charge de la CU légère à modérée. Cela comprend les lignes directrices émises par l’American College of Gastroenterology (ACG),1 la British Society of Gastroenterology (BSG),4 et le Toronto UC Consensus Group.3 Dans les recommandations récemment publiées de l’Organisation internationale pour l’étude de la MICI (IOIBD), appelées STRIDE-II, le 5-ASA a de nouveau été identifié comme une stratégie de première ligne de la CU légère à modérée même si l’objectif thérapeutique de ces recommandations, la guérison endoscopique, est relativement difficile à atteindre.5
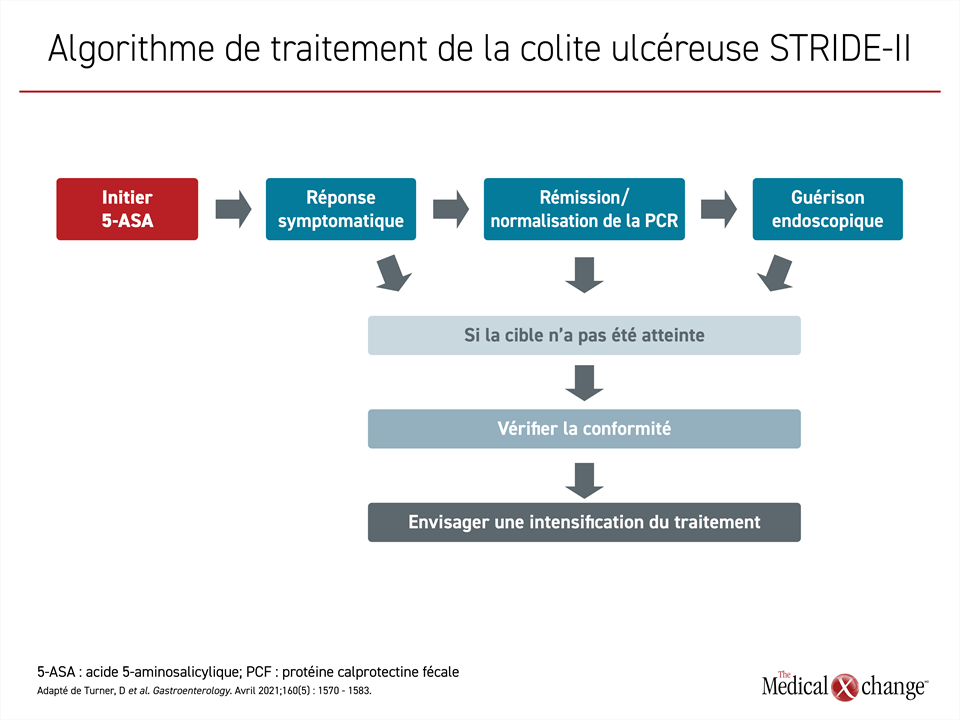
La rémission de la maladie est l’objectif commun de toutes les principales lignes directrices sur la CU, mais la définition de la rémission varie. En 2015, au moment où les dernières lignes directrices consensuelles de Toronto (Toronto Consensus Guidelines, TCT) ont été publiées, un avantage clinique pour obtenir une rémission endoscopique n’avait pas encore été démontré. L’objectif à ce moment était de maintenir une rémission sans corticostéroïdes. À l’inverse, les recommandations de STRIDE-II, publiées en 2021,5 ont identifié la guérison endoscopique comme étant la cible à long terme selon des preuves que ce niveau plus profond de rémission offre une probabilité réduite de rechute (Figure 1).6
D’autres signes de maîtrise de la maladie, comme la normalisation des marqueurs inflammatoires, sont également identifiés comme des signes importants de réponse thérapeutique s’ils ne sont pas un objectif thérapeutique. Des niveaux encore plus profonds de résolution de la maladie, comme la guérison histologique, pourraient constituer une barrière encore plus grande à la récidive de la maladie que la guérison endoscopique, mais cela demeure une question de spéculation en l’absence d’essais contrôlés associant ce paramètre d’évaluation à de meilleurs résultats7.
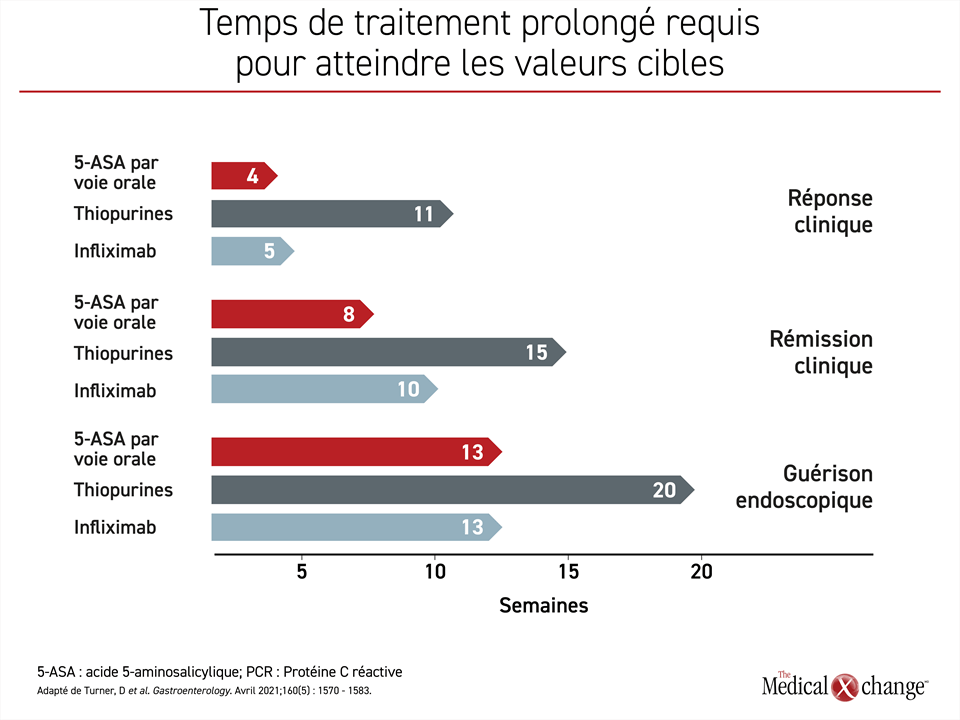
Chez les patients atteints de CU légère à modérée, la maîtrise de la maladie et la guérison dépendent du temps. Selon un aperçu des lignes directrices de la STRIDE-II, le nombre moyen de semaines de maîtrise des symptômes après l’instauration du 5-ASA est de 4 semaines. Les étapes subséquentes du processus de guérison, comme la rémission clinique et la guérison endoscopique, sont plus longues (Figure 2).
Traitements par le 5-ASA différenciés
À la différence de la sulfasalazine, qui est généralement moins bien tolérée que la mésalamine,8, 9 le 5-ASA au Canada est offert en quatre préparations orales et en trois suppositoires pour administration rectale. Bien qu’elles soient prises par la bouche, les formulations orales, comme les suppositoires, atteignent les tissus enflammés comme des traitements topiques. L’étiquetage de ces médicaments, qui se sont tous révélés efficaces et bien tolérés dans le traitement de la CU légère à modérée, est similaire.
Il n’est pas clair si les agents du groupe oral ou du groupe suppositoire diffèrent de manière significative en termes d’efficacité et de sécurité lorsque l’observance au traitement est comparable. De vastes études comparatives sur les différents agents de cette classe n’ont jamais été réalisées. Pour les traitements oraux, les deux différences les plus importantes concernent le mécanisme par lequel ils retardent la libération du 5-ASA pour augmenter la quantité de médicament actif libéré dans le côlon plutôt que plus élevée dans le tractus gastro-intestinal et le fardeau lié aux comprimés. Ces deux différences sont liées. Une administration plus efficace du médicament actif au site d’activité de la maladie est associée à une nécessité plus faible d’ingestion de médicaments par voie orale.
Des quatre produits 5-ASA à administration orale au Canada connus sous les noms de marque PentasaMD, MezavantMD, Teva 5-ASAMDet SalofalkMD, trois retardent la libération du médicament par des mécanismes dépendant du pH. L’autre utilise un mécanisme dépendant du temps. Seules Pentasa, la préparation de 5-ASA qui utilise une libération retardée en fonction du temps, et Mezavant, qui utilise une composition multimatrice brevetée (MMXâ), permettent une administration quotidienne d’entretien avec seulement peu de comprimés pris une fois par jour. Avec l’administration en fonction du pH, la plupart des médicaments sont libérés lorsque les comprimés ou les capsules atteignent l’iléon terminal, lorsque le pH atteint un niveau qui déclenche la libération du médicament. L’administration en fonction du temps est conçue pour une libération graduelle du médicament une fois que le comprimé atteint l’intestin grêle, ce qui permet une distribution plus uniforme dans la partie proximale du côlon où l’activité de la maladie est souvent concentrée10 (Figure 3).
Des trois suppositoires rectaux 5-ASA disponibles au Canada, PentasaMD, SalofalkMD, et MezeraMD, les deux premiers sont indiqués pour le traitement de la CU distale. Le troisième, qui est une mousse, est indiqué pour le traitement de la CU légèrement active du côlon sigmoïde et du rectum. Dans les cas de la CU légère à modérée, les traitements oraux sont généralement utilisés en première ligne, bien que les suppositoires puissent être une option privilégiée pour les patients présentant une inflammation largement confinée au rectum et au côlon sigmoïde. Dans les cas de maladie étendue, un traitement par voie orale et des suppositoires rectaux pourraient être appropriés pour obtenir une maîtrise de la maladie, mais un traitement d’entretien par le 5-ASA administré par voie orale pourrait être préférable chez les patients qui ne sont pas à l’aise avec l’administration rectale.
Atteindre et maintenir la rémission de la CU légère à modérée
L’activité des 5-aminosalicylates dans la CU est reconnue depuis plus de 50 ans.11 Bien que l’administration efficace de ce traitement sous forme active au site de la maladie ait déjà été un défi, des produits 5-ASA oraux viables sont disponibles depuis plus de 25 ans. Dans le cadre des plus récentes revues de Cochrane, l’efficacité du 5-ASA dans le traitement de la CU a été établie avec un « degré de certitude élevé » sur la base de 54 essais contrôlés par placebo. L’analyse a permis de conclure qu’il existe une certitude modérée selon laquelle le 5-ASA est plus efficace que la sulfasalazine, qui associe la sulfapyridine au 5-ASA. Elle était plus largement utilisée avant que l’administration de 5-ASA en fonction du pH et du temps ne rende cette approche inutile.
Pour la colite du côté gauche légère à modérée, le 5-ASA oral sert souvent de traitement d’induction et de traitement d’entretien. Chez les patients présentant une atteinte plus étendue, y compris une proctite, l’ajout de lavements au 5-ASA ou une courte cure de corticostéroïdes peut être nécessaire pour obtenir ou retrouver une rémission, mais de nombreux patients peuvent espérer de longues périodes de contrôle de la maladie avec le 5-ASA oral seul. Ce sont les nombreuses preuves des avantages et la longue historique d’innocuité qui expliquent la cohérence avec laquelle les directives recommandent ce traitement de première ligne dans la CU légère à modérée.
L’avènement de la stratégie de traitement par cible
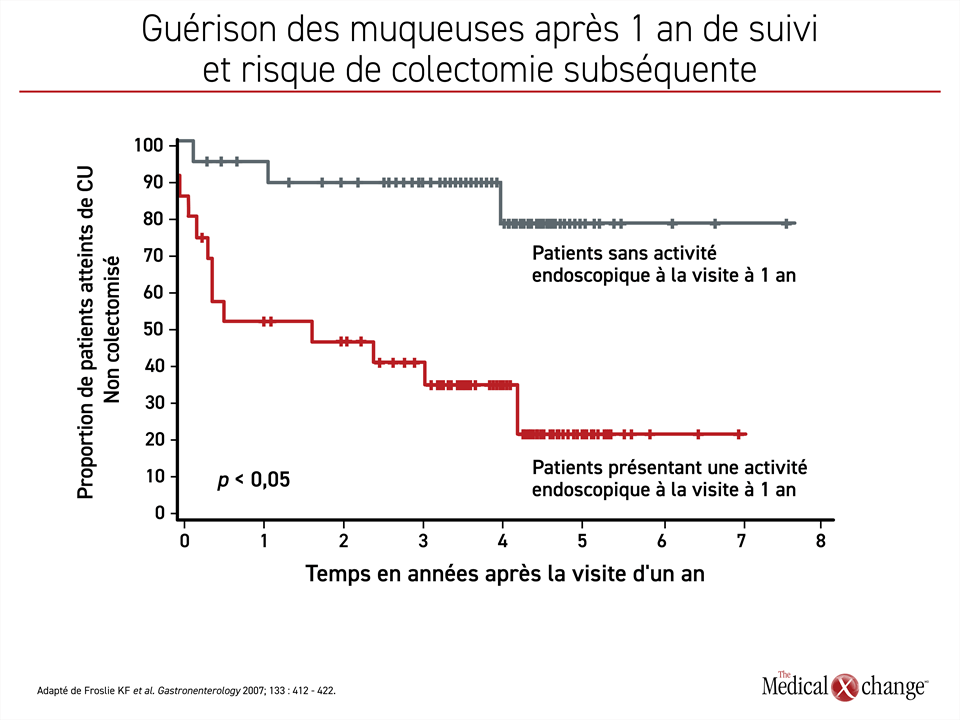
Dans les lignes directrices, le 5-ASA, comme d’autres traitements, est recommandé dans le cadre d’un traitement ciblé. Également connue sous le nom de « traitement ciblé », la thérapie orientée vers un objectif est tirée d’une série d’études qui ont associé une plus grande résolution de l’inflammation à une plus grande barrière ultérieure à la rechute de la CU. Parmi les exemples, une étude a comparé les patients qui avaient obtenu et maintenu une guérison muqueuse à la fin d’un an de traitement à ceux qui n’en avaient pas obtenu. Au bout de 7 ans, la proportion de patients ayant subi une colectomie subséquente était significativement plus faible chez ceux qui avaient atteint le plus haut niveau de rémission de la maladie (~ 20 % vs > 70 %)12 (Figure 4).
Chez les patients suivis au fil du temps, la guérison endoscopique par rapport à une forme moins rigoureuse de rémission a été associée à moins de chirurgies; moins d’hospitalisations, et des périodes de rémission plus longues.13 Il a également été démontré qu’elle se traduit par une meilleure qualité de vie.14 Ces avantages sous-tendent l’appel à la rémission endoscopique dans les récentes recommandations de STRIDE-II, ainsi que la spéculation selon laquelle des définitions encore plus rigoureuses du contrôle de la maladie pourraient constituer une barrière encore plus grande à la rechute.15
Sélection des stratégies de 5-ASA pour l’observance
Pour la CU légère à modérée, le plus grand défi à des niveaux de guérison profonds pourrait être une meilleure observance et non de meilleurs traitements. Dans la CU, l’observance du traitement d’induction doit prolonger la maîtrise des symptômes jusqu’à la guérison de la muqueuse enflammée, ce qui représente une période beaucoup plus longue. Même pendant les périodes de quiescence de la maladie, l’observance du traitement d’entretien est nécessaire pour prévenir la réactivation de la maladie.
L’observance des traitements d’entretien par le 5-ASA pour la colite ulcéreuse légère à modérée s’est révélée faible à plusieurs reprises.16 Dans une étude canadienne rétrospective portant sur les données des réclamations, seuls 27,7 % des patients avaient une bonne adhésion au 5-ASA, définie par un taux de possession de médicaments d’au moins 80 %, au bout de 12 mois.17 D’autres études ont estimé que l’adhésion à long terme au 5-ASA se situait entre 40 et 60 %.16
Les raisons de la non-observance sont complexes. Le sexe masculin et le jeune âge font partie des facteurs de risque de mauvaise observance,16 mais les maladies chroniques avec des périodes de faible fardeau des symptômes, comme l’insuffisance cardiaque,18 présentent un risque de non-observance lorsque l’absence de symptômes supprime l’incitation à prendre les médicaments aux intervalles prescrits.17,19.
La menace d’une mauvaise observance en cas de CU légère ou modérée est une mauvaise maîtrise de la maladie et un risque accru de complications. Dans une étude prospective sur la CU, une mauvaise observance a été associée à une récidive cinq fois plus importante.19 En plus d’une augmentation du risque d’hospitalisation, ainsi que du coût des hospitalisations,20 les conséquences à long terme de la non-observance peuvent mettre la vie en danger. Comparativement aux patients qui n’avaient pas été traités systématiquement pour la CU, une étude de cas témoins publiée il y a plus de 20 ans a associé une observance à long terme avec une réduction de 81 % du risque de cancer colorectal. 21
Il existe deux étapes importantes pour améliorer l’observance. La première est l’éducation du patient qui comprend une description détaillée des objectifs du traitement et de l’importance de traiter au-delà de la maîtrise des symptômes. Même lorsque l’inflammation s’est résorbée et que les lésions ont guéri, le 5-ASA d’entretien constitue une barrière importante à la rechute et à un cercle vicieux de maladie récurrente-rémittente.
La deuxième consiste à prescrire un schéma thérapeutique que le patient trouve facile à intégrer dans une routine quotidienne. Même si les traitements d’induction complexes peuvent représenter un coût inévitable pour le soulagement rapide des symptômes, il est important de reconnaître que les traitements d’entretien sont souvent utilisés lorsqu’il y a un fardeau de symptômes faible ou absent. Une posologie monoquotidienne devrait être préférable lorsqu’elle est efficace. De plus, il a été démontré qu’un faible fardeau posologique est important pour les maladies chroniques en général et pour la prescription de 5-ASA par voie orale chez les patients atteints de CU, en particulier19,22,23.
Résumé
Pour la CU légère à modérée, les principales lignes directrices conviennent du traitement par le 5-ASA comme norme pour l’induction et le maintien de la rémission. L’orientation de traitement vers la cible adoptée par de nombreuses lignes directrices dépend de la prémisse selon laquelle la maîtrise des symptômes est importante, mais insuffisante. Des niveaux plus profonds de maîtrise de la maladie représentés par la suppression de l’activité inflammatoire subclinique, à savoir la normalisation des biomarqueurs et la guérison endoscopique, ont été liés à de meilleurs résultats, mais dépendent de l’observance durable à long terme. Les patients doivent être impliqués dans leurs propres soins en comprenant les objectifs du traitement et l’aspect critique de la poursuite du traitement même en l’absence de symptômes, une étape facilitée par des régimes simples intégrés dans un programme quotidien.
Références
1. Rubin DT, Ananthakrishnan AN, Siegel CA, Sauer BG, Long MD. ACG Clinical Guideline: Ulcerative Colitis in Adults. Am J Gastroenterol 2019;114(3):384-413. DOI: 10.14309/ajg.0000000000000152.
2. Ko CW, Singh S, Feuerstein JD, et al. AGA Clinical Practice Guidelines on the Management of Mild-to-Moderate Ulcerative Colitis. Gastroenterology 2019;156(3):748-764. DOI: 10.1053/j.gastro.2018.12.009.
3. Feuerstein JD, Isaacs KL, Schneider Y, et al. AGA Clinical Practice Guidelines on the Management of Moderate to Severe Ulcerative Colitis. Gastroenterology 2020;158(5):1450-1461. DOI: 10.1053/j.gastro.2020.01.006.
4. Lamb CA, Kennedy NA, Raine T, et al. British Society of Gastroenterology consensus guidelines on the management of inflammatory bowel disease in adults. Gut 2019;68(Suppl 3):s1-s106. DOI: 10.1136/gutjnl-2019-318484.
5. Turner D, Ricciuto A, Lewis A, et al. STRIDE-II: An Update on the Selecting Therapeutic Targets in Inflammatory Bowel Disease (STRIDE) Initiative of the International Organization for the Study of IBD (IOIBD): Determining Therapeutic Goals for Treat-to-Target strategies in IBD. Gastroenterology 2021;160(5):1570-1583. DOI: 10.1053/j.gastro.2020.12.031.
6. Ungaro R, Colombel JF, Lissoos T, Peyrin-Biroulet L. A Treat-to-Target Update in Ulcerative Colitis: A Systematic Review. Am J Gastroenterol 2019;114(6):874-883. DOI: 10.14309/ajg.0000000000000183.
7. Chateau T, Feakins R, Marchal-Bressenot A, Magro F, Danese S, Peyrin-Biroulet L. Histological Remission in Ulcerative Colitis: Under the Microscope Is the Cure. Am J Gastroenterol 2020;115(2):179-189. DOI: 10.14309/ajg.0000000000000437.
8. Ransford RA, Langman MJ. Sulphasalazine and mesalazine: serious adverse reactions re-evaluated on the basis of suspected adverse reaction reports to the Committee on Safety of Medicines. Gut 2002;51(4):536-9. DOI: 10.1136/gut.51.4.536.
9. Sehgal P, Colombel JF, Aboubakr A, Narula N. Systematic review: safety of mesalazine in ulcerative colitis. Aliment Pharmacol Ther 2018;47(12):1597-1609. DOI: 10.1111/apt.14688.
10. Iacucci M, de Silva S, Ghosh S. Mesalazine in inflammatory bowel disease: a trendy topic once again? Can J Gastroenterol 2010;24(2):127-33. DOI: 10.1155/2010/586092.
11. Mayberry J. The history of 5-ASA compounds and their use in ulcerative colitis–trailblazing discoveries in gastroenterology. J Gastrointestin Liver Dis 2013;22(4):375-7. (https://www.ncbi.nlm.nih.gov/pubmed/24369317).
12. Froslie KF, Jahnsen J, Moum BA, Vatn MH, Group I. Mucosal healing in inflammatory bowel disease: results from a Norwegian population-based cohort. Gastroenterology 2007;133(2):412-22. DOI: 10.1053/j.gastro.2007.05.051.
13. Reinink AR, Lee TC, Higgins PD. Endoscopic Mucosal Healing Predicts Favorable Clinical Outcomes in Inflammatory Bowel Disease: A Meta-analysis. Inflamm Bowel Dis 2016;22(8):1859-69. DOI: 10.1097/MIB.0000000000000816.
14. Lichtenstein GR, Ramsey D, Rubin DT. Randomised clinical trial: delayed-release oral mesalazine 4.8 g/day vs. 2.4 g/day in endoscopic mucosal healing–ASCEND I and II combined analysis. Aliment Pharmacol Ther 2011;33(6):672-8. DOI: 10.1111/j.1365-2036.2010.04575.x.
15. Long MD, Rubin DT. Histologic Remission in Ulcerative Colitis: Are We There Yet? Am J Gastroenterol 2019;114(5):713-715. DOI: 10.14309/ajg.0000000000000235.
16. Testa A, Castiglione F, Nardone OM, Colombo GL. Adherence in ulcerative colitis: an overview. Patient Prefer Adherence 2017;11:297-303. DOI: 10.2147/PPA.S127039.
17. Lachaine J, Yen L, Beauchemin C, Hodgkins P. Medication adherence and persistence in the treatment of Canadian ulcerative colitis patients: analyses with the RAMQ database. BMC Gastroenterol 2013;13:23. DOI: 10.1186/1471-230X-13-23.
18. Ruppar TM, Cooper PS, Mehr DR, Delgado JM, Dunbar-Jacob JM. Medication Adherence Interventions Improve Heart Failure Mortality and Readmission Rates: Systematic Review and Meta-Analysis of Controlled Trials. J Am Heart Assoc 2016;5(6). DOI: 10.1161/JAHA.115.002606.
19. Kane SV. Strategies to improve adherence and outcomes in patients with ulcerative colitis. Drugs 2008;68(18):2601-9. DOI: 10.2165/0003495-200868180-00006.
20. Bassi A, Dodd S, Williamson P, Bodger K. Cost of illness of inflammatory bowel disease in the UK: a single centre retrospective study. Gut 2004;53(10):1471-8. DOI: 10.1136/gut.2004.041616.
21. Moody GA, Jayanthi V, Probert CS, Mac Kay H, Mayberry JF. Long-term therapy with sulphasalazine protects against colorectal cancer in ulcerative colitis: a retrospective study of colorectal cancer risk and compliance with treatment in Leicestershire. Eur J Gastroenterol Hepatol 1996;8(12):1179-83. DOI: 10.1097/00042737-199612000-00009.
22. Farrell B, French Merkley V, Ingar N. Reducing pill burden and helping with medication awareness to improve adherence. Can Pharm J 2013;146:262-269.
23. Lee J, Jee SR, Kim HW, et al. Factors associated with low adherence to oral 5-aminosalicylic acid in patients with ulcerative colitis. PLoS One 2019;14(3):e0214129. DOI: 10.1371/journal.pone.0214129.