neurologie
Réunion annuelle de 2022 de l’American Academy of Neurology (AAN)
La thérapie génique : sûre et efficace chez les enfants plus âgés atteints d’amyotrophie spinale
Seattle – Les symptômes de la forme la plus fréquente et la plus grave d’amyotrophie spinale (AS), une maladie neuromusculaire d’origine génétique, se manifestent dès les premiers mois de vie. Or lorsqu’ils sont traités avant leur apparition à l’aide d’un agent homologué récemment, la plupart des enfants ont un développement normal par la suite. Bien que l’utilité de la thérapie génique n’ait pas été aussi bien étudiée chez les enfants symptomatiques âgés de 6 mois et plus, les données réunies dans un registre prospectif portent à croire qu’ils en retirent aussi des bienfaits s’ils sont traités à 24 mois au plus tard. Leurs fonctions neuromusculaires affichent d’ailleurs des gains que le traitement ait été administré à 6 mois et plus ou à 12 mois et plus. Le registre fait état de la bonne tolérabilité et de l’efficacité de cet agent à posologie pondérale, même si les enfants plus vieux reçoivent de plus fortes doses en raison de leur poids plus élevé.
L’onasemnogène abéparvovec, l’agent de thérapie génique, a été homologué à la fin de 2020 au Canada. Contrairement au nusinersen et au risdiplam, les deux autres agents indiqués contre l’AS, une seule perfusion d’onasemnogène abéparvovec suffit pour rétablir la production déficiente de protéine SMN, ce qui rend le traitement d’entretien inutile. Nous disposons de peu de données sur son administration après l’apparition des symptômes, mais cela pourrait changer grâce au registre RESTORE, un registre d’observation multinational (clinicaltrials.gov; NCT04174157) dans lequel on a documenté les gains observés à la suite de l’administration d’un traitement, peu importe lequel, après l’apparition des symptômes d’AS chez des enfants.
Pour une entrevue exclusive avec le Dr Nicolas Chrestian couvrant l’impact sur la pratique clinique, cliquez ici
Le registre RESTORE, pour des données de pratique clinique obtenues chez des enfants plus vieux
« L’onasemnogène abéparvovec est une option thérapeutique efficace pour les enfants plus vieux et plus lourds, y compris ceux ayant déjà reçu un autre traitement », a affirmé le Dr Richard S. Finkel, directeur du Programme de neurosciences expérimentales, du St. Jude’s Children’s Hospital, de Memphis, au Tennessee.
« [Nous disposons] d’une option thérapeutique efficace pour les enfants plus vieux et plus lourds, y compris ceux ayant déjà reçu un autre traitement. »
Même si l’AS est relativement rare, le registre RESTORE compte déjà plus de 300 patients. Une analyse a porté sur les 145 premiers enfants qui ont été traités à 6 mois ou plus par l’onasemnogène abéparvovec selon 4 schémas thérapeutiques possibles : en monothérapie, en remplacement d’un autre traitement de fond, après ajout d’un autre traitement de fond ou en association d’emblée avec un autre traitement de fond. De ce nombre, 67 enfants étaient âgés de 6 à moins de 12 mois (groupe 1) et 67 autres, de 12 à moins de 24 mois (groupe 2). Un autre groupe comptait 11 enfants qui ont été traités à 24 mois ou plus (groupe 3), ce qui ne respecte pas l’indication homologuée, mais reflète la réalité d’un registre de pratique clinique.
Évaluation des fonctions motrices chez des enfants plus vieux
Plusieurs mesures de la réponse et de l’innocuité ont été utilisées, mais dans l’analyse la plus récente, c’est le score obtenu à l’échelle CHOP INTEND (Children’s Hospital of Philadelphia Infant Test of Neuromuscular Disorders) qui a été le principal paramètre d’efficacité. Cet outil expressément créé pour la surveillance de l’AS permet d’évaluer le fonctionnement neuromusculaire sur une échelle de 0 à 64 points, une variation de 4 points ou plus étant vue comme significative sur le plan clinique.
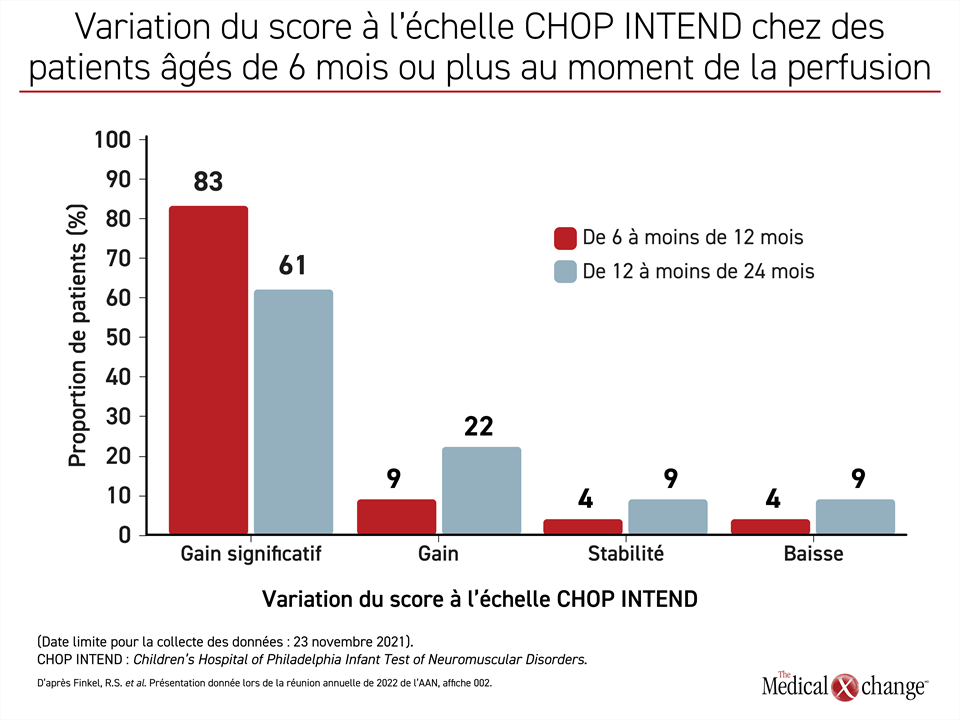
Partant d’une amélioration minimale de 4 points, 19 (83 %) des 23 patients du groupe 1 (au moins 2 évaluations sur l’échelle CHOP INTEND, espacées de plus de 2 mois) évaluables jusqu’à maintenant ont satisfait ce critère témoignant d’un gain significatif; 2 autres (9 %) ont obtenu une amélioration inférieure à 4 points, 1 a obtenu un résultat équivalent et le dernier a enregistré un moins bon résultat.
De même, 14 (61 %) des 23 patients plus vieux du groupe 2 évaluables ont satisfait ce critère. Le score a grimpé de moins de 4 points chez 5 patients (22 %), est resté stable chez 2 autres et a baissé chez les 2 derniers (Figure 1).
Aucun des patients du groupe 3 n’est encore évaluable, mais ils continueront d’être suivis au moyen du registre RESTORE, tout comme les 44 enfants du groupe 1 et 44 enfants du groupe 2. Il est prévu d’y recruter plus de 500 enfants de partout dans le monde et le suivi devrait durer 15 ans.
Sans traitement plusieurs types d’AS sont mortels
L’AS est causée par l’absence ou la délétion du gène SMN1. Le type 1 est à la fois le plus grave et le plus répandu, et le type 2, tout comme le type 1, est habituellement mortel dès la petite enfance s’il n’est pas traité. Le nombre de copies du gène SMN2 est un facteur qui détermine la gravité de la maladie. À l’instar du gène SMN1, le gène SMN2 peut coder pour la production de la protéine SMN, mais en plus faible quantité. La plupart des patients atteints d’AS de type 1 sont porteurs de seulement 2 copies du gène SMN2. Ils produisent moins de protéine SMN et ont tendance à manifester des symptômes plus tôt que ceux atteints d’AS de type 2, et leur maladie évolue plus vite.
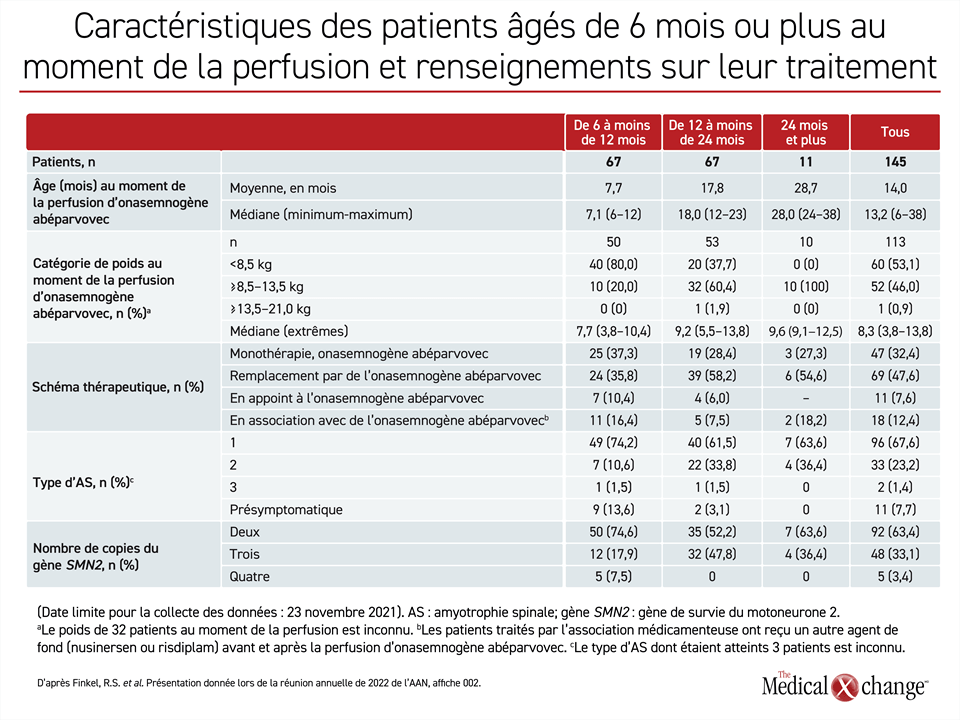
Si on compare les 67 patients recrutés dans le registre RESTORE à l’âge de 6 à moins de 12 mois aux 67 autres recrutés entre 12 et moins de 24 mois, on constate qu’un plus grand nombre des plus jeunes (74 % vs 62 %) étaient atteints du type 1 et qu’ils étaient moins susceptibles d’être aux prises avec le type 2 (11 % vs 34 %). La plupart des autres enfants des deux groupes étaient asymptomatiques au moment de leur recrutement de sorte que le phénotype n’a pas encore pu être déterminé.
Les différences observées pour la chronologie et la gravité des symptômes peuvent expliquer les schémas thérapeutiques du registre RESTORE. Les patients plus jeunes étaient plus susceptibles d’avoir reçu de l’onasemnogène abéparvovec en monothérapie (37 % vs 28 %) et moins susceptibles d’être passés à ce médicament après avoir reçu un autre agent de fond (36 % vs 58 %). Ils étaient également plus susceptibles d’avoir reçu de l’onasemnogène abéparvovec en association avec un autre médicament de fond ou en appoint à un traitement antérieur (27 % vs 14 %) (Tableau 1).
La thérapie génique a eu un effet positif même dans le groupe d’enfants plus âgés
Les patients plus jeunes ont été plus nombreux à obtenir une amélioration notable de leur score à l’échelle CHOP INTEND, ce qui s’explique par les effets positifs de l’augmentation de protéine SMN fonctionnelle dès le début de la maladie, mais il faut souligner que la majorité des patients des deux groupes d’âge en ont retiré des bienfaits. Le Dr Finkel a aussi insisté sur l’obtention d’un taux de réponse supérieur à 80 % chez les enfants plus jeunes, même si la majorité d’entre eux étaient atteints de la forme la plus grave de la maladie. Selon les données étudiées, le nombre de copies du gène SMN2 n’est pas un facteur de prédiction de la réponse.
Il a ajouté : « Si on compare les porteurs de 2 copies [du gène SMN2] aux porteurs de 3 copies, on obtient une amélioration pratiquement équivalente. Le nombre de copies ne semble pas être un facteur de stratification majeur [pour la réponse à la thérapie génique] ».
« Si on compare les porteurs de 2 copies [du gène SMN2] aux porteurs de 3 copies, on obtient une amélioration pratiquement équivalente. Le nombre de copies ne semble pas être un facteur de stratification majeur. »
Dans l’ensemble, les chercheurs ont noté une amélioration de 1 point par mois environ du score CHOP INTEND dans les différents groupes sur une période d’observation de 10 mois à peu près. Jusqu’à maintenant la réponse ne se révèle pas seulement indépendante du nombre de copies, mais aussi de la stratification — que les patients aient reçu de l’onasemnogène abéparvovec en monothérapie, après un autre agent de fond, en association avec un agent de fond ou en appoint à un traitement antérieur.
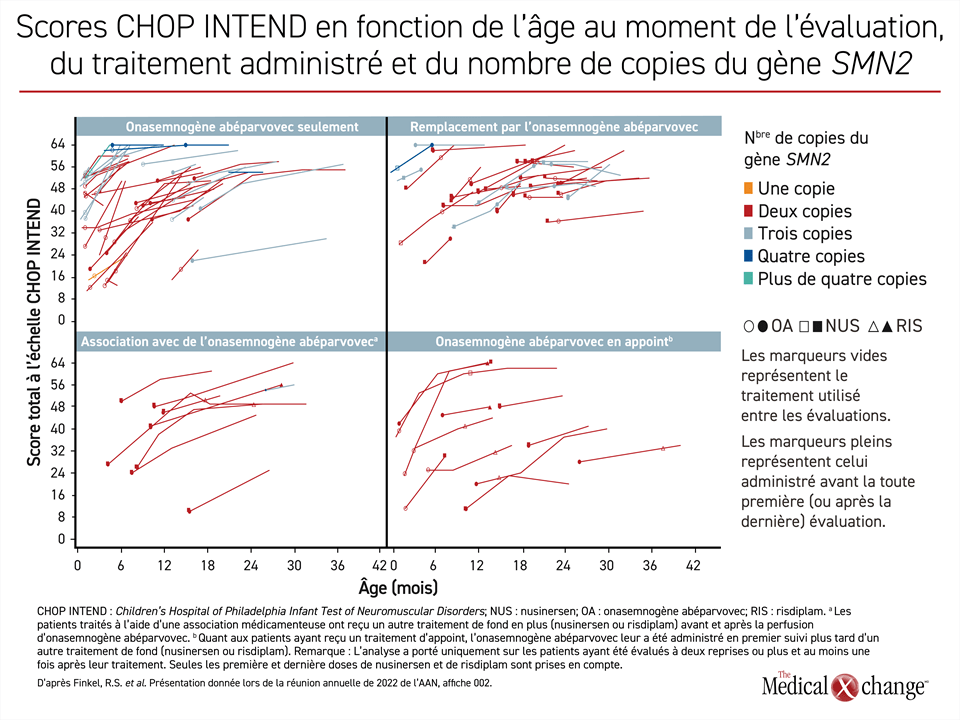
« En étudiant les courbes, on peut voir que presque tous les enfants se sont généralement améliorés. »
« Presque toutes les courbes empruntent une trajectoire ascendante », a déclaré le Dr Finkel. Reconnaissant que le gradient ou l’amélioration était moins prononcé chez les patients plus âgés que chez les plus jeunes, il a ajouté : « Je crois que nous pouvons voir que presque tous les enfants se sont généralement améliorés » (Figure 2).
Une innocuité rassurante chez les enfants plus âgés atteints d’AS
L’innocuité de l’onasemnogène abéparvovec chez les enfants plus vieux a été, en plus de l’efficacité, un élément majeur de l’analyse des données du registre RESTORE non seulement en raison des différents problèmes possibles à cet égard, mais aussi parce que la dose de cet agent est établie en fonction du poids. La dose recommandée est de 1,1 x 1014 génomes de vecteur par kilogramme de poids corporel, administrée en une seule perfusion d’une heure. Comme les enfants prennent du poids en vieillissant, la dose qu’ils reçoivent est donc beaucoup plus élevée. Les données tirées du registre étaient toutefois rassurantes.
« Le tableau d’innocuité de l’onasemnogène abéparvovec chez les patients traités à l’âge de 6 mois ou plus correspond à celui qui avait déjà été rapporté avec cet agent, a déclaré le Dr Finkel. La comparaison des patients en fonction de leur âge et de leur poids n’a fait ressortir aucune tendance à la hausse du risque d’effets indésirables ni de la gravité des effets indésirables ».
« Le tableau d’innocuité de l’onasemnogène abéparvovec chez les patients traités à l’âge de 6 mois ou plus correspond à celui qui avait déjà été rapporté avec cet agent. »
Comme ce fut le cas lors des essais prospectifs, l’analyse des données du registre RESTORE a fait état d’une hausse des taux d’enzymes hépatiques et de la troponinémie, et d’une baisse du nombre de plaquettes. Les effets hépatotoxiques relevés dans cette série étaient majoritairement asymptomatiques, quoique deux enfants ont été atteints d’insuffisance hépatique aiguë; l’un d’eux avait 6 mois et l’autre, 21 mois. Les cas de thrombopénie symptomatique ou d’élévation de la troponinémie n’ont eu aucune conséquence clinique. Quatre cas de microangiopathie thrombotique observée après l’administration d’onasemnogène abéparvovec avaient été rapportés antérieurement, mais aucun cas supplémentaire n’a été observé. Dans cette série, le taux d’effets indésirables graves en général et le taux d’effets indésirables de grade 3 ou plus étaient plus faibles chez les enfants plus vieux que chez les plus jeunes (33,3 % vs 26,5 % et 36,4 % vs 26,5 %, respectivement).
Il est encore impératif de diagnostiquer et de traiter l’AS rapidement
À la lumière des données de pratique clinique tirées du registre RESTORE, l’onasemnogène abéparvovec « est une option thérapeutique efficace pour les patients plus vieux, peu importe leur situation quant aux traitements de fond antérieurs, a soutenu le Dr Finkel. Il n’empêche que ces données ne réduisent en rien l’importance de diagnostiquer l’AS rapidement et d’entreprendre le traitement le plus tôt possible après la naissance, de préférence avant même l’apparition des symptômes ».
« Aux États-Unis, 39 des 50 états disposent de batteries de tests de dépistage qui comprennent l’AS », a affirmé le Dr Finkel. C’est important parce que les données issues d’études de phase III menées avec l’onasemnogène abéparvovec confirment que la plupart des enfants traités pendant qu’ils sont encore asymptomatiques se développent normalement pendant la petite enfance. L’effet positif de la thérapie génique met en évidence l’urgence de traiter rapidement les enfants atteints d’AS de type 1 et porteurs de seulement 2 copies du gène SMN2. Il se peut que les non-spécialistes ne constatent l’absence de développement de la motricité globale consécutive à une carence en protéine SMN qu’une fois que les enfants sont âgés de plusieurs mois, mais selon le Dr Finkel, il est fréquent que les bébés atteints d’AS ne semblent pas se développer normalement dès leurs premières semaines de vie.
Tous les patients traités tôt ont affiché des améliorations
Lors du congrès de l’AAN, l’étude de phase III SPR1NT a de nouveau été passée en revue et les résultats étaient impressionnants. Tous les sujets d’une cohorte de 14 enfants atteints d’AS et porteurs de 2 copies du gène SMN2 (les porteurs de 3 copies font l’objet d’une analyse distincte) ont reçu de l’onasemnogène abéparvovec pas plus de 34 jours après leur naissance, puis ont été suivis pendant 18 mois. Le patient le plus jeune au moment de son traitement avait 8 jours. Or les 14 enfants sont tous capables de s’asseoir seuls et 11 d’entre eux y sont parvenus à un âge jugé normal.
À 18 mois, soit à un âge où il est à prévoir qu’une forte proportion d’enfants atteints d’AS non traitée ait besoin d’assistance alimentaire et peut-être même d’assistance respiratoire, 11 pouvaient se tenir debout sans aide, 9 étaient capables de marcher seuls, 5 d’entre eux y étant arrivés à un âge jugé normal. Tous les enfants ont survécu et aucun d’eux n’a besoin d’assistance respiratoire ou alimentaire.
Les données de pratique clinique collectées dans le registre RESTORE montrent que les enfants plus vieux peuvent aussi retirer des bienfaits de la thérapie génique. Cela dit, il faudra assurer un meilleur suivi pour pouvoir mesurer l’utilité de ce traitement par rapport à l’administration de nusinersen par voie intrathécale ou à celle de risdiplam par voie orale pour préserver durablement les étapes du développement franchies. Les enfants qui ne sont pas traités pendant qu’ils sont encore asymptomatiques ne rattraperont probablement pas leur retard, mais les gains réalisés pour leur fonctionnement neuromusculaire semblent cliniquement importants, même si la thérapie génique est retardée.
Résumé
La thérapie génique opposée à l’AS, une maladie congénitale qui altère peu à peu le fonctionnement neuromusculaire, est offerte depuis plus d’un an au Canada. L’homologation de ce traitement repose sur des études de phase III menées surtout chez des enfants asymptomatiques. Elles ont révélé que beaucoup d’enfants franchissent les étapes normales de leur développement après une seule dose de ce médicament. Les données probantes fournies par le registre RESTORE montrent que les enfants qui le reçoivent après l’apparition des symptômes, même après l’âge de 12 mois, peuvent aussi en retirer des avantages importants. L’onasemnogène abéparvovec a une posologie pondérale. Or la dose plus forte administrée aux enfants plus vieux et donc plus lourds semble aussi bien tolérée que celle reçue par les enfants plus jeunes.