Hématologie
64e réunion annuelle et exposition de l’American Society of Hematology (ASH)
L’éventail thérapeutique opposé à la leucémie myéloïde chronique s’enrichit d’un inhibiteur à petite molécule novateur
Nouvelle-Orléans – Le premier agent d’une nouvelle classe thérapeutique ciblant expressément la poche myristoylée d’ABL (STAMP) a été homologué l’an dernier pour le traitement de la leucémie myéloïde chronique (LMC). Comme c’est souvent le cas avec les nouveaux agents, son emploi est autorisé en troisième ligne, à la suite de l’échec des traitements types. Son efficacité et son innocuité en pareil contexte ont été étayées par de nouvelles analyses à long terme présentées à la réunion de 2022 de l’ASH. De nouvelles données laissent aussi entrevoir la possibilité d’intervenir plus tôt en remplaçant les ITK par cet agent en cas de résistance primaire.
L’homologation par le Canada l’an dernier de l’asciminib, le premier agent de la classe des inhibiteurs « STAMP » (Specifically Targeting the ABL Myristoyl Pocket), pour le traitement de la leucémie myéloïde chronique en phase chronique (LMC-PC) chez les porteurs du chromosome Philadelphie (Ph+) après l’échec de traitements par au moins deux inhibiteurs de la tyrosine kinase (ITK) a reposé sur les résultats de l’étude de phase III intitulée ASCEMBL. Non seulement le taux de réponse moléculaire majeure (RMM) obtenu avec l’asciminib à 24 semaines équivalait presque au double (25,5 % vs 13,2 %) de celui enregistré avec le bosutinib, un ITK de deuxième génération, mais après un suivi médian de 14,9 mois, le taux d’abandons pour cause d’effet indésirable (5,8 % vs 21,1 %) a également été près de 75 % plus bas (Réa, D. et al. Blood 2021;138:2031-2041).
Pour une entrevue exclusive avec le Dr Pierre Laneuville couvrant l’impact sur la pratique clinique, cliquez ici.
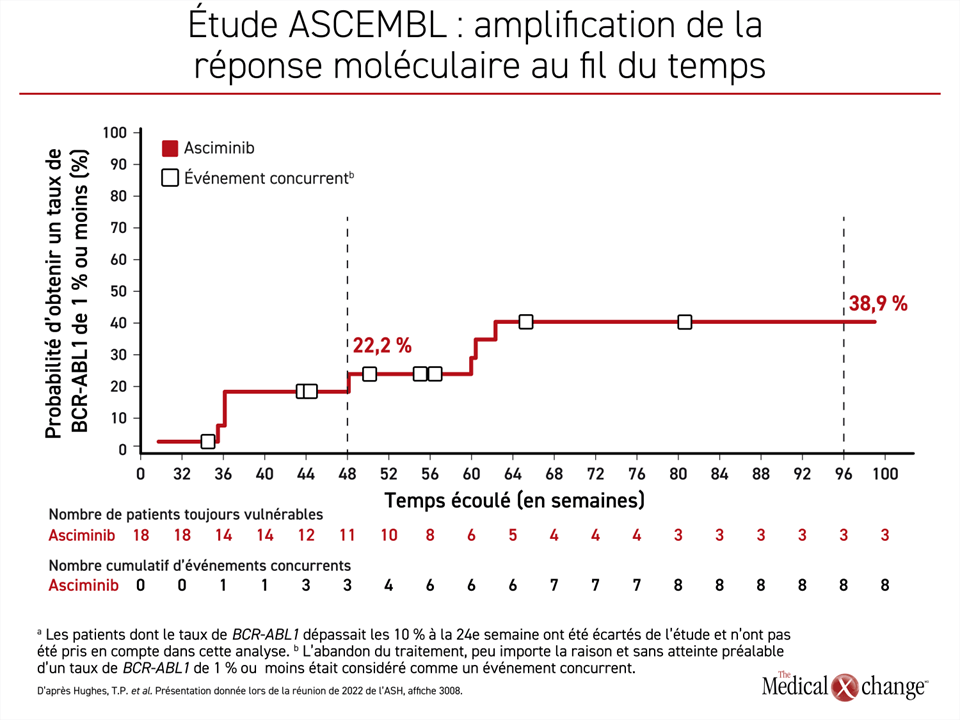
Les données de l’étude ASCEMBL actualisées après un suivi de 2 ans présentées à la réunion de 2022 de l’ASH montrent que la réponse au traitement ininterrompu par l’asciminib s’est amplifiée au fil du temps. Par exemple, selon le Dr Timothy P. Hughes, chef du Département d’hématologie, à l’Hôpital royal d’Adélaïde, en Australie, 22,2 % et 38,9 % des patients du groupe asciminib ayant un taux de BCR-ABL1 ≤ 1 % à 24 semaines affichaient toujours une réponse de cette ampleur à 1 an et à 2 ans, s’ils avaient poursuivi leur traitement (figure 1).
Augmentation des taux de réponse au fil du temps
Dans ces cas d’échec des ITK, « ces résultats montrent que les patients qui poursuivent leur traitement par l’asciminib ont de très fortes chances d’obtenir une RMM plus tard. L’efficacité de l’asciminib une fois que les ITK de deuxième génération ont échoué fait en sorte que cet agent doit être vu comme la nouvelle norme thérapeutique », a affirmé le Dr Hughes.
« Ces résultats montrent que les patients… ont de très fortes chances d’obtenir une RMM. »
L’imatinib, un ITK de première génération, puis les ITK de deuxième génération comme le nilotinib et le dasatinib, ont considérablement amélioré le pronostic de la LMC. Ces agents à prise orale inhibent plusieurs voies de signalisation impliquées dans l’évolution de cette maladie, notamment la protéine BCR-ABL1 en lui faisant compétition pour l’occupation des sites de liaison à l’ATP. Or l’asciminib est le premier inhibiteur allostérique de BCR-ABL1; il cible expressément la poche myristoylée d’ABL (STAMP) plutôt que la poche de fixation à l’ATP. Des études cliniques ont validé les observations faites en laboratoire selon lesquelles ce site de fixation réduit au minimum les effets collatéraux tout en contournant les sources de résistance aux ITK.
Lors de l’étude ASCEMBL, 233 patients atteints de LMC ayant subi de nombreux traitements ont été répartis aléatoirement de façon à recevoir 40 mg d’asciminib deux fois par jour ou 500 mg de bosutinib une fois par jour. En plus des taux de RMM plus élevés, les chercheurs ont objectivé chez les sujets qui n’affichaient pas une réponse cytogénétique complète (RCyC) à leur admission à l’étude, un taux de RCyC de 40,8 % chez ceux du groupe asciminib et de 24,2 % chez ceux du groupe bosutinib. Pour ce qui est des patients dont les mutations étaient connues d’emblée (sauf ceux porteurs des mutations T315I ou V299L), les chercheurs ont constaté une RMM chez 6 des 17 patients (35 %) traités par l’asciminib contre 2 des 8 patients (25 %) ayant reçu du bosutinib.
Des bienfaits sont exercés, peu importe l’ITK utilisé antérieurement
Dans l’analyse actualisée de l’étude ASCEMBL dont il est question ici, les réponses ont été stratifiées en fonction du dernier ITK reçu avant le recrutement. Sauf dans de très rares exceptions, l’asciminib a eu l’avantage sur le bosutinib pour l’obtention d’un taux de BCR-ABL1 ≤ 1 % chez les patients dont ce taux était > 1 % au moment de leur admission, que l’échec du dernier ITK soit dû à une résistance ou à une intolérance. Prenons les patients dont le traitement par le dasatinib avait échoué en raison d’une résistance; 43,6 % de ceux du groupe asciminib et 6,9 % de ceux du groupe bosutinib ont obtenu un taux de BCR-ABL1 ≤ 1 %. Quand une intolérance expliquait l’échec du traitement par le dasatinib, ces taux s’élevaient à 52,0 % et à 28,6 %.
En revanche, si l’asciminib a effectivement surpassé le bosutinib chez les patients n’ayant pas toléré le nilotinib (66,7 % vs 40,0 %), il n’y est pas parvenu chez ceux dont l’échec du traitement était dû à une résistance (38,7 % vs 50 %). L’asciminib l’a emporté sur le bosutinib chez les patients ayant reçu de l’imatinib comme dernier ITK, que ce traitement ait échoué en raison d’une résistance (50,0 % vs 20,0 %) ou d’une intolérance (71,4 % vs 0 %).
Une étude de phase II menée en première ligne
Les nouvelles analyses de l’étude ASCEMBL ayant fait état d’une amplification de la réponse au fil du temps ont été rejointes par deux études prospectives sur l’emploi de l’asciminib à des stades moins avancés de la maladie. Les 100 patients atteints d’une LMC nouvellement diagnostiquée répartis dans 15 établissements australiens et néo-zélandais qui ont participé à l’étude de phase II intitulée ASCEND-CML, que le Dr Hugues a aussi présentée devant l’ASH, y ont reçu de l’asciminib comme traitement de première ligne.
Tous les participants à cette étude prennent 40 mg d’asciminib deux fois par jour. Le traitement sera jugé efficace s’il permet d’atteindre les taux de BCR-ABL1 préconisés dans les lignes directrices de l’ELN (European LeukemiaNet), soit : ≤ 10 % à 3 mois, ≤ 1 % à 6 mois et ≤ 0,1 % à 12 mois. Le traitement sera vu comme un échec si le taux de BCR-ABL1 excède 10 % à 3 ou à 6 mois ou s’il dépasse 1 % à 12 ou à 18 mois. Le cas échéant, les patients continueront de prendre de l’asciminib, mais un ITK choisi par leur médecin y sera adjoint. La dose d’asciminib sera portée à 80 mg deux fois par jour dans les cas où les taux visés par l’ELN ne sont toujours pas atteints à un intervalle de mesure ou à un autre, mais qui ne peuvent pas être considérés comme des échecs.
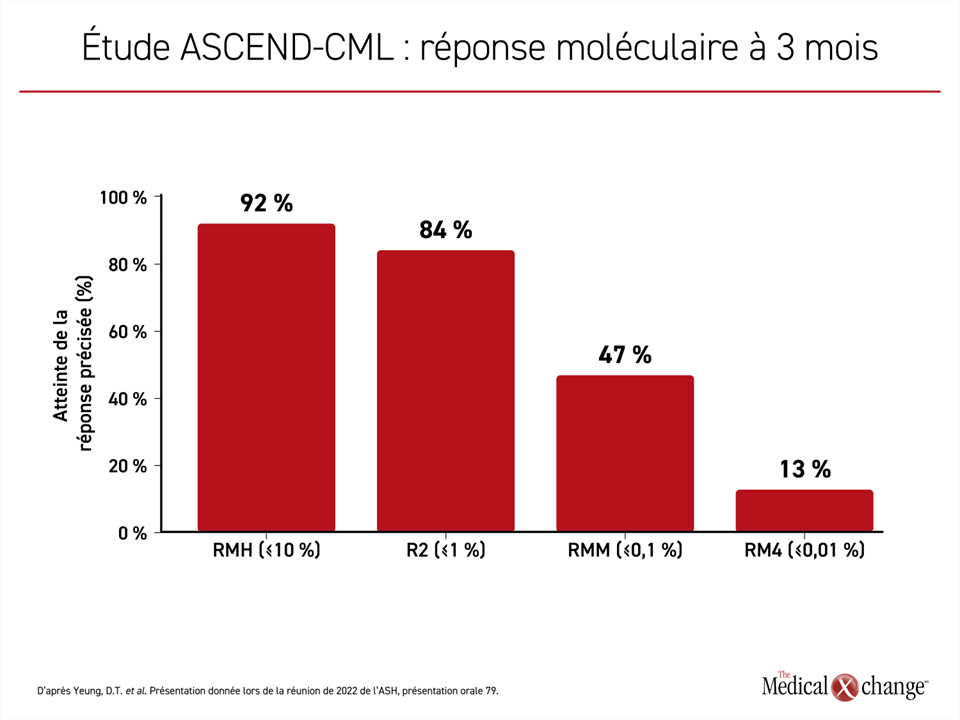
Une analyse intermédiaire des données a révélé que 59 des 63 patients (92 %) suivis depuis 3 mois au moins affichaient une réponse moléculaire hâtive (taux de BCR-ABL1 ≤ 10 % à 3 mois). Vingt-neuf d’entre eux ont obtenu une RMM et onze, une réponse moléculaire soutenue (RM4) (figure 2).
La dose d’asciminib de certains patients a été majorée conformément au protocole de l’étude, mais ils n’ont pas été suivis depuis assez longtemps pour qu’il soit possible d’estimer la fréquence à laquelle une telle augmentation s’impose. Jusqu’à maintenant, selon la définition donnée à l’échec thérapeutique, le traitement n’a échoué chez aucun patient pas plus qu’il n’a justifié l’ajout d’un ITK.
Les patients affichant une résistance primaire ont besoin d’une solution de rechange aux ITK
Le Dr Hugues croit que l’intérêt pour l’emploi de l’asciminib en première ligne vient surtout de la minorité de patients atteints de LMC qui présentent une résistance primaire aux ITK ou qui ne les supportent pas. Aucun cas de résistance à l’asciminib n’a été rapporté pendant l’étude ASCEND-CML et son innocuité y était encourageante. Les effets indésirables de grade ≥ 3 étaient les suivants : thrombopénie (5,4 %), neutropénie (6,5 %), anémie (2,2 %) et anomalies des lipases (6,5 %). Les abandons pour cause d’effets indésirables, qui sont tous survenus pendant les 3 premiers mois de traitement, étaient motivés par des hausses des taux de lipase ou d’amylase (3 patients) et par une thrombopénie (1 patient).
« Il se peut que les cytopénies et les hausses des taux de lipase soient des effets de classe des inhibiteurs de l’ABL1, mais aucune occlusion vasculaire n’a été observée jusqu’à maintenant », a affirmé le Dr Hughes en ajoutant qu’il est prévu de prolonger le suivi.
Objectif : augmenter les taux de réponse moléculaire profonde (RMP) à 5 ans
Quant à une autre application possible de l’asciminib dans les cas de LMC, une étude ouverte multicentrique a répartition aléatoire intitulée ASC4MORE a porté sur des stratégies visant à augmenter les taux de RMP chez des patients ayant amorcé un traitement par de l’imatinib auquel il était prévu d’ajouter l’inhibiteur « STAMP » ou que l’on pouvait remplacer par du nilotinib. Quatre stratégies ont été évaluées au terme d’une répartition aléatoire menée selon un rapport 1:1:1:1. L’étude visait essentiellement à obtenir une RMP (RM4,5) à 48 semaines.
« Nous savons que les ITK de deuxième génération permettent à plus de patients d’obtenir une RMP que l’imatinib. Pourtant de 30 à 60 % des patients n’y parviennent pas, même après 5 ans de traitement », a expliqué le Dr Jorge Cortes, directeur du Centre de cancérologie de la Géorgie, à Augusta, en Géorgie. Il a laissé entendre que les patients ont besoin d’options thérapeutiques sûres, efficaces et utilisables dès les premiers traitements pour qu’un plus grand nombre d’entre eux obtiennent une RMP durable. »
« De 30 à 60 % des patients traités par un ITK de deuxième génération n’obtiennent pas de RMP, même après 5 ans de traitement. »
Lors de l’étude ASC4MORE, les 84 patients prenant 400 mg d’imatinib une fois par jour en première ligne qui n’avaient toujours pas obtenu une RMP au bout d’une année de traitement ont été répartis aléatoirement de façon à recevoir en appoint 40 mg ou 60 mg d’asciminib une fois par jour, à poursuivre leur traitement par l’imatinib ou à le remplacer par 300 mg de nilotinib deux fois par jour.
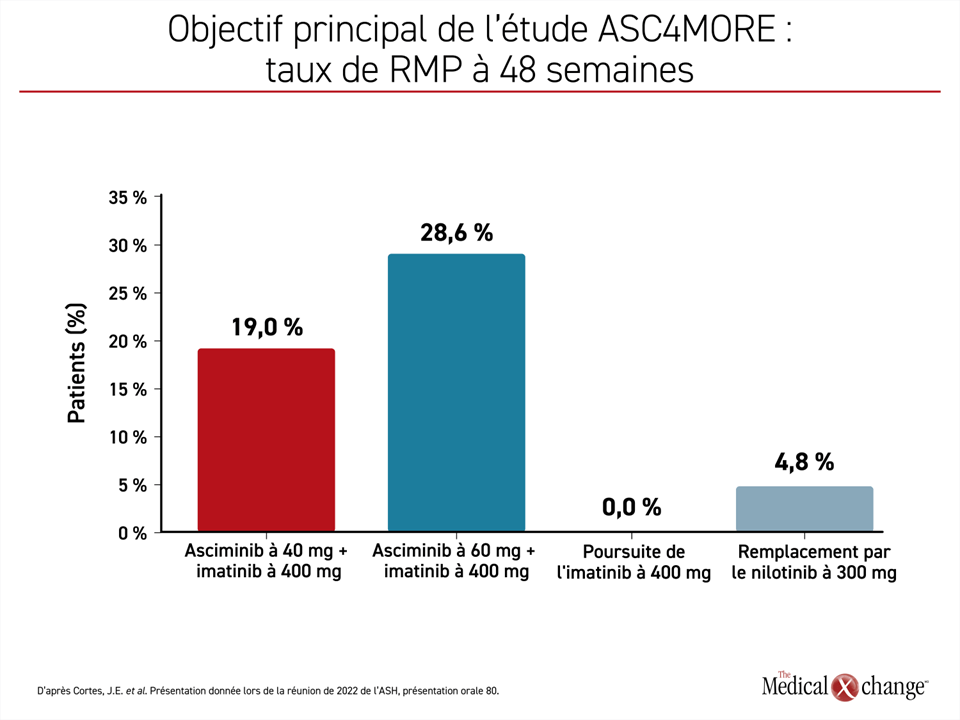
L’objectif principal a été atteint à la 48e semaine, une RMP ayant été observée chez 19,0 % et 28,6 % des sujets affectés à l’asciminib à 40 mg et à 60 mg en appoint, 0 % de ceux ayant poursuivi leur traitement par l’imatinib en monothérapie et 4,8 % de ceux passés au nilotinib (figure 3). Le délai médian écoulé pour y parvenir a été de 12,1 et de 12,4 semaines dans les groupes asciminib à 40 et à 60 mg en appoint et de 24,6 semaines dans le groupe passé au nilotinib.
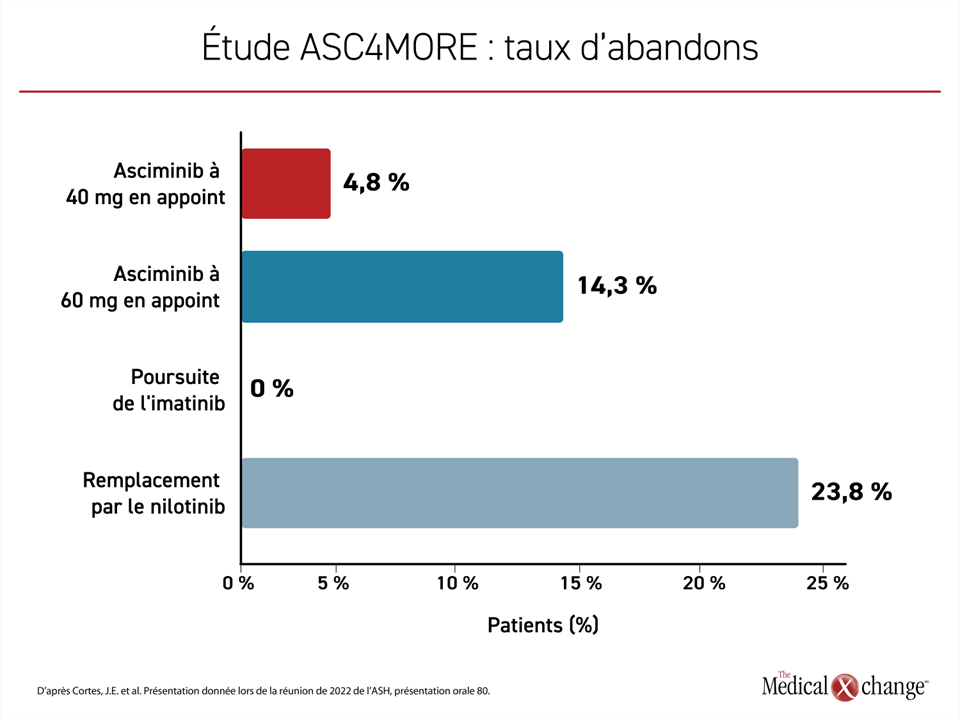
Comparativement à la poursuite du traitement par l’imatinib à 400 mg utilisé seul, les trois autres schémas thérapeutiques ont été reliés à un taux d’effets indésirables plus élevé. Cela dit, le taux d’effets indésirables de grade ≥ 3 et le taux d’abandons ont été plus faibles dans les groupes recevant de l’asciminib en appoint que dans le groupe nilotinib (figure 4). À la date butoir fixée pour la collecte des données, 85,7 % et 76,2 % des sujets des groupes asciminib à 40 mg et à 60 mg en appoint suivaient toujours leur traitement par rapport à 61,9 % des sujets passés au nilotinib et à 23,8 % de ceux ayant continué à prendre de l’imatinib en monothérapie.
Peu d’abandons du traitement par l’inhibiteur « STAMP »
« Grâce à une d’exposition médiane d’une plus longue durée, nous pouvons constater que l’asciminib utilisé en appoint a entraîné moins d’effets indésirables graves et d’abandons du traitement pour cause d’effets indésirables que le nilotinib », a rapporté le Dr Cortes, notant au passage que la tolérabilité est importante pour la qualité de vie des patients et pour faire en sorte que ces derniers n’abandonnent pas leur traitement.
« Cette étude n’était pas dotée de la puissance nécessaire pour découvrir le traitement permettant le mieux d’obtenir une RMP chez les patients affichant une réponse insuffisante à l’imatinib, mais le taux élevé de RMP observé avec l’asciminib en appoint est prometteur, surtout s’il est employé chez des patients incapables d’obtenir une telle réponse après une année ou plus de traitement de première ligne avec cet ITK », a souligné le Dr Cortes.
« Le taux élevé de RMP observé avec [l’inhibiteur « STAMP »] en appoint est prometteur, surtout s’il est employé chez des patients incapables d’obtenir une telle réponse après une année ou plus de traitement de première ligne avec cet ITK. »
Évaluation de l’inhibiteur « STAMP » en première ligne
Les chercheurs de l’étude ASC4MORE prévoient maintenant ajouter un groupe de sujets traités par l’asciminib en monothérapie à leur étude. Le Dr Cortes croit cependant que deux études en cours, soit les études ASC4FIRST et ASC4START nous en apprendront beaucoup plus sur la possibilité d’utiliser l’inhibiteur « STAMP » comme traitement de première ligne de la LMC, puisqu’elles servent toutes les deux à étudier cet agent dans un tel contexte et qu’elles comportent des paramètres d’évaluation de son efficacité. Toutefois, l’étude ASC4START, qui est menée chez des patients atteints d’une LMC-PC Ph+ nouvellement diagnostiquée affectés aléatoirement à l’asciminib ou au nilotinib, porte essentiellement sur la tolérabilité, son paramètre d’évaluation principal étant le temps écoulé avant l’abandon du traitement pour cause d’effets indésirables.
« L’arsenal thérapeutique opposé à la LMC évolue. Bien que la rémission sans traitement soit l’objectif ultime du traitement, il est désormais envisageable d’obtenir une maîtrise de la maladie alliée à une qualité de vie acceptable grâce à un éventail plus large d’options thérapeutiques », a déclaré le Dr Cortes.
Conclusion
L’asciminib, premier agent d’une nouvelle classe thérapeutique, est aujourd’hui offert pour le traitement de troisième ligne de la LMC. Or ses caractéristiques uniques laissent entrevoir la possibilité de l’utiliser plus tôt. L’asciminib cible très précisément le gène BCR-ABL1 sur un site de liaison qui semble générer moins de résistance. Il pourrait même se révéler plus actif que les ITK de deuxième génération pour produire une RMM rapidement, un facteur pronostic que l’on sait important. Les études en cours permettront de positionner cet agent en regard des autres options thérapeutiques visant à obtenir une RMP rapidement et durablement.