cardiologie
Insuffisance cardiaque : revue d'experts et commentaires tirés de la littérature
Comment prolonger la survie dans les cas d’insuffisance cardiaque au Canada
Eileen O’Meara, M.D., FRCP(C)
Cardiologue, Institut de cardiologie de Montréal
Professeur de médecine, Université de Montréal
Montréal (Québec)
Nathaniel Hawkins, MBChB, M.D., MPH
Professeur agrégé de clinique, Université de la Colombie-Britannique
Centre d’innovation cardiovasculaire de l’Université de la C.-B.
Vancouver (Colombie-Britannique)
Quatre classes de médicaments préconisées dans les lignes directrices (CMPLD) auraient un effet positif sur la survie des patients atteints d’insuffisance cardiaque à fraction d’éjection réduite (ICFEr) et conviendraient toutes les quatre à la plupart de ces patients selon une analyse du Registre canadien sur l’insuffisance cardiaque (CAN-HF) de 2023 publiée récemment1. Or, dans les faits, beaucoup d’entre eux ne bénéficient même pas d’une de ces CMPLD et sont donc une source constante de décès évitables au Canada. L’inhibiteur de l’angiotensine allié à un inhibiteur de la néprilysine (ARNI), qui forme à lui seul une des quatre CMPLD, a été reconnu comme le grand oublié, mais il n’est pas seul. Les quatre CMPLD (bêtabloquants [BB], antagonistes des récepteurs minéralocorticoïdes [ARM], ARNI et inhibiteurs du cotransporteur sodium-glucose de type 2 [iSGLT2]) exercent des bienfaits majeurs sur la morbidité et la mortalité indépendamment des trois autres. Elles sont donc toutes essentielles à la réduction optimale du risque.
Contexte
Les études phares à répartition aléatoire des 30 dernières années ont confirmé que quatre classes de médicaments prolongent la survie dans les cas d’insuffisance cardiaque (IC) à fraction d’éjection ventriculaire gauche (FEVG) de 40 % ou moins. Si la Société canadienne de cardiologie (SCC) préconise une classe de médicaments quelconque dans ses plus récentes lignes directrices, c’est en raison de ces études2. Les bienfaits de trois des classes de médicaments actuellement offertes pour améliorer la survie dans les cas d’ICFEr, soit les iECA, les BB et les ARM, ont été établis entre la fin des années 1980 et le début des années 2000. Deux autres classes s’y sont greffées dernièrement, l’ARNI qui a supplanté les iECA et les iSGLT2; les CMPLD actuelles restent donc au nombre de quatre.
Pour une entrevue exclusive avec la Dre Eileen O’Meara couvrant l’impact sur la pratique clinique, cliquez ici
Lors d’études phares, la première classe de médicaments à s’être montrée supérieure aux traitements types comme les vasodilatateurs et les diurétiques pour prolonger la survie a été celle des iECA3,4. Les BB les ont rejoints comme CMPLD après avoir prolongé la survie de patients recevant le traitement type additionné d’un iECA comparativement à un placebo5. De même, les ARM, la troisième classe, ont quant à eux été reliés à des gains pour la survie indépendants de ceux des iECA et des BB6. Les antagonistes des récepteurs de l’angiotensine (ARA) ont ensuite été reconnus comme des remplaçants acceptables des iECA en cas d’intolérance ou de contre-indications7. Ces deux types d’agents sont souvent réunis sous l’appellation d’inhibiteurs du système rénineangiotensine (iSRA) dans les lignes directrices, dont celles de la SCC.
En 2017, des lignes directrices sur l’IC, dont celles de la SCC, ont été actualisées de façon à y intégrer l’ARNI après que son ajout aux autres CMPLD déjà établies ait permis de prolonger encore plus la survie8. L’étude déterminante qui a motivé cette actualisation est l’étude PARADIGM-HF (2014), qui a démontré la supériorité de l’ARNI (sacubitril-valsartan) sur un iECA9. Le sacubitril, un inhibiteur de la néprilysine, empêche l’activation de processus neurohormonaux favorisant le remodelage cardiaque, alors que le valsartan, un ARA, fait partie de la classe des iSRA au même titre que les iECA10. Lors de l’étude PARADIGM-HF, l’ARNI a eu l’avantage sur l’énalapril, un iECA, pour ce qui est de la survie chez des patients atteints d’ICFEr traitée au moyen des CMPLD établies que sont les BB et les ARM.
La SCC a de nouveau apporté des changements aux CMPLD dans ses lignes directrices les plus récentes à la lumière d’études portant sur des iSGLT22. Lors des études DAPA‑HF et EMPEROR-Reduced, qui ont respectivement porté sur la dapagliflozine et l’empagliflozine11,12, l’ajout d’un iSGLT2 a prolongé la survie et réduit les hospitalisations pour IC de patients qui étaient déjà traités par trois CMPLD (BB, ARM, ARNI ou iSRA) comparativement à un placebo. L’iSGLT2, qui s’était déjà révélé efficace pour prévenir l’IC chez des patients atteints de diabète13, a fait montre de sa polyvalence dans ces deux études en permettant de maîtriser l’IC et en confirmant les bienfaits cliniques de ces agents, et ce même chez les patients atteints d’IC avec FEVG supérieure à 40 % 14.
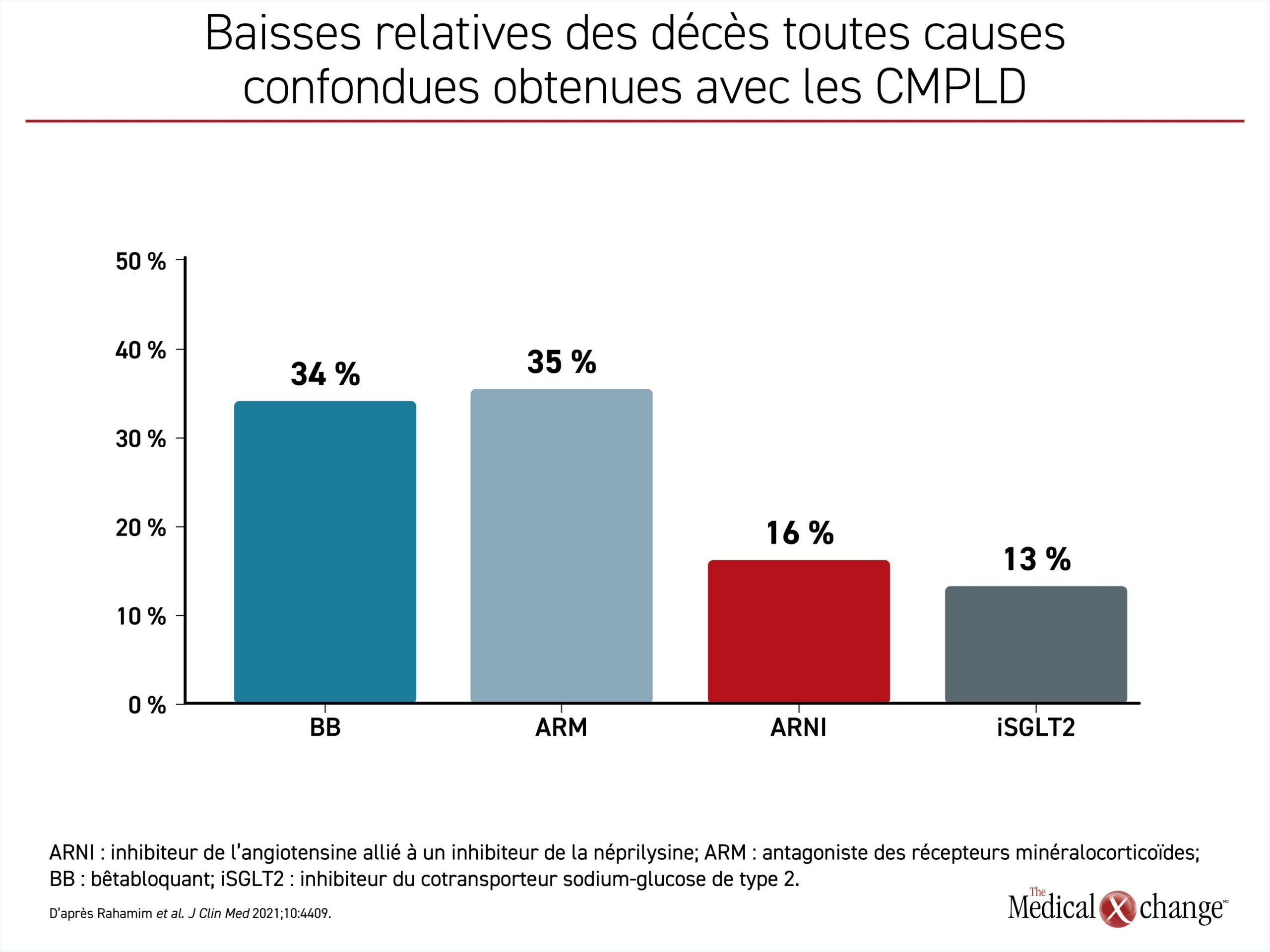
Les effets additifs des médicaments sont un concept fondamental pour qui veut réduire la mortalité et la morbidité de façon optimale. Toutes les études cliniques phares imposaient le recours aux traitements de fond jugés optimaux à l’époque. Chaque fois que les CMPLD se sont enrichies, au moins une étude clinique d’envergure avait révélé que l’agent ajouté avait réduit le nombre des décès indépendamment des CMPLD antérieures. Ces gains supplémentaires correspondaient à environ 15 à 30 % de ceux produits par les CMPLD antérieures (Figure 1)15. Exception faite des rares patients auxquels certains agents des CMPLD ne conviennent pas, le meilleur moyen de prolonger la vie dans les cas d’ICFEr consiste à utiliser les quatre CMPLD simultanément. Aucune ne doit être laissée de côté et toutes doivent être administrées le plus tôt possible.
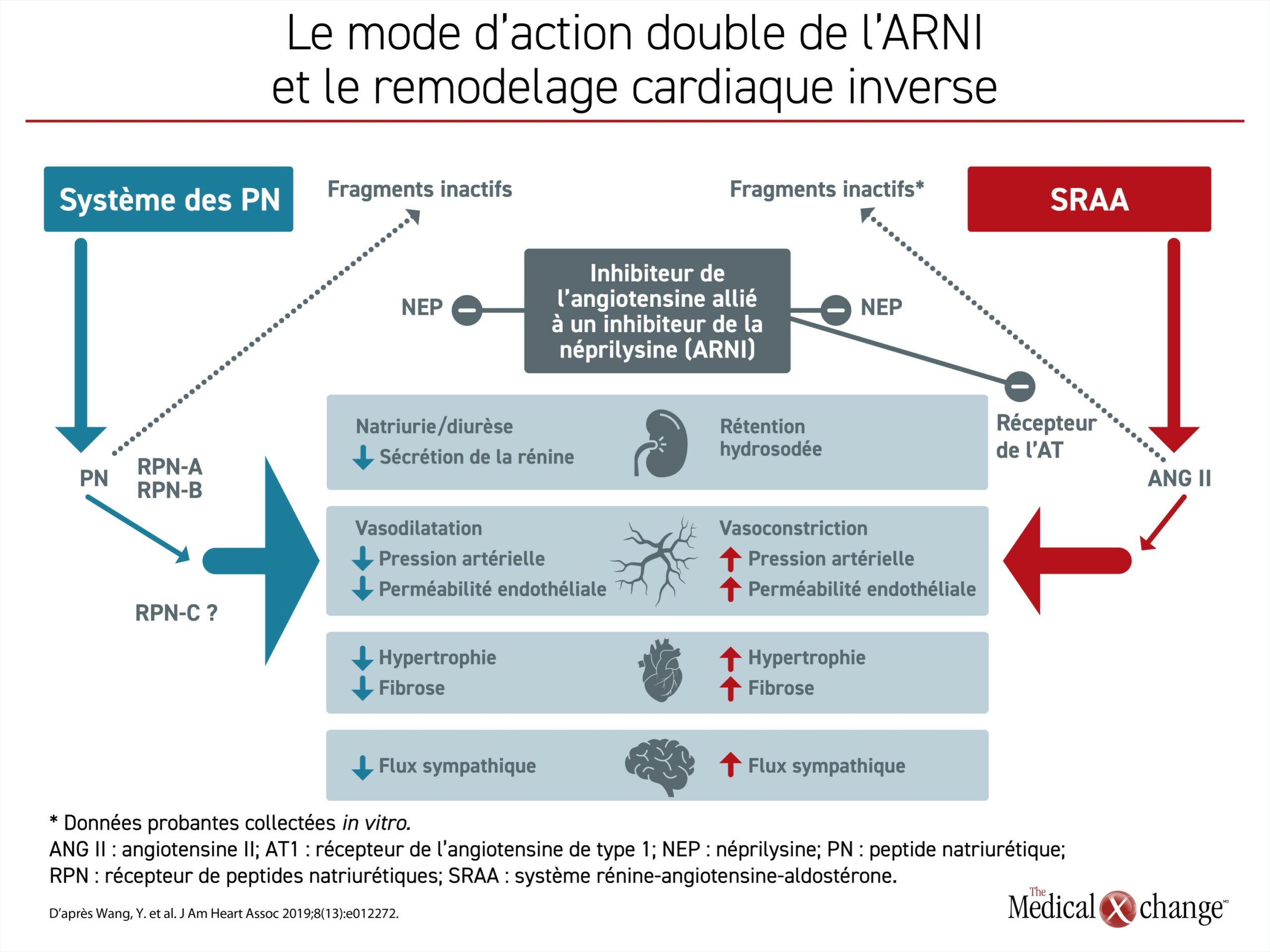
Ces effets positifs sont logiques, car les CMPLD modulent des mécanismes physiopathologiques différents favorisant l’aggravation de l’IC, d’où leur effet positif additif. Les BB ciblent surtout le système nerveux sympathique18, les ARM inhibent l’aldostérone, qui intervient dans la pathogenèse de la fibrose cardiovasculaire19, et les iSRA ont pour cible l’angiotensine, un médiateur de la vasoconstriction20. Chacun d’eux, entre autres effets, bloque les principales voies du remodelage cardiaque. Si l’ARNI a l’avantage sur les iSRA, c’est parce qu’il agit sur deux fronts21 : l’inhibition de l’angiotensine et le blocage de la néprilysine, une enzyme qui dégrade les peptides natriurétiques. Ces deux actions inhibent la régulation positive neurohormonale qui participe au remodelage cardiaque (Figure 2)21. Les iSGLT2 permettent aussi d’améliorer directement et indirectement le sort des patients atteints d’IC en agissant sur plusieurs voies faisant intervenir des effets rénaux, la fonction vasculaire et des médiateurs du stress cardiaque22.
Registre CAN-HF : des décès évitables sont imputables à l’adoption sous-optimale des CMPLD
Des études antérieures, dont celles menées au Canada, nous ont appris que les CMPLD ne sont pas systématiquement prescrites dans les cas d’ICFEr même si leurs bienfaits sur la survie sont parfaitement définis. En effet, bon nombre des 3500 patients atteints d’ICFEr inscrits au registre étatsunien CHAMP-HF ne se sont pas fait prescrire l’ARNI, de bêtabloquants ou d’ARM (86 %, 33 % et 67 %, respectivement)23. Une enquête pancanadienne a révélé que plus de 85 % des patients ne prenaient toujours pas l’ARNI un an après que cet agent ait été intégré aux lignes directrices canadiennes sur l’IC à titre de CMPLD fondamentale24. Les auteurs ont non seulement conclu que cette omission se soldait par des décès évitables, mais qu’elle générait en plus des coûts annuels estimés à 40 millions de dollars en hospitalisations évitables motivées par une IC.
Selon des études récentes sur l’emploi des CMPLD en pratique clinique, le problème est toujours là1. Alors que l’IC, la plus grande cause de décès d’origine cardiovasculaire au Canada, est diagnostiquée chez plus de 100 000 personnes chaque année25, une étude des données du registre CAN-HF est venue confirmer les observations selon lesquelles la majorité des patients atteints d’ICFEr sont admissibles aux quatre CMPLD, mais qu’une forte proportion d’entre eux n’en reçoit pas même pas une1.
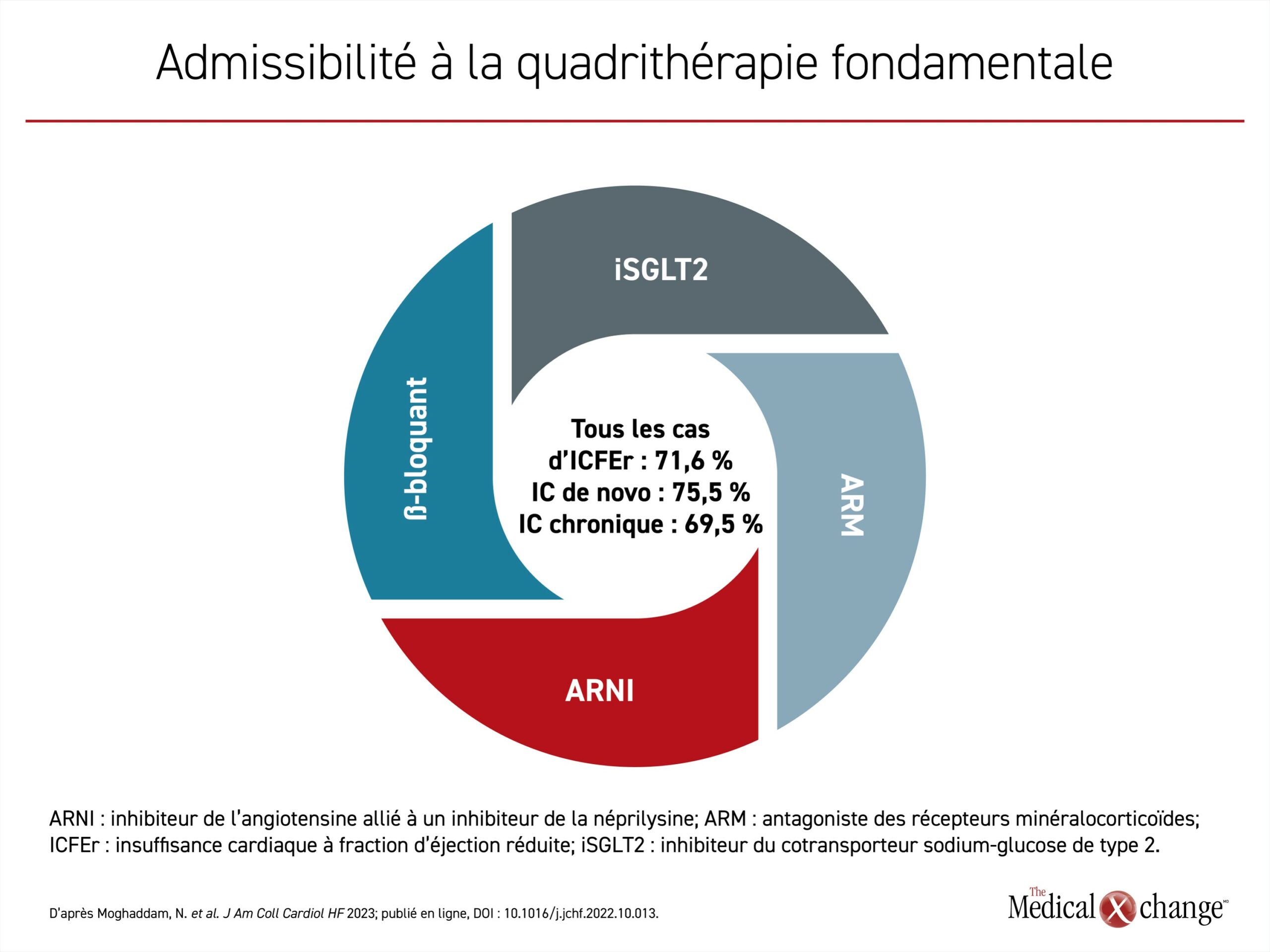
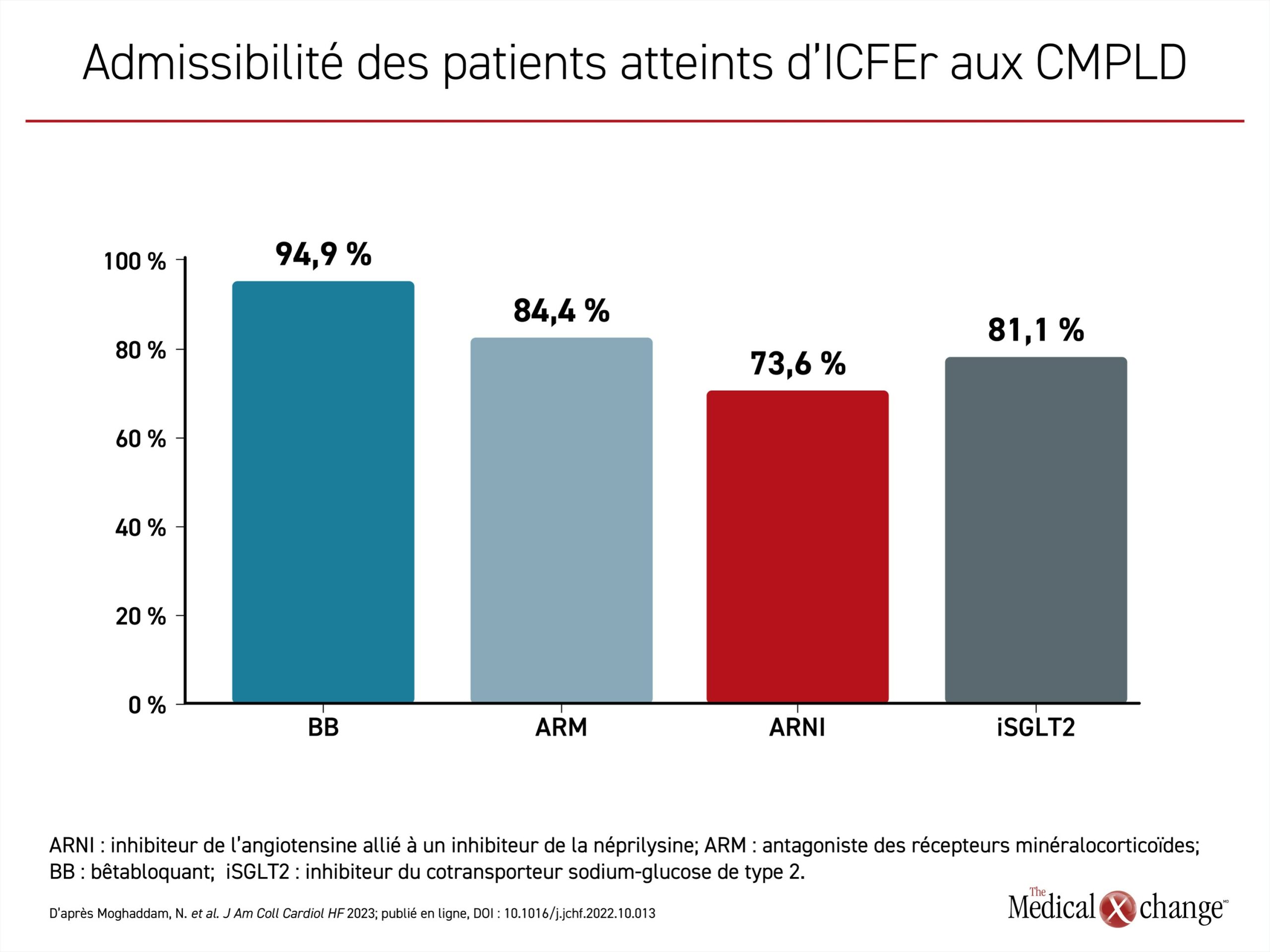
Cette étude a servi à évaluer 809 patients atteints d’IC nouvellement diagnostiquée et traitée dans sept établissements canadiens sur une période de 3 ans (2017‑2020)1. De ce nombre, 455 (56 %) étaient atteints d’ICFEr définie d’après une fraction d’éjection ventriculaire gauche (FEVG) de 40 % ou moins, la FEVG des autres étant supérieure à 40 %. La grande majorité des patients atteints d’ICFEr avaient reçu leur diagnostic depuis peu (de novo) ou avaient des antécédents de cette maladie (chronique), et auraient pu recevoir les traitements fondamentaux. Les quatre CMPLD auraient en effet pu convenir à 75,5 % de tous les cas de novo et à 69,5 % des cas d’ICFEr chronique (Figure 3). Chez les patients hospitalisés pour cause d’ICFEr, le taux d’admissibilité à l’instauration d’un traitement par l’ARNI s’élevait à 73,6 %, à 94,9 % pour les bêtabloquants, à 84,4 % pour les ARM et à 81,1 % pour les iSGLT2 (Figure 4).
Les motifs expliquant le plus souvent qu’un patient inscrit au registre CAN-HF ne puisse pas recevoir au moins une des quatre CMPLD étaient l’hypotension et un dysfonctionnement rénal. Les agents des quatre CMPLD exercent un effet hypotenseur plus ou moins marqué qui peut être préoccupant pour certains patients, mais le risque d’hypotension est probablement insuffisant chez la plupart d’entre eux pour les priver des bienfaits possibles sur la survie d’un traitement optimisé par les CMPLD. En outre, il ne faut pas négliger la possibilité que ces agents amplifient la baisse de la clairance de la créatinine. Cela dit, l’évaluation du risque d’hypotension et d’insuffisance rénale devrait permettre de concevoir un plan de traitement qui autorise l’utilisation d’agents des quatre CMPLD chez la plupart des patients. Conclusion : il est souvent possible d’éviter de priver les patients d’un traitement susceptible de leur sauver la vie.
Selon l’ensemble des données, il se peut que les cliniciens n’adhèrent pas au consensus dégagé par les experts, qui recommande d’amorcer un traitement par les quatre CMPLD avant le départ des patients de l’hôpital, sauf chez ceux que l’on sait présenter des contre-indications. Or cela contrevient aux lignes directrices canadiennes de 2021 qui préconisent, en l’absence de contre-indications, l’instauration d’un traitement comportant un agent de chacune des CMPLD appuyé par des données probantes le plus tôt possible après le diagnostic2.
Les modifications aux lignes directrices mettent l’accent sur une instauration rapide du traitement
Les lignes directrices canadiennes de 2021 décrivent plusieurs stratégies pour aider les cliniciens à amorcer rapidement un traitement par les CMPLD, mais aussi pour souligner l’importance d’éliminer le moindre retard2. Jusqu’en 2017, il était fréquent d’y aller graduellement en faisant appel aux CMPLD une à une, en commençant par les iSRA et en les faisant suivre par les autres CMPLD plus ou moins l’ordre dans lequel elles ont été reconnues comme telles. La lenteur de ce processus d’ajout et d’ajustement des doses retardait l’optimisation du traitement et risquait fort d’entraîner des problèmes. Quand l’ARNI est devenu une CMPLD en 2017, le risque de retard était encore plus grand, puisqu’il fallait sevrer les patients de l’iECA qu’ils prenaient déjà, sans compter que la menace d’un oedème de Quincke provoqué par le remplacement précipité de l’iECA par l’ARNI commandait une pause de 36 heures entre le moment où le patient commençait à prendre l’ARNI et celui où il cessait de prendre son iECA. Cette pause est inutile chez les patients prenant déjà un ARA, mais cette étape supplémentaire pour passer de l’iECA à l’ARNI était très souvent vue comme un frein à la prescription rapide de l’ARNI ou pire encore, une incitation à l’omettre une fois l’ICFEr diagnostiquée1,23,24. Les dernières lignes directrices canadiennes insistent sur l’importance d’entreprendre rapidement un traitement par les quatre CMPLD et d’en régler la posologie dans les meilleurs délais2.
Les lignes directrices citent l’étude PIONEER-HF pour appuyer l’intérêt de la prescription rapide de l’ARNI12 qui est maintenant vu comme un agent à utiliser en première intention pendant l’hospitalisation2. Cette étude à répartition aléatoire a permis d’observer de meilleurs résultats, notamment une diminution des réhospitalisations motivées par l’IC chez des patients hospitalisés pour cause d’ICFEr quand l’ARNI commençait à leur être administré avec des CMPLD plutôt qu’un iECA, l’énalapril, administré avec des CMPLD (groupe témoin). La modulation neurohormonale instantanée observée avec l’amorce rapide de l’ARNI s’est traduite par une baisse immédiate des taux élevés de NT-proBNP, un biomarqueur de l’activation neurohormonale, d’un stress hémodynamique et d’incidents cardiovasculaires à venir.
En 2021, la mise à jour d’un arbre décisionnel consensuel créé pour l’ICFEr par l’American College of Cardiology (ACC) et publié conjointement en 2017 par l’ACC et l’American Heart Association (AHA) allait dans le même sens26. Les lignes directrices de 2017 de l’ACC et de l’AHA formulaient les mêmes recommandations relativement aux CMPLD que la version 2017 des lignes directrices canadiennes 2,27, mais la version mise à jour en 2021, tout comme celle des lignes directrices canadiennes effectuée la même année, s’attaque en plus aux retards dans l’instauration et le réglage posologique des CMPLD.
Autre parallèle avec les lignes directrices canadiennes de 2021, la version de l’ACC de 2021 qualifie l’instauration immédiate d’un traitement par l’ARNI de sûre et d’efficace chez les patients qui n’ont pas encore reçu un iSRA26. Quant aux patients prenant déjà un iECA, la recommandation d’un sevrage de 36 heures tient toujours, mais les deux séries de lignes directrices stipulent que cette étape ne doit pas justifier que l’on retarde l’amorce du traitement par l’ARNI.
Bienfaits globaux des CMPLD
Bien qu’il ait été démontré à maintes reprises que l’ARNI est la CMPLD la plus souvent omise dans la pratique courante actuelle, la situation presse aussi pour les autres agents, y compris les inhibiteurs du SGLT2, la plus récente classe de médicament qui s’est jointe aux CMPLD opposées à l’ICFEr. Lors de l’étude à double insu EMPULSE, des patients hospitalisés en raison d’une IC aiguë ont été répartis aléatoirement de façon à recevoir de l’empagliflozine ou un placebo28. Compte tenu du paramètre d’évaluation principal hiérarchisé composé des décès toutes causes confondues, des incidents liés à l’IC et du temps écoulé avant la survenue de tels incidents, le taux de réussite de 1,36 attribué à l’instauration rapide d’un traitement par un inhibiteur du SGLT2 était extrêmement significatif par rapport au placebo (p = 0,0054). Cette étude ne portait pas uniquement sur l’ICFEr et l’effet positif a été observé, peu importait la fraction d’éjection.
Lors de l’étude SOLOIST-WHF, plus de 1200 patients atteints de diabète et d’IC ont été répartis aléatoirement de façon à recevoir de la sotagliflozine (un inhibiteur combiné SGLT1/SGLT2) ou un placebo avant leur départ de l’hôpital (48,8 %) ou une médiane de 2 jours après leur départ (51,2 %)29. Bien que cette étude ait été interrompue par manque de fonds, l’instauration rapide d’un traitement par la sotagliflozine a été reliée à un nombre significativement moins élevé de décès d’origine cardiovasculaire et de visites aux urgences motivées par l’IC comparativement au placebo, le paramètre d’évaluation principal.
Si on insiste autant sur l’instauration et le réglage posologique rapides des CMPLD dans les cas d’ICFEr, c’est en raison des données prouvant leurs bienfaits cumulatifs. Une méta-analyse portant sur 75 études réalisées chez près de 100 000 patients a permis d’établir un parallèle entre l’association formée d’un iECA, d’un BB, d’un ARM, de l’ARNI et d’un iSGLT2 et une baisse de plus de 60 % des décès toutes causes confondues, assortie d’un intervalle de confiance étroit (RRI : 0,39; IC à 95 % : de 0,31 à 0,49) comparativement à l’absence de traitement17. Cette association a été reliée à des réductions similaires du risque de décès d’origine cardiovasculaire et d’hospitalisation pour cause d’IC.
Une analyse comparative visant à évaluer les répercussions de l’utilisation d’un plus ou moins grand nombre de CMPLD a révélé que la réduction des décès toutes causes confondues frôlait les 50 % pour une association composée de 3 agents versus une autre formée de 2 agents (RRI : 0,53; IC à 95 % : de 0,40 à 0,70)16. Selon les estimations, les baisses obtenues pour les hospitalisations motivées par l’IC et plusieurs paramètres d’évaluation combinés, tels que les décès d’origine cardiovasculaire et les hospitalisations motivées par l’IC, étaient comparables. Au vu de ces données, on a estimé que l’association formée des quatre agents permet de prolonger la survie d’un patient de 55 ans atteint d’ICFEr de 6,3 années en moyenne.
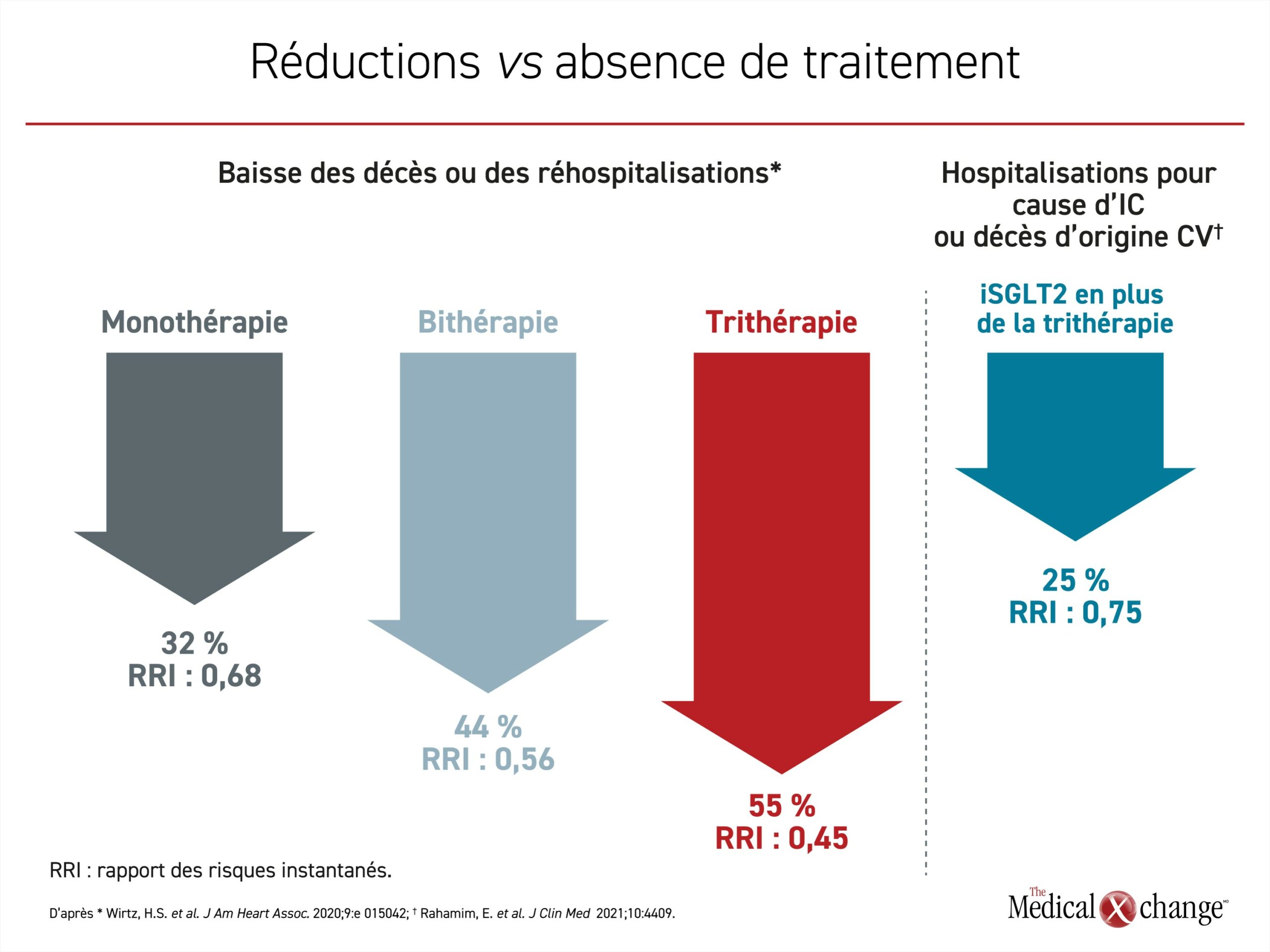
Une analyse observationnelle rétrospective réalisée en pratique clinique sur les CMPLD administrées après une hospitalisation pour cause d’IC, a révélé que le risque lié au paramètre d’évaluation principal composé du décès ou d’une réhospitalisation motivée par l’IC suivant un traitement à l’aide de trois CMPLD (BB, ARM, ARNI ou iSRA) baissait de 55 % comparativement à l’absence de traitement (RRI : 0,45; IC à 95 % : de 0,41 à 0,50)30. Elle a aussi fait ressortir une réduction graduelle du paramètre d’évaluation avec la monothérapie (32 %), la bithérapie (44 %) et la trithérapie (55 %) (Figure 5).
Comme les bienfaits de ces agents ne sont pas aussi bien cernés chez les patients atteints d’insuffisance cardiaque à fraction d’éjection préservée (ICFEp), ou une FEVG supérieure à 40 %, les auteurs de l’analyse du registre CAN-HF ont également recherché des effets positifs qui seraient passés sous le radar chez ces patients1. Or ils ont estimé d’après les l’étude PARAGON-HF et TOPCAT31,32, que l’ARNI et les ARM pourraient convenir à jusqu’à 50 % et 80 % de ces patients, respectivement. Les auteurs ont toutefois insisté sur la nécessité de réaliser de nouvelles analyses afin d’optimiser la sélection des patients pour ces traitements tout en affirmant que la médecine factuelle a ce qu’il faut pour multiplier les moyens d’améliorer le sort des patients hospitalisés en raison d’une insuffisance cardiaque aiguë.
Les données probantes fournies dans les documents récents, dont l’analyse publiée dernièrement, les lignes directrices canadiennes de 2021 et l’arbre décisionnel consensuel de l’ACC actualisé en 2021, prêchent toutes pour une prise en charge musclée de l’ICFEr2,26. Plutôt que d’opter pour une démarche graduelle classique, il faut donc entreprendre un traitement par les quatre CMPLD le plus tôt possible, même durant l’hospitalisation de référence, et ensuite tenter d’atteindre les doses cibles rapidement. Dans l’ensemble, les agents appartenant aux CMPLD sont bien tolérés et sûrs lorsque les schémas posologiques habituels sont respectés. L’obtention de gains optimaux pour la survie repose donc sur l’utilisation des quatre CMPLD chez les patients qui y sont admissibles.
Résumé
Chacune des quatre classes de médicaments fondamentales proposées pour traiter l’ICFEr permet de prolonger la survie indépendamment des trois autres et est bien expliquée dans les lignes directrices. Cela dit, selon l’analyse du registre CAN-HF effectuée et publiée récemment, les retards que connaissent l’amorce du traitement et l’atteinte des doses cibles entraîneraient des décès évitables. Fréquemment, lorsque l’ICFEr n’est pas bien prise en charge, c’est que les iSRA ne sont pas remplacés par l’ARNI ou parce qu’un traitement par un iSGLT2 n’est pas amorcé rapidement. Cependant, le recours aux agents des autres CMPLD est souvent différé ou n’est pas optimisé assez vite, d’où le risque de décès évitables.
Références
- Moghaddam N, Hawkins NM, McKelvie R, Poon S. Patient eligibility for established and novel guideline-directed medical therapies after acute heart failure hospitalization. JACC HF 2023;11;S2213-1779(22)00638-2.DOI: 10.1016/j.jchf.2022.10.013.
- McDonald M, Virani S, Chan M, et al. CCS/CHFS Heart Failure Guidelines Update: Defining a New Pharmacologic Standard of Care for Heart Failure With Reduced Ejection Fraction. Can J Cardiol 2021;37(4):531-546. DOI: 10.1016/j.cjca.2021.01.017.
- Investigators S, Yusuf S, Pitt B, Davis CE, Hood WB, Cohn JN. Effect of enalapril on survival in patients with reduced left ventricular ejection fractions and congestive heart failure. N Engl J Med 1991;325(5):293-302. DOI: 10.1056/NEJM199108013250501.
- Pfeffer MA, Braunwald E, Moye LA, et al. Effect of captopril on mortality and morbidity in patients with left ventricular dysfunction after myocardial infarction. Results of the survival and
ventricular enlargement trial. The SAVE Investigators. N Engl J Med 1992;327(10):669-77. DOI: 10.1056/NEJM199209033271001. - Lechat P, Packer M, Chalon S, Cucherat M, Arab T, Boissel JP. Clinical effects of beta-adrenergic blockade in chronic heart failure: a metaanalysis of double-blind, placebo-controlled, randomized trials. Circulation 1998;98(12):1184-91. DOI: 10.1161/01.cir.98.12.1184.
- Zannad F, Gattis Stough W, Rossignol P, et al. Mineralocorticoid receptor antagonists for heart failure with reduced ejection fraction: integrating evidence into clinical practice. Eur Heart J
2012;33(22):2782-95. DOI: 10.1093/eurheartj/ehs257. - Peterson RC, Dunlap ME. Angiotensin II receptor blockers in the treatment of heart failure. Congest Heart Fail 2002;8(5):246-50; 256. DOI: 10.1111/j.1527-5299.2000.01156.x.
- Ezekowitz JA, O’Meara E, McDonald MA, et al. 2017 Comprehensive Update of the Canadian Cardiovascular Society Guidelines for the Management of Heart Failure. Can J Cardiol 2017;33(11):1342-1433. DOI: 10.1016/j.cjca.2017.08.022.
- McMurray JJ, Packer M, Desai AS, et al. Angiotensin-neprilysin inhibition versus enalapril in heart failure. N Engl J Med 2014;371(11):993-1004. DOI: 10.1056/NEJMoa1409077.
- Pascual-Figal D, Bayes-Genis A, Beltran-Troncoso P, et al. Sacubitril-Valsartan, Clinical Benefits and Related Mechanisms of Action in Heart Failure With Reduced Ejection Fraction. A Review. Front Cardiovasc Med 2021;8:754499. DOI: 10.3389/fcvm.2021.754499.
- McMurray JJV, Solomon SD, Inzucchi SE, et al. Dapagliflozin in Patients with Heart Failure and Reduced Ejection Fraction. N Engl J Med 2019;381(21):1995-2008. DOI: 10.1056/NEJMoa1911303.
- Anker SD, Butler J, Filippatos G, et al. Empagliflozin in Heart Failure with a Preserved Ejection Fraction. N Engl J Med 2021;385(16):1451-1461. DOI: 10.1056/NEJMoa2107038.
- Keller DM, Ahmed N, Tariq H, et al. SGLT2 Inhibitors in Type 2 Diabetes Mellitus and Heart Failure-A Concise Review. J Clin Med 2022;11(6). DOI: 10.3390/jcm11061470.
- Vaduganathan M, Docherty KF, Claggett BL, et al. SGLT-2 inhibitors in patients with heart failure: a comprehensive meta-analysis of five randomised controlled trials. Lancet 2022;400(10354):757-767. DOI: 10.1016/S0140-6736(22)01429-5.
- Rahamim E, Nachman D, Yagel O, et al. Contemporary Pillars of Heart Failure with Reduced Ejection Fraction Medical Therapy. J Clin Med 2021;10(19). DOI: 10.3390/jcm10194409.
- Vaduganathan M, Claggett BL, Jhund PS, et al. Estimating lifetime benefits of comprehensive disease-modifying pharmacological therapies in patients with heart failure with reduced ejection fraction: a comparative analysis of three randomised controlled trials. Lancet 2020;396(10244):121-128. DOI: 10.1016/S0140-6736(20)30748-0.
- Tromp J, Ouwerkerk W, van Veldhuisen DJ, et al. A Systematic Review and Network Meta-Analysis of Pharmacological Treatment of Heart Failure With Reduced Ejection Fraction. JACC Heart Fail 2022;10(2):73-84. DOI: 10.1016/j.jchf.2021.09.004.
- Barrese V, Taglialatela M. New advances in beta-blocker therapy in heart failure. Front Physiol 2013;4:323. DOI: 10.3389/ fphys.2013.00323.
- Leopold JA. Aldosterone, mineralocorticoid receptor activation, and cardiovascular remodeling. Circulation 2011;124(18):e466-8. DOI: 10.1161/CIRCULATIONAHA.111.067918.
- Ferrario CM. Cardiac remodelling and RAS inhibition. Ther Adv Cardiovasc Dis 2016;10(3):162-71. DOI: 10.1177/1753944716642677.
- Wang Y, Zhou R, Lu C, Chen Q, Xu T, Li D. Effects of the Angiotensin- Receptor Neprilysin Inhibitor on Cardiac Reverse Remodeling: Meta-Analysis. J Am Heart Assoc 2019;8(13):e012272. DOI: 10.1161/ JAHA.119.012272.
- Lopaschuk GD, Verma S. Mechanisms of Cardiovascular Benefits of Sodium Glucose Co-Transporter 2 (SGLT2) Inhibitors: A State-of-the- Art Review. JACC Basic Transl Sci 2020;5(6):632-644. DOI: 10.1016/j. jacbts.2020.02.004.
- Greene SJ, Butler J, Albert NM, et al. Medical Therapy for Heart Failure With Reduced Ejection Fraction: The CHAMP-HF Registry. J Am Coll Cardiol 2018;72(4):351-366. DOI: 10.1016/j.jacc.2018.04.070.
- Huitema AA, Daoust A, Anderson K, et al. Optimal Usage of Sacubitril/Valsartan for the Treatment of Heart Failure: The Importance of Optimizing Heart Failure Care in Canada. CJC Open 2020;2(5):321-327. DOI: 10.1016/j.cjco.2020.03.015.
- Poon S, Leis B, Lambert L, et al. The State of Heart Failure Care in Canada: Minimal Improvement in Readmissions Over Time Despite an Increased Number of Evidence-Based Therapies. CJC Open 2022;4(8):667-675. DOI: 10.1016/j.cjco.2022.04.011.
- Maddox TM, Januzzi JL, Jr., Allen LA, et al. 2021 Update to the 2017 ACC Expert Consensus Decision Pathway for Optimization of Heart Failure Treatment: Answers to 10 Pivotal Issues About Heart Failure With Reduced Ejection Fraction: A Report of the American College of Cardiology Solution Set Oversight Committee. J Am Coll Cardiol 2021;77(6):772-810. DOI: 10.1016/j.jacc.2020.11.022.
- Yancy CW, Jessup M, Bozkurt B, et al. 2017 ACC/AHA/HFSA Focused Update of the 2013 ACCF/AHA Guideline for the Management of Heart Failure: A Report of the American College of Cardiology/ American Heart Association Task Force on Clinical Practice Guidelines and the Heart Failure Society of America. Circulation 2017;136(6):e137-e161. DOI: 10.1161/CIR.0000000000000509.
- Kosiborod MN, Angermann CE, Collins SP, et al. Effects of Empagliflozin on Symptoms, Physical Limitations, and Quality of Life in Patients Hospitalized for Acute Heart Failure: Results From the EMPULSE Trial. Circulation 2022;146(4):279-288. DOI: 10.1161/ CIRCULATIONAHA.122.059725.
- Bhatt DL, Szarek M, Steg PG, et al. Sotagliflozin in Patients with Diabetes and Recent Worsening Heart Failure. N Engl J Med 2021;384(2):117-128. DOI: 10.1056/NEJMoa2030183.
- Wirtz HS, Sheer R, Honarpour N, et al. Real-World Analysis of Guideline-Based Therapy After Hospitalization for Heart Failure. J Am Heart Assoc 2020;9(16):e015042. DOI: 10.1161/JAHA.119.015042.
- Velazquez EJ, Morrow DA, DeVore AD, et al. Angiotensin-Neprilysin Inhibition in Acute Decompensated Heart Failure. N Engl J Med 2019;380(6):539-548. DOI: 10.1056/NEJMoa1812851.
- Cikes M, Claggett B, Shah AM, et al. Atrial Fibrillation in Heart Failure With Preserved Ejection Fraction: The TOPCAT Trial. JACC Heart Fail 2018;6(8):689-697. DOI: 10.1016/j.jchf.2018.05.005.